
【题目】下列说法中正确的是( )
A.化学反应不一定都有能量变化
B.增大反应物浓度,活化分子百分数增大,化学反应速率一定增大
C.升高温度,活化分子百分数增大,化学反应速率一定增大
D.一般使用催化剂可以降低反应的活化能,增大活化分子百分数,从而提高反应物的转化率
科目:高中化学 来源: 题型:
【题目】将一定量的镁铝合金投入100 mL一定浓度的盐酸中,合金溶解。向所得溶液中滴加5 mol/L NaOH溶液,生成的沉淀质量与加入的NaOH溶液的体积如图所示,由图中数据分析计算,正确的是( )

A. 原合金中镁的质量为9.6g
B. 铝的质量为5.4g
C. 盐酸的物质的量浓度为8mol/L
D. 图像中A点沉淀为Al(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学一选修3:物质结构与性质】X、Y、Z、W四种元素的部分信息如下表所示。
元素 | X | Y | Z | W |
相关 信息 | 短周期元素,最高化合价为 +7价 | 基态原子中,电子占据的最高能层符号为L,最高 能级上只有两个自旋方向相同的电子 | 核外电子共有15种运动状态 | 能与X形成两种常见化合物WX2、WX3,酚遇WX3溶液能发生显色反应 |
回答下列问题:
(1) W的基态原子电子排布式为____, X、Y、Z三种元素电负性由大到小的顺序为___(用具体的元素符号填写)。
(2)化合物YX4、ZX3、ZX5 (气态或液态时)中,中心原子的轨道类型不是sp3杂化的是________(填化学式,下同),分子构型是正四面体的是______, 属于极性分子的是____。
(3)已知WX3的熔点:306℃,沸点:319℃,则WX3的晶体类型为____,Y与氢元素能形成YnH2n+2 (n为正整数)的一系列物质,这一系列物质沸点的变化规律以及影响的因素是______________。
(4)Z可形成多种含氧酸,如H3ZO4、HZO3、H3ZO3等,其中酸性最强的是______(填化学式)。
(5)W元素的单质晶体在不同温度下有两种堆积方式,晶胞分别如下图所示。在面心立方晶胞中W原子的配位数为___;若W的原子半径为r cm,阿伏加德罗常数为NA,则其体心立方晶体的密度可表示为_____gcm-3。
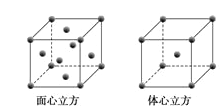
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】发展以煤制乙烯、丙烯、丁烯等低碳烯烃,部分替代石油化工产品的道路是我国保障能源安全战略的重要措施。间接法是先由煤制合成气(组成为H2、CO和少最的CO2)制备甲醇或二甲醚(CH3OCH3),其主要过程包括以下四个反应:
甲醇合成反应:
①CO(g)+2H2(g)![]() CH3OH(g) △H1=-90.1 kJmol-1
CH3OH(g) △H1=-90.1 kJmol-1
②CO2(g)+3H2(g)![]() CH3OH(g) +H2O(g) △H2=-49.0kJmol-1
CH3OH(g) +H2O(g) △H2=-49.0kJmol-1
水煤气变换反应:
③CO(g)+ H2O(g)![]() CO2(g)+ H2(g) △H3=-41.1kJmol-1
CO2(g)+ H2(g) △H3=-41.1kJmol-1
二甲醚合成反应:
④2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H4=-24.5kJmol-1
CH3OCH3(g)+H2O(g) △H4=-24.5kJmol-1
回答下列问题:
(1)分析上述反应(均可逆),发生反应④对于CO转化率的影响是_______(填“增大”、“减小”或“无影响”,其理由是__________。
(2)在二个体积均为1.0L的恒容密闭容器中发生上述二甲醚合成反应④。实验数据见下表:
容器编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |||
CH3OH(g) | CH3OCH3(g) | H2O(g) | CH3OCH3(g) | H2O(g) | ||
a | 387 | 0.20 | 0 | 0 | 0.080 | 0.080 |
b | 387 | 0.40 | 0 | 0 | ||
c | 207 | 0.20 | 0 | 0 | 0.090 | 0.090 |
①387℃时,反应④的化学平衡常数K=__________。
②达到平衡时,容器b中CH3OH的转化率为________。
③达到平衡时,容器c中CH3OCH3的体积分数为________。
(3)由H2和CO可直接制备二甲醚:2CO2(g)+4H2(g)=CH3OCH(g)+H2O(g) ΔH=__________;为提高反应物的转化率,根据化学反应原理,理论上应采取的措施是________(填序号)。
A.高温高压 B.低温低压 C.高温低压 D.低温高压
(4)有研究者用Cu-Zn-Al和Al2O3作催化剂,压强为5.0 MPa的条件下,由合成气[![]() =2]直接制备二甲醚,结果如下图所示.已知:选择性=
=2]直接制备二甲醚,结果如下图所示.已知:选择性=![]() ×100%。则有图可知二甲醚的选择性达最大值时对应的温度是____________。
×100%。则有图可知二甲醚的选择性达最大值时对应的温度是____________。

(5)2016年,我国的两个科研团队在合成气直接制备低碳烯烃(nCO+2nH2![]() CnH2n+nH2O)的研究中连续取得重大突破,论文分别发表在《德国应用化学》(2016.03.16)、《Nature》(2016.10.06)杂志上。
CnH2n+nH2O)的研究中连续取得重大突破,论文分别发表在《德国应用化学》(2016.03.16)、《Nature》(2016.10.06)杂志上。![]() =2时,前者在400℃,1MPa的条件下,CO转化率为11%,低碳烯烃选择性达74%;后者在250℃,0.1~0.5MPa的条件下,CO转化率为31.8%,低碳烯烃选择性为60.8%,则其中低碳烯烃的产率较大者的值为_________。
=2时,前者在400℃,1MPa的条件下,CO转化率为11%,低碳烯烃选择性达74%;后者在250℃,0.1~0.5MPa的条件下,CO转化率为31.8%,低碳烯烃选择性为60.8%,则其中低碳烯烃的产率较大者的值为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
以硅藻土为载体的五氧化二钒(V2O5)是接触法生成硫酸的催化剂。从废钒催化剂中回收V2O5既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为:
物质 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
质量分数/% | 2.2~2.9 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | <1 |
以下是一种废钒催化剂回收工艺路线:
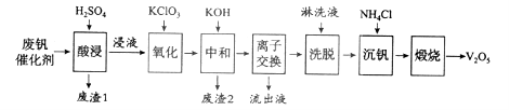
回答下列问题:
(1)“酸浸”时V2O5转化为VO2+,反应的离子方程式为___________,同时V2O4转成VO2+。“废渣1”的主要成分是__________________。
(2)“氧化”中欲使3 mol的VO2+变为VO2+,则需要氧化剂KClO3至少为______mol。
(3)“中和”作用之一是使钒以V4O124形式存在于溶液中。“废渣2”中含有_______。
(4)“离子交换”和“洗脱”可简单表示为:4ROH+ V4O124![]() R4V4O12+4OH(ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈_____性(填“酸”、“碱”或“中”)。
R4V4O12+4OH(ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈_____性(填“酸”、“碱”或“中”)。
(5)“流出液”中阳离子最多的是________。
(6)“沉钒”得到偏钒酸铵(NH4VO3)沉淀,写出“煅烧”中发生反应的化学方程式____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuCl2广泛应用于工业生产,溶于水形成绿色溶液。CuCl晶体呈白色,露置于潮湿空气中易被氧化,实验室用图所示的实验仪器及药品来制备纯净、干燥的氯气并与粗铜(含杂质铁)反应制备氯化铜(铁架台、铁夹及酒精灯省略)。
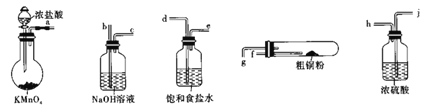
(1)完成上述实验,气流方向连接各仪器接口的顺序是________a→______、____→______、_____→______、 _________→________;反应时,盛粗铜粉的试管中现象是_______________。
(2)实验完毕,取试管中的固体有盐酸溶解后,欲提纯氯化铜,请简述实验方案:_________________。(室温,Fe(OH))3 沉淀完全的pH为3.2)
(3)向制得的氯化铜溶液中通入SO2,加热一段时间既可制得CuCl,写出该反应的离子方式:_______。
(4)已知:ⅰ.CuCl的盐酸溶液能吸收CO形成Cu(CO)Cl·H2O
ⅱ.保险粉(Na2S2O4)和KOH的混合溶液能吸收氧气。
某同学利用如图所示装置,测定某混合气体中H2、CO、SO2和O2的百分组成
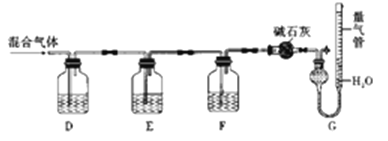
①D瓶测定__________;F洗气瓶中盛放的试剂是__________________。
②E瓶中发生反应的离子方程式为____________________。
③为了准确读取G中量气管的数据,读数时除了视线与凹液面最低处相平以外,还要注意__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z均为短周期主族元素,已知它们的原子序数的关系为X+Z=2Y,且Z的最高价氧化物对应的水化物是强酸。则下列有关说法正确的是
A. 若X是Na,则Z的最高价一定为偶数
B. 若X是O,则YX一定是离子化合物
C. 若Y是O,则非金属性Z>Y>X
D. 若Y是Na,则X、Z不可能是同一主族元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学选修5:有机化学基础]
肉桂酸甲酯是一种重要的食用香精,下图朵合成它的反应路线:
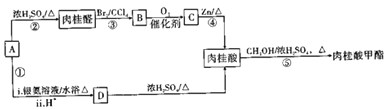
己知:I.芳香族化合物A的分子式为C9H10O2,且只有-个侧链;侧链每个C上最多只有一个官能团;
Ⅱ. lmol A完全催化氧化的产物只能与1molNaOH完全反应
(1) A的结构简式为_______________,肉桂醛的分子式为_______________。
(2)上述合成路线中使用②③步反应的目的是_________________。
(3)第⑤步反应的化学方程式为___________________________。
(4)写出A与银氨溶液反应的化学方程式:_______________________。
(5)D分子中含有多种官能团,不能发生的反应类型有__________(填序号)。
a.酯化反应 b.取代反应 c.加聚反应
d.水解反应 e.消去反应 f.氧化反应
(6) 写出符合下列条件的肉桂醛的同分异构体:_________________(至少3种)。
ⅰ.分子中无甲基
ⅱ.所有碳原子一定在同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积固定的密闭容器中,加入2molA和1molB发生下列反应并且达到化学平衡状态,2A(g)+B(g) ![]() 3C(g)+D(g),平衡时C的浓度为amol·L-1。若维持容器体积和温度不变,按下列4种方法配比作为起始物质充入该容器中,达到平衡后,C的浓度仍为amol·L-1的是( )
3C(g)+D(g),平衡时C的浓度为amol·L-1。若维持容器体积和温度不变,按下列4种方法配比作为起始物质充入该容器中,达到平衡后,C的浓度仍为amol·L-1的是( )
A.4molA+2molB B.3molC+1molB+1molD+1molA
C.2molA+1molB+1molD D.1molA+0.5molB + 1.5molC+0.5molD
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com