
【题目】短周期主族元素X,Y,Z,W原子序数依次增大,m是W的单质,r是X的单质,s是Y的单质,n、p及q是这些元素组成的二元化合物;t由其中的三种元素组成,其水溶液呈碱性;p是淡黄色固体,q是一种耐高温材料,它们的关系如图所示.下列说法正确的是( ) 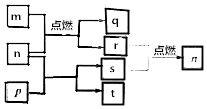
A.Y,Z,W的简单离子的电子层结构相同
B.原子半径:r(X)<r(Y)<r(Z)<r(W)
C.简单氢化物的稳定性:X>Y
D.Y与Z两种元素形成的化合物一定只含离子键
【答案】A
【解析】解:短周期主族元素X、Y、Z、W原子序数依次增大,m是W的单质,r是X的单质,s是Y的单质,n、p及q是这些元素组成的二元化合物;t由其中的三种元素组成,其水溶液呈碱性;p是淡黄色固体,q是一种耐高温材料,结合图转化可知,p为Na2O2 , n为CO2 , t为Na2CO3 , s为O2 , m为Mg,q为MgO,r为C,则元素X为C、Y为O、Z为Na,W为Mg,
A.Y、Z、W的简单离子的电子层结构相同,均为10电子结构,故A正确;
B.电子层越多,原子半径越大,同周期原子序数大的原子半径小,则原子半径:r(Y)<r(X)<r(W)<r(Z),故B错误;
C.非金属性Y>X,则简单氢化物的稳定性:X<Y,故C错误;
D.Y与Z两种元素形成的化合物为Na2O,含离子键,若为Na2O2时含离子键和共价键,故D错误;
故选A.


科目:高中化学 来源: 题型:
【题目】除去下列物质中的杂质(括号中为杂质),采用的试剂和除杂方法错误的是( )
选项 | 含杂质的物质 | 试剂 | 除杂方法 |
A | C2H4(SO2) | NaOH溶液 | 洗气 |
B | C6H6(Br2) | Fe粉 | 蒸馏 |
C | C6H5NO2(HNO3) | NaOH溶液 | 分液 |
D | C2H2(H2S) | CuSO4溶液 | 洗气 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关氨或铵盐的说法不正确的是( )
A.NH3属于弱电解质
B.可用湿润的红色石蕊试纸检验氨气
C.用盐酸滴定氨水,当溶液呈中性时,c(NH4+)=c(Cl﹣)
D.常温时,0.1mol?L﹣1NH4Cl溶液加水稀释, ![]() 的值不变
的值不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在不同温度下,水达到电离平衡时c(H+)与c(OH-)的关系如图所示,下列说法中正确的是
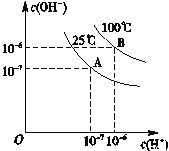
A. 25℃时,0.2mol/LBa(OH)2溶液和0.2mol/LHCl溶液等体积混合,所得溶液的pH等于7
B. 25℃时,pH=12的氨水和pH=2的H2SO4溶液等体积混合,所得溶液的pH大于7
C. 100℃时,pH=12的NaOH溶液和pH=2的H2SO4溶液等体积混合时恰好中和,所得溶液的pH等于7
D. 100℃时,0.2mol/LNaOH溶液与0.1mol/LH2SO4等体积混合后恰好中和,所得溶液pH等于7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.甲烷和苯都能发生取代反应
B.乙醇和乙酸都能与氢氧化钠发生中和反应
C.乙烯和聚乙烯都能与溴的四氯化碳溶液发生加成反应
D.淀粉、油脂、蛋白质都属于天然高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨工艺的一个重要工序是铜洗,其目的是用铜液[醋酸二氨合铜(I)、氨水]吸收在生产过程中产生的CO和CO2等气体。铜液吸收CO的反应是放热反应,其反应方程式为:Cu(NH3)2Ac+CO+NH3![]() [Cu(NH3)3CO]Ac
[Cu(NH3)3CO]Ac
完成下列填空:
(1)如果要提高上述反应的反应速率,可以采取的措施是_________。(选填编号)
a.减压b.增加NH3的浓度 c.升温 d.及时移走产物
(2)铜液中的氨可吸收二氧化碳,写出该反应的化学方程式。_____________________
(3)简述铜液吸收CO及铜液再生的操作步骤(注明吸收和再生的条件)__________________。
(4)铜液的组成元素中,短周期元素原子半径从大到小的排列顺序为___________。其中氮元素原子最外层电子排布的轨道表达式是_____________。通过比较_____________可判断氮、磷两种非金属元素的非金属性强弱。
(5)已知CS2与CO2分子结构相似,CS2的电子式是_______。醋酸二氨合铜中铜的配位数为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列有关曲线与对应的叙述正确的是

A. 图甲表示不同温度下,水溶液中H+和OH-的浓度变化,温度a>b
B. 图乙表示30%H2O2在60℃时分解率与pH关系,说明pH越大H2O2分解率越大
C. 图丙表示体积均为V0、pH均为3的盐酸和醋酸稀释时的pH变化,a表示盐酸
D. 图丁是等浓度NaCl和NaI溶液分别用AgNO3溶液滴定,则Ksp(AgI)>Ksp(AgCl)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ca(H2PO2)2(次磷酸钙,一元中强酸H3PO2的钙盐)是一种白色结晶粉末,溶于水(常温时,溶解度16.7g/100g水),其水溶液呈现弱酸性.可用作医药、抗氧化剂以及制备次磷酸钠等.由白磷(P4)与石灰乳制备Ca(H2PO2)2的实验步骤如下:
步骤1.在三口烧瓶中加入白磷和石灰乳,先通入N2 , 然后在约98°C下充分搅拌1h,同时收集产生的PH3 .
步骤2.将反应液静置、过滤.
步骤3.向滤液中通入适量CO2 , 再过滤.
步骤4.用次磷酸溶液调节步骤3滤液的pH,浓缩、冷却结晶、干燥得次磷酸钙.
a.步骤1先通入N2的目的是 .
b.步骤1石灰乳与 P4(白磷)发生反应的化学方程式为;步骤2过滤所得滤渣成分为 .
c.步骤3的目的是 .
d.请补充完整由产品进一步制备NaH2PO2H2O的实验方案:取产品次磷酸钙加入烧杯中,加适量的水溶解, , 干燥得到NaH2PO2H2O.
(已知:在常压下,加热蒸发次磷酸钠溶液会发生爆炸,100℃时NaH2PO2H2O的溶解度为667g/100g水)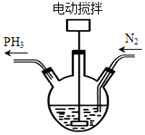
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅蓄电池的工作原理为Pb+PbO2+2H2SO4===2PbSO4+2H2O。下列判断不正确的是
A. 充电时正极的电极反应式:PbSO4+2H2O-2e-===PbO2+4H++SO![]()
B. 当电路中转移0.2 mol电子时,电池中消耗的H2SO4为0.2 mol
C. 铅蓄电池充电时SO![]() 向Pb电极迁移
向Pb电极迁移
D. 铅蓄电池充电时,铅电极应接外加电源的负极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com