
| A. | 0.1molC2H6O分子中含有C-H键数为0.5NA | |
| B. | 0.1molCl2和0.1molHI充分反应后气体分子数为0.2NA | |
| C. | CO2通过Na2O2使其增重2.8g,反应中转移电子数为0.2NA | |
| D. | 3.Og甲醛(HCHO)和乙酸的混合物中含有的原子总数为0.4NA |
分析 A.C2H6O可能为乙醇或者甲醚;
B.氯气与碘化氢反应方程式:Cl2+2HI=I2+2HCl,碘化氢常温下为固体;
C.依据方程式:2Na2O2+2CO2=2Na2CO3+O2,△m~2e-
56g 2mol
据此计算;
D.甲醛和乙酸的最简式为CH2O,3.0g混合物中含有0.1mol最简式.
解答 解:A.0.1molC2H6O,如果为乙醇(CH3CH2OH),则含有C-H键数为0.5NA,如果为甲醚(CH3OCH3),则C-H键数为0.6NA,故A 错误;
B.氯气与碘化氢反应方程式:Cl2+2HI=I2+2HCl,0.1molCl2和0.1molHI反应,氯气过量,HI完全反应,反应完成后体系中含有0.1molHCl,0.05molCl2,0.05molI2,气体分子数为0.15NA,故B错误;
C.依据方程式:2Na2O2+2CO2=2Na2CO3+O2,△m~2e-
56g 2mol
2.8g 0.1mol
所以CO2通过Na2O2使其增重2.8g,反应中转移电子数为0.1NA,故C错误;
D.3.0g含甲醛和乙酸混合物中含有0.1mol最简式CH2O,含有0.4mol原子,含有的原子总数为0.4NA,故D正确;
故选:D.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和常见有机物结构是解题关键,难度不大.


科目:高中化学 来源: 题型:解答题
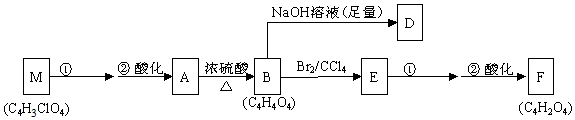
 +(2n-1)H2O .
+(2n-1)H2O .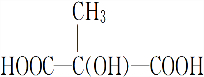 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
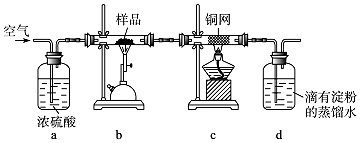

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | lmolNacl 固体中含有NA个Na+ | |
| B. | 18gD2O和18gH2 O中含有的质子数均为10NA | |
| C. | 标准状况下2.24LH2O 含有的共价键数为0.2NA | |
| D. | 密闭容答中2molNO 与lmolO2充分反应,产物的分子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
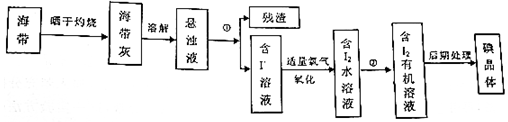
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 非金属性强弱为:X>Y>Z | |
| B. | 气态氢化物的稳定性由强到弱为X、Y、Z | |
| C. | 原子半径大小是:X<Y<Z | |
| D. | 对应阴离子的还原性按X、Y、Z顺序减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ②③④ | C. | ②③⑤ | D. | ②⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com