
【题目】下列化合物中只有非极性共价键的是( )
A.NaClB.NaOHC.H2SD.H2
科目:高中化学 来源: 题型:
【题目】POCl3是有机合成的催化剂,研究小组利用Cl2、PCl3和H2O在105~109℃下制备POCl3。

已知:①PCl3易被氧化易水解,沸点为76℃;②POCl3易水解,沸点为105.8℃。
(1)A装置制取氯气,仪器“2”的名称是______________,离子方程式为________。
(2)PCl3的电子式为____________,仪器“I”的作用是____________。
(3)仪器“3”装入的物质是________,当温度为105--109℃时,逐滴滴入。制备POCl3的化学反应方程式是________。
(4)制备POCl3的关键是必需保证m(Cl2)/m(H2O)≥3.94,当比值小于3.94时得不到POCl3,原因是_________________。
(5)装置连接顺序是A--_____,C中盛装的物质是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在含CH3COOH和CH3COO-的溶液中, CH3COOH、CH3COO-二者中各自所占的物质的量分数(a)随溶液pH变化的关系如图所示。
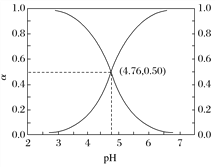
下列说法不正确的是
A. 在pH<4.76的溶液中,c(CH3COO-)<c(CH3COOH)
B. 在pH=7的溶液中,a(CH3COOH)=0,a(CH3COO-)=1.0
C. 在pH>4.76的溶液中,c(CH3COO-)与c(OH-)之和可大于c(H+)
D. 在pH=4.76的溶液中加盐酸,a(CH3COOH)与a(CH3COO-)之和保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某容积一定的密闭容器中,可逆反应:A(g)+B(g)![]() xC(g),符合下列图象(Ⅰ)所示关系。由此推断对图(Ⅱ)的正确说法是( )
xC(g),符合下列图象(Ⅰ)所示关系。由此推断对图(Ⅱ)的正确说法是( )
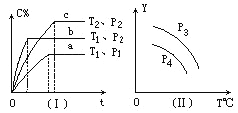
A. P3>P4,Y轴表示A的质量
B. P3<P4,Y轴表示B的百分含量
C. P3>P4,Y轴表示混合气体密度
D. P3>P4,Y轴表示混合气体平均摩尔质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是
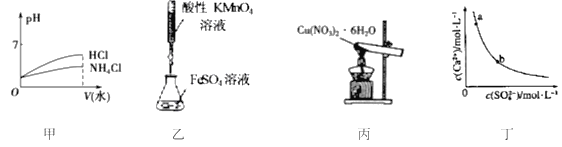
A. 图中表示将pH相同的NH4Cl溶液和HCl溶液稀释相同的倍数
B. 实验室用图乙装置滴定FeSO4溶液
C. 实验室用图丙装置脱结晶水得无水硝酸铜固体
D. 图丁表示常温下CaSO4在水中的沉淀溶解平衡曲线,图中a点溶液可通过蒸发变到b点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中能用来区别SO2和CO2气体的是( ) ①澄清的石灰水
②氯水
③酸性高锰酸钾溶液
④氯化钡溶液
⑤品红溶液.
A.①④⑤
B.②③⑤
C.①②③
D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于燃料电池的说法正确的是
A.燃料电池是通过燃烧方式将化学能转换为电能
B.氢氧燃料电池中,通入氢气的一极为正极
C.氢氧燃料电池是一种环境友好电池
D.燃料电池的能量转化率可达100%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜元素位于元素周期表中第ⅠB族,在化合物中其化合价可以呈现+1、+2 价。铜的单质及其化合物在很多领域有重要的应用。
Ⅰ.CuSO4和Cu(NO3)2是常见的+2价铜的化合物,有较为广泛的应用。
(1)向CuSO4溶液中滴加氨水,最后可以得到深蓝色的[Cu(NH3)4]SO4溶液。
①N、O、S三种元素的第一电离能由大到小的顺序为______________________________。
②比较NH3 和[Cu(NH3)4]2+中H-N-H键角的大小:NH3___________[Cu(NH3)4]2+(填“>”或“<”),并说明理由________________________。
(2)制备Cu(NO3)2的一种方法是在N2O4的乙酸乙酯溶液中加入铜,反应一段时间后,加热即可得到Cu(NO3)2。
①NO3- 的立体构型的名称为_______________,N原子的杂化方式为________________。NO3- 的一种等电子体为________________________。
②N2O4会发生类似于水的自偶电离N2O4![]() NO++NO3- ,制备无水Cu(NO3)2的化学方程式为__________________________________________。
NO++NO3- ,制备无水Cu(NO3)2的化学方程式为__________________________________________。
Ⅱ.CuCl是较为常见的+1价铜的化合物。
(3)基态Cu+ 的价层电子排布式为________________________。
(4)CuCl的晶胞结构如图所示,C1原子位于立方体的顶点和面心,Cu原子位于Cl原子构成的四面体体心。
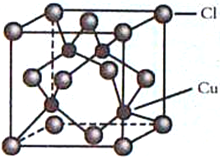
①每个Cl原子周围距Cl原子最近且等距离的Cu原子数目为________________。
②设NA为阿伏加德罗常数的值,晶体的密度为ρg/cm3,CuCl的摩尔质量为M g/mol,计算晶胞中距离最近的两个Cu原子间的距离为___________pm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取50.0mL Na2CO3和Na2SO4的混合溶液,加入过量BaCl2溶液后,得到沉淀14.51g,将沉淀用过量稀HNO3处理后,沉淀质量减少到4.66g,并有气体放出,试计算:
(1)原溶液中Na2SO4的物质的量为______________;
(2)生成气体的体积(标准状况)为_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com