
(1)���ǵ�ѭ���е���Ҫ���ʣ����ĺϳ���Ŀǰ�ձ�ʹ�õ��˹��̵�������
(1)��֪��H��H����Ϊ436 KJ��mol��1��N��N����Ϊ945KJ��mol��1��N��H����Ϊ391 KJ��mol��1��д���ϳɰ���Ӧ���Ȼ�ѧ����ʽ��________
(2)���淴ӦN2��3H2![]() 2NH3�ں����ܱ������н��У��ﵽƽ��״̬�ı�־��________��
2NH3�ں����ܱ������н��У��ﵽƽ��״̬�ı�־��________��
�ٵ�λʱ��������n mo1��N2��ͬʱ����3n mol��H2
�ڵ�λʱ����1��N��N�����ѵ�ͬʱ����6��N��H������
��������N2��H2��NH3�����ʵ���Ϊ1��3��2
�ܳ����£����������ܶȲ��ٸı��״̬
�ݳ����£���������ƽ����Է����������ٸı��״̬
(3)�����£���һ��2 L���ܱ������г���2.6 mol��H2��1 mol��N2����Ӧ�����ж�NH3��Ũ�Ƚ��м�⣬�õ����������±�����
5 min�ڣ�����N2��ƽ����Ӧ����Ϊ________���������¸÷�Ӧ�Ļ�ѧƽ�ⳣ��K��________����Ӧ�ﵽƽ�������ƽ����ϵ�м���H2��N2��NH3��2 mol����ѧƽ�⽫��________(�����Ӧ�����淴Ӧ��)�����ƶ���
(4)���ǵ��ʹ�ҵ����Ҫԭ�ϣ�ij���ʳ�����Ȼʯ���(��Ҫ�ɷ�CaSO4)Ϊԭ�������̬����(NH4)2SO4��(��֪Ksp(CaSO4)��7.10��10��5 Ksp(CaCO3)��4.96��10��9)�乤���������£�
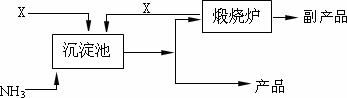
��д���Ʊ�(NH4)2SO4�ķ�Ӧ����ʽ��________���������й����ݼ���������Ӧ�ܷ�����ԭ��________��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ||
| ���� |
| ||
| ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʱ��/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c��NH3��/mol?L-1 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʱ��/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c��NH3��/mol?L-1 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013���㽭ʡ�߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ������
��10�֣�(1) ���ǵ�ѭ���е���Ҫ���ʣ����ĺϳ���Ŀǰ�ձ�ʹ�õ��˹��̵�������
��1����֪��H��H����Ϊ436KJ��mol-1��N��N����Ϊ945 KJ��mol-1��N��H����Ϊ391 KJ��mol-1��д���ϳɰ���Ӧ���Ȼ�ѧ����ʽ��
��2�����淴ӦN2 +3H2 2NH3 �ں����ܱ������н��У��ﵽƽ��״̬�ı�־��
2NH3 �ں����ܱ������н��У��ﵽƽ��״̬�ı�־��
�ٵ�λʱ��������n mo1 N2��ͬʱ����3n mol H2
�ڵ�λʱ����1��N��N�����ѵ�ͬʱ����6��N��H������[��Դ:Z.xx.k.Com]
��������N2��H2��NH3�����ʵ���Ϊ1��3��2
�ܳ����£����������ܶȲ��ٸı��״̬
�ݳ����£���������ƽ����Է����������ٸı��״̬
��3�������£���һ��2L���ܱ������г���2.6 mol H2��1 mol N2����Ӧ�����ж�NH3��Ũ�Ƚ��м�⣬�õ����������±�����
|
ʱ��/min |
5 |
10 |
15 |
20 |
25 |
30 |
|
C(NH3)/mol��L-1 |
0.08 |
0.14 |
0.18 |
0.20 |
0.20 |
0.20 |
5min�ڣ�����N2��ƽ����Ӧ����Ϊ ���������¸÷�Ӧ�Ļ�ѧƽ�ⳣ��K= ����Ӧ�ﵽƽ�������ƽ����ϵ�м���H2��N2��NH3��2mol����ѧƽ�⽫�� �������Ӧ�����淴Ӧ���������ƶ���
��4�����ǵ��ʹ�ҵ����Ҫԭ�ϡ�ij���ʳ�����Ȼʯ�����Ҫ�ɷ�CaSO4��Ϊԭ�������̬����(NH4)2SO4������֪Ksp(CaSO4)=7.10��10-5 Ksp(CaCO3)=4.96��10-9���乤���������£�

��д���Ʊ�(NH4)2SO4�ķ�Ӧ����ʽ�� ��
�������й����ݼ���������Ӧ�ܷ�����ԭ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com