
| A. | 常温常压下,32 g 臭氧中含有2NA个氧原子 | |
| B. | 标准状况下,22.4 L CCl4中含有的分子数为NA | |
| C. | 23 g钠离子中含有的电子数为NA | |
| D. | Zn+2H+=Zn2++H2↑ 2mol H+被氧化时转移2mol 电子 |
分析 A.根据臭氧的分子式计算原子数;
B.标准状况下,CCl4是液体;
C.23 g钠离子的物质的量为1mol,中含有的电子数为10NA;
D.反应Zn+2H+=Zn2++H2↑中 H+是氧化剂,应被还原.
解答 解:A.32g臭氧分子中,含有氧原子物质的量:n=$\frac{32g}{48g/mol}$×3=2mol,含有氧原子的个数为2NA,故A正确;
B.标准状况下,CCl4是液体,而气体摩尔体积适用于气体,故B错误;
C.23 g钠离子的物质的量为1mol,中含有的电子数为10NA,而不是NA,故C错误;
D.反应Zn+2H+=Zn2++H2↑中 H+是氧化剂,应被还原,而不是被氧化,故D错误;
故选A.
点评 本题主要考查了阿伏伽德罗常数的运用,注意气体摩尔体积的应用条件、氧化还原概念的判断、相关公式的换算运用,平时须总结常见易错点.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同质量H2与Cl2,H2的分子数比Cl2多 | |
| B. | 摩尔是用来衡量微观粒子多少的物理量 | |
| C. | 0.1molH2SO4含有氢原子数的精确值为1.204×1023 | |
| D. | 0.5mol氢的质量是0.5g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
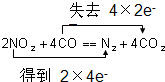
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用氨制碳酸氢铵 | B. | 制普通玻璃 | ||
| C. | 用铁矿石炼铁 | D. | 汽车用乙醇汽油作燃料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氮原子的质量就是氮的相对原子质量 | |
| B. | 氢氧化钠的摩尔质量是40 g | |
| C. | 1mol H2SO4中含有1mol H2 | |
| D. | 氩气的摩尔质量在数值上等于它的相对原子质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100 g质量分数为98%的浓硫酸中所含有的氧原子数为4 NA | |
| B. | 足量的Fe与6.72 L Cl2反应转移的电子数为0.6 NA | |
| C. | 密闭容器中1 molN2与4 molH2反应生成的NH3分子数小于2NA | |
| D. | 常温常压下,92 g的NO2和N2O4混合气体含有的氧原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Na+、Cl-、NO3- | B. | Al3+、Na+、NO3-、Cl- | ||
| C. | K+、Na+、Cl-、AlO2- | D. | K+、NH4+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,含有离子键和非极性共价键的化合物的电子式为
,含有离子键和非极性共价键的化合物的电子式为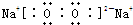 ;含有极性共价键和非极性共价键的化合物的电子式为
;含有极性共价键和非极性共价键的化合物的电子式为 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com