
| A.2mol/L硫酸溶液 | B.2mol/L氢氧化钠溶液 |
| C.2mol/L硫酸镁溶液 | D.硅酸溶液 |
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:阅读理解
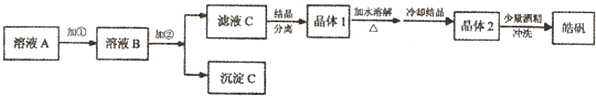
| 温度(℃) | 60 | 240 | 930 | 1000 |
| 残留固体质量(g) | 19.7 | 16.1 | 8.1 | 8.1 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:2016届四川省成都市六校协作体高一上学期期中考试化学试卷(解析版) 题型:填空题
Ⅰ.某化学兴趣小组对下列三组物质进行研究:
A.HCl H2SO4 H2CO3 HNO3
B.溶液 水 悬浊液 胶体
C.Na2CO3 NaNO3 AgNO3 Ba(NO3)2
请你帮他们完善下列空白:
|
|
A |
B |
C |
|
分类标准 |
含氧酸 |
分散系 |
|
|
不属于该类别的物质 |
|
|
Na2CO3 |
Ⅱ.现有下列物质:①铝 ②氢氧化铁胶体 ③氯化氢 ④SO2 ⑤NaHSO4 固体 ⑥Ba(OH)2固体 ⑦稀硫酸 ⑧醋酸 ⑨烧碱 ⑩熔融NaNO3
(1)按物质的分类方法填写表格的空白处:(填编号)
|
分类标准 |
能导电的物质[ |
电解质 |
强电解质 |
|
属于该类的物质 |
|
|
|
(2)①与⑨的溶液反应的离子方程式为
(3)用Fe(OH)3胶体进行下列实验:
(a)将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附的颜色逐渐变 (填“深”或“浅”),这表明 。
(b)向其中逐滴加入过量稀硫酸溶液,现象是_______ _______;
(4)向Ba(OH)2溶液逐滴加入NaHSO4溶液至恰好不再生成沉淀为止,写出此步的离子方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com