
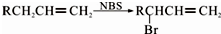 .
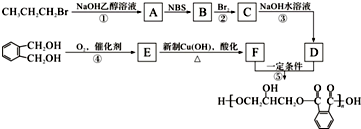
.
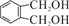 的同分异构体中同时符合下列条件的芳香族化合物共有
的同分异构体中同时符合下列条件的芳香族化合物共有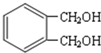 →E→F→
→E→F→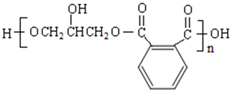 ,结合反应条件可知,E为
,结合反应条件可知,E为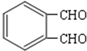 ,F为
,F为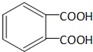 ,据此答题.
,据此答题. →E→F→
→E→F→ ,结合反应条件可知,E为
,结合反应条件可知,E为 ,F为
,F为 ,
, ,C为BrCH2CHBrCH2Br,C的名称是1,2,3-三溴丙烷,
,C为BrCH2CHBrCH2Br,C的名称是1,2,3-三溴丙烷, ;1,2,3-三溴丙烷;
;1,2,3-三溴丙烷; ,有两个醛基,所以1mol E与足量的银氨溶液反应能生成4molAg,故错误;
,有两个醛基,所以1mol E与足量的银氨溶液反应能生成4molAg,故错误; ,有两个羧基,能与NaHCO3反应产生CO2,故正确;
,有两个羧基,能与NaHCO3反应产生CO2,故正确;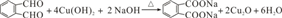 ,
,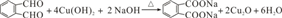 ;
;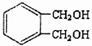 的同分异构体中同时符合下列条件:a.能发生消去反应,b.能与过量浓溴水反应生成白色沉淀的芳香族化合物为
的同分异构体中同时符合下列条件:a.能发生消去反应,b.能与过量浓溴水反应生成白色沉淀的芳香族化合物为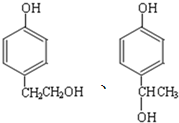 ,以及这两种物质的基团在邻位和间位的化合物,共有6 种,
,以及这两种物质的基团在邻位和间位的化合物,共有6 种, ,
, .
.


科目:高中化学 来源: 题型:
| A、Na2CO3比NaHCO3的溶度大 |
| B、受热时NaHCO3比Na2CO3稳定 |
| C、澄清的石灰水能与Na2CO3反应而不与NaHCO3反应 |
| D、向相同浓度的NaHCO3与Na2CO3溶液中分别滴入2滴酚酞溶液,前者红色更深 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同主族元素含氧酸的酸性随核电荷数的增加而减弱 |
| B、核外电子排布相同的微粒化学性质相同 |
| C、Cl-、S2-、Ca2+、K+半径逐渐减小 |
| D、还原性强弱:F-<Cl-<I- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.5g |
| B、5.0 g |
| C、10.0g |
| D、12.5g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol过氧化钠固体与足量的水反应,转移的电子数目为2NA |
| B、Fe在1molCl2中充分燃烧,转移的电子数目为3NA |
| C、将含有0.1molFeCl3的FeCl3饱和溶液,滴入沸水中加热形成Fe(OH)3胶体,所含的胶体粒子数目少于0.1NA |
| D、足量的MnO2粉末与含有4molHCl的浓盐酸充分反应,转移的电子数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
 Ⅰ.常温下ClO2是黄绿色,有刺激性气味的气体,液态呈红棕色,熔点为-59℃,沸点为11.0℃;
Ⅰ.常温下ClO2是黄绿色,有刺激性气味的气体,液态呈红棕色,熔点为-59℃,沸点为11.0℃;查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某溶液中加入AgNO3溶液,生成白色沉淀,说明原溶液中有Cl- |
| B、某溶液中加入BaCl2溶液,生成白色沉淀,说明原溶液中有SO42- |
| C、某溶液中加入稀硫酸,生成无色气体,说明原溶液中有CO32- |
| D、某溶液中加入NaOH溶液,生成能使湿红色石蕊试纸变蓝的气体,说明原溶液中有NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

| A、1 mol S(g)与O2(g)完全反应生成SO2(g),反应放出的热量小于297.0 kJ | ||
B、一定条件下1 mol SO2(g)和
| ||
| C、在相同条件下,SO2 (g)比SO3 (g)稳定 | ||
D、S(s)与O2(g)反应生成SO3(g)的热化学方程式S(s)+
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com