
 某同学称取了4.0g NaOH固体,欲配制100mL溶液.
某同学称取了4.0g NaOH固体,欲配制100mL溶液.分析 (1)根据实验操作的步骤以及每步操作需要仪器确定反应所需仪器,然后确定用到的能确定体积的两种玻璃仪器;
(2)根据固体溶解需用玻璃棒搅拌加快溶解,在转移溶液时用玻璃棒引流;
(3)根据C=$\frac{n}{V}$判断,如果n偏小或V偏大,则配制溶液的浓度偏低,如果n偏大或V偏小,则配制溶液浓度偏大;
(4)标签上应注明药品名称的化学式和浓度.
解答 解:(1)操作步骤有计算、称量、稀释、移液、洗涤移液、定容、摇匀等操作,用托盘天平、药匙称取氢氧化钠,在烧杯中稀释(可用量筒加水),用玻璃棒搅拌,冷却至室温后转移到100mL容量瓶中,并用玻璃棒引流,洗涤2-3次,将洗涤液转移到容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加至溶液凹液面与刻度线水平相切,盖好瓶塞颠倒摇匀,所以需要的仪器为:托盘天平、药匙、量筒、烧杯、玻璃棒、100mL容量瓶、胶头滴管,用到的能确定体积的两种玻璃仪器是量筒、100mL容量瓶;
故答案为:量筒、100mL容量瓶;
(2)NaOH固体溶解需用玻璃棒搅拌加快溶解,在转移溶液时用玻璃棒引流,所以玻璃在实验中的作用有搅拌、引流;
故答案为:搅拌、引流;
(3)①少量液体溅出烧杯外,溶质的物质的量减小,溶液浓度偏小,故答案为:偏小;
②定容时仰视仪器上的刻度线,溶液的体积偏大,所配制溶液浓度偏小,故答案为:偏小;
③定容后,将容量瓶振荡摇匀后,静置发现液面低于刻度线,于是又加入少量水至刻度线,液体下落下来,溶液的体积偏大,所配制溶液浓度偏小,故答案为:偏小;
(4)标签上应注明药品名称的化学式和浓度: ,故答案为:
,故答案为: .
.
点评 本题考查一定物质的量浓度溶液的配制,难度不大,注意实验步骤、仪器的作用、误差分析为易错点.


科目:高中化学 来源: 题型:选择题
| A. | Cu(OH)2+HCl;Cu(OH)2+CH3COOH | B. | NaHCO3+H2SO4;KHCO3+HCl | ||
| C. | NaHCO3+NaOH;Ca(HCO3)2+NaOH | D. | BaCl2+H2SO4;Ba(OH)2+H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 表示的分子式C6H14;名称是2-甲基戊烷.
表示的分子式C6H14;名称是2-甲基戊烷. 中含有的官能团的名称为羟基、酯基.
中含有的官能团的名称为羟基、酯基.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 福尔马林可作食品的保鲜剂 | |
| B. | 用激光笔分别照射盛有牛奶、食盐水的玻璃杯,都有光亮的通路 | |
| C. | “地沟油”禁止食用,但经过加工处理后,可以用来制肥皂和生物柴油 | |
| D. | 半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
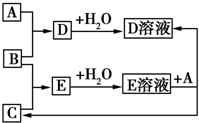 已知A、B、C为中学化学中常见的单质.室温下,A为固体,B和C均为气体.在适宜的条件下,它们可以按如图进行反应.下列说法中不正确的是( )
已知A、B、C为中学化学中常见的单质.室温下,A为固体,B和C均为气体.在适宜的条件下,它们可以按如图进行反应.下列说法中不正确的是( )| A. | A、B、C中三种元素的任意两种元素形成的化合物所属物质类别可能是氧化物 | |
| B. | A、B、C中三种元素形成的化合物所属物质类别一定不是碱 | |
| C. | 如果E溶液是一种强酸,则E溶液为盐酸 | |
| D. | A、B、C中有一种金属且为A |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用带玻璃塞的试剂瓶盛放稀H2SO4溶液 | |
| B. | 用广泛pH试纸测得稀盐酸的pH为2.2 | |
| C. | 向饱和FeCl3溶液中滴加过量氨水,可制得Fe( OH)3胶体 | |
| D. | 焰色反应时,用稀硫酸洗净铂丝,并在火焰上灼烧至无色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com