
【题目】(10分)离子推断题:
有一未知的无色溶液,可能含有以下离子中的若干种(忽略由水电离产生的H+、OH-):H+、NH4+、K+、Mg2+、Fe3+、Al3+,NO3-、CO32-、SO42-,现取两份100mL溶液进行如下实验:
①第一份加入足量的BaCl2溶液后,有白色沉淀产生,经洗涤、干燥后,称量沉淀质量为6.99g;
②第二份逐滴滴加NaOH溶液,测得沉淀的物质的量与NaOH溶液的体积关系如下图所示。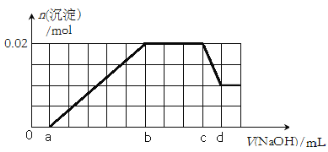
根据上述实验事实,回答以下问题:
(1)该溶液中一定不存在的阳离子有 ;
(2)在实验②中,NaOH溶液滴至b~c段过程中发生的离子反应方程式为 ;NaOH溶液的浓度为 (用含字母c、d的代数式表示);
(3)确定原溶液一定含有Mg2+、Al3+、H+,其物质的量之比n(Mg2+):n(Al3+):n(H+)为 (填数字,下同);
(4)原溶液中NO3-的浓度为c(NO3-),则c(NO3-)的取值范围为 。
【答案】22.(10分)
(1)Fe3+ (2分) (2)NH4+ + OH-= NH3·H2O(2分) 10/(d-c) mol·L-1(2分)
(3)1:1:1 (2分) (4)c(NO3-)≥0.3 mol·L-1(2分)
【解析】
试题分析:由于原溶液是无色的,所以一定不含黄色Fe3+离子。根据实验①证明可能含有CO32-、SO42-中的一种或两种离子;根据实验②证明0-a发生H++OH-=H2O,a-b发生Al3++3OH-=Al(OH)3↓、Mg2++2OH-=Mg(OH)2↓,NH4+ +OH-=NH3H2O,Al(OH)3+OH-=AlO2-+2H2O,据此回答。
(1)根据上述分析,该溶液中一定不存在的阳离子有Fe3+。
(2)在实验②中,NaOH溶液滴至b~c段过程中没有沉淀生成,也没有沉淀溶解,只能是NH4+ 与碱的反应,所以发生的离子反应方程式为NH4+ + OH-= NH3·H2O;当NaOH过量时,发生反应Al(OH)3+ OH-= AlO2-+ 2H2O,根据图像可知,反应的氢氧化铝为0.01mol,则NaOH的物质的量也为0.01mol, NaOH溶液的浓度为0.01mol÷(d-c)×10-3L=10/(d-c) mol·L-1;
(3)根据上述分析可知,氢氧化铝的物质的量为0.01mol,即溶液中的Al3+为0.01mol,氢氧化镁为0.01mol,溶液中的Mg2+为0.01mol,根据化学反应Al3++3OH-=Al(OH)3↓、Mg2++2OH-=Mg(OH)2↓,溶液中的Mg2+和Al3+一共消耗0.05molOH-,所以图像中一个单位为0.01mol,则原溶液中含有的Mg2+、Al3+、H+的物质的量之比1:1:1。
(4)根据上述分析,溶液中含有Mg2+,因为MgCO3 是沉淀,则原溶液中没有CO32-,只有SO42-,BaSO4沉淀的物质的量为6.99g÷233g/mol=0.03mol,H+的物质的量为0.01mol,Mg2+的物质的量为0.01mol,Al3+的物质的量为0.01mol,NH4+ 的物质的量为0.03mol,因为溶液呈电中性,若没有其他阳离子,原溶液中的NO3-的物质的量为0.01+0.01×2+0.01×3+0.03-0.03×2=0.03mol,浓度为c(NO3-)=0.03mol÷0.1L=0.3 mol·L-1,若溶液中还有其它阳离子,则c(NO3-)的取值范围为c(NO3-)≥0.3 mol·L-1。


科目:高中化学 来源: 题型:
【题目】n L三种气态烃混合物与足量氧气混合点燃后,恢复到原来状态(常温常压),体积共缩小2n L,这三种烃不可能的组合是 ( )
A.CH4、C2H4、C3H4以任意比混合
B.C2H6、C4H6、C2H2以2:1:2的物质的量之比混合
C.C3H8、C4H8、C2H2以11:14:26的质量之比混合
D.CH4、C3H6、C2H2以a:b:b体积比混合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NO 为阿伏加德罗常数,下列说法正确的是
A、250C时,15g乙烷气体中含3.5NO 个共价键
B、标准状况下,22.4L苯在Fe 催化条件下可与NO 个Br2 发生取代反应
C、18g2H2O中含有电子数为10NO
D、1mol N2和3mol H2发生反应N2(g)+3H2(g)![]() 2NH3(g),共有6NO 个电子转移
2NH3(g),共有6NO 个电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+B(g)→C(g) △H,分两步进行:①A(g)+B(g)→X(g)△H1,②X(g) →C(g)△H2, 反应过程中能量变化如图所示,E1表示A+B→X的活化能,下列说法正确的是( )
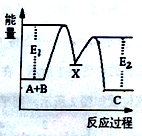
A.△H1=△H一△H2>0 B.X是反应A(g)+B(g)→C(g)的催化剂
C.E2是反应②的活化能 D.△H1=E1-E2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某强酸性溶液X可能含有A13+、NH4+、Fe2+、Fe3+、CO32-、SO32-、SO42-、C1-中的一种或几种,取该溶液进行连续实验,实验过程如下:
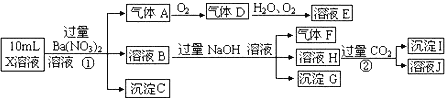
根据以上信息,回答下列问题:
上述离子中,溶液X中除H+外还肯定含有的离子是__________
请设计简单的实验检验不能确定是否含有的离子(若不止一种,可任选一种)的存在:
写出反应①的离子方程式 ;
④假设测定A、F、I均为0.1mol,100mL X溶液中n(H+)=0.4mol,当沉淀C物质的量大于0.7mol时,溶液X中还一定含有 .
(2)实验室常见的几种气体发生装置如图A、B、C所示:
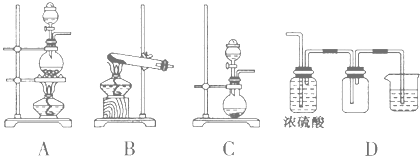
①实验室可以用B或C装置制取氨气,如果用B装置制取氨气其化学反应方程式为 。
②气体的性质是选择气体收集方法的主要依据.下列气体的性质与收集方法无关的是 (填序号,下同).
A.密度 B.颜色 C.溶解性 D.热稳定性 e.与氧气反应
③若用A装置与D装置相连制取并收集X气体,则X可能是下列气体中的 (填序号).
A.CO2 B.NO C.Cl2 D.H2 e.HCl
其中在D装置中连接烧杯的目的是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2016年高考上海卷】一定条件下,一种反应物过量,另一种反应物仍不能完全反应的是 ( )
A.过量的氢气与氮气 B.过量的浓盐酸与二氧化锰
C.过量的铜与浓硫酸 D.过量的锌与18 mol/L硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【百强校·2016届大庆一中上学期第四次月考】下列各组离子能在溶液中大量共存的是( )
A. K+、Na+、Cl-、NO3- B.Fe3+、K+、Br-、SCN-
C.NH4+、Na+、CO32-、OH- D.Al3+、Mg2+、SO42-、HCO3-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com