
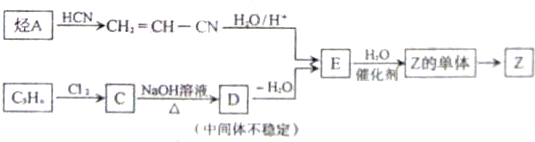

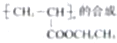 实验,此实验过程涉及的反应类型有
实验,此实验过程涉及的反应类型有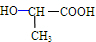 ,
,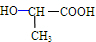 发生缩聚反应生成高聚物Z为
发生缩聚反应生成高聚物Z为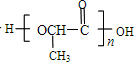 .由转化关系可知,C为卤代烃,发生水解反应得到D,D脱去水得到E,则B为CH2=CH-CH3,与氯气发生取代反应生成C为CH2=CH-CCl3,D为CH2=CH-C(OH)3,据此解答.
.由转化关系可知,C为卤代烃,发生水解反应得到D,D脱去水得到E,则B为CH2=CH-CH3,与氯气发生取代反应生成C为CH2=CH-CCl3,D为CH2=CH-C(OH)3,据此解答.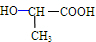 ,
,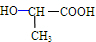 发生缩聚反应生成高聚物Z为
发生缩聚反应生成高聚物Z为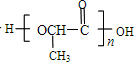 .由转化关系可知,C为卤代烃,发生水解反应得到D,D脱去水得到E,B为CH2=CH-CH3,与氯气发生取代反应生成C为CH2=CH-CCl3,D为CH2=CH-C(OH)3,
.由转化关系可知,C为卤代烃,发生水解反应得到D,D脱去水得到E,B为CH2=CH-CH3,与氯气发生取代反应生成C为CH2=CH-CCl3,D为CH2=CH-C(OH)3,| 光照 |
| 光照 |
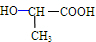 ,可发生缩聚反应,方程式为
,可发生缩聚反应,方程式为 ,
, ;
;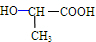 制取高聚物聚丙烯酸乙酯,先与乙醇发生酯化反应生成CH3CH(OH)COOCH2CH3,再发生消去反应生成CH2=CHCOOCH2CH3,最后发生加聚反应得到聚丙烯酸乙酯,故答案为:酯化反应、消去反应、加聚反应;
制取高聚物聚丙烯酸乙酯,先与乙醇发生酯化反应生成CH3CH(OH)COOCH2CH3,再发生消去反应生成CH2=CHCOOCH2CH3,最后发生加聚反应得到聚丙烯酸乙酯,故答案为:酯化反应、消去反应、加聚反应;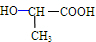 )的某种同分异构体具有下列性质:能发生银镜反应,1mol该物质与足量金属钠反应可生成1gH2,则含有一个-OH、1个-CHO,该物质分子中且个手性碳原子,存在连接4故本题乙酯或原子团的碳原子,则该同分异构体为
)的某种同分异构体具有下列性质:能发生银镜反应,1mol该物质与足量金属钠反应可生成1gH2,则含有一个-OH、1个-CHO,该物质分子中且个手性碳原子,存在连接4故本题乙酯或原子团的碳原子,则该同分异构体为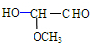 ,含有醛基、羟基、醚键三种官能团,故答案为:3;
,含有醛基、羟基、醚键三种官能团,故答案为:3;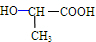 )的分子式相同,且满足下列条件的所有同分异构体:①能发生银镜反应 ②能发生水解反应,应含有甲酸形成的酯基,③能发生酯化反应,还含有羟基,符合条件的同分异构体有:
)的分子式相同,且满足下列条件的所有同分异构体:①能发生银镜反应 ②能发生水解反应,应含有甲酸形成的酯基,③能发生酯化反应,还含有羟基,符合条件的同分异构体有: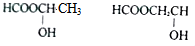 ,故答案为:
,故答案为: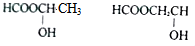 .
.


科目:高中化学 来源: 题型:
| A、0.044mol/L |
| B、0.44mol/L |
| C、4.4mol/L |
| D、44mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、OH-+CO32-+2H+═HCO3-+H2O |
| B、2OH-+CO32-+3H+═HCO3-+2H2O |
| C、2OH-+CO32-+4H+═CO2+3H2O |
| D、OH-+CO32-+3H+═CO2+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
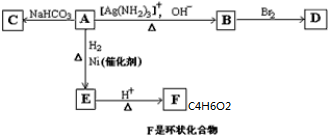
查看答案和解析>>
科目:高中化学 来源: 题型:
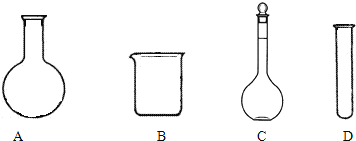
| 实验 | 酸或碱 | 现象 |
| A | 1滴0.2mol/LNaOH溶液 | 不变色 |
| B | 1滴水 | 缓慢变浅棕褐色 |
| C | 1滴0.1mol/L硫酸溶液 | 迅速变棕褐色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铝粉投入到NaOH溶液中:2Al+2OH-=2AlO2-+H2↑ |
| B、NaAlO2溶液中加入过量盐酸:AlO2-+H++H2O=Al(OH)3↓ |
| C、NaAlO2溶液中通入过量的CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
| D、Al2O3粉末溶于NaOH溶液中:Al2O3+2OH-=2AlO2-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、平衡向正反应方向移动 |
| B、a<b |
| C、物质B的质量分数增加 |
| D、物质A的转化率降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
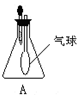 使用装置A进行实验时,将滴管中的液体加入到锥形瓶中,发现气球鼓起来.试推测锥形瓶中的气体和滴管中的物质可能为( )
使用装置A进行实验时,将滴管中的液体加入到锥形瓶中,发现气球鼓起来.试推测锥形瓶中的气体和滴管中的物质可能为( )| A、Cl2和饱和食盐水 |
| B、NO和水 |
| C、O2和水 |
| D、SO2和NaOH溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com