
 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案科目:高中化学 来源:2015-2016学年甘肃省高二上期末化学试卷(解析版) 题型:选择题
一种燃料电池中发生的化学反应为:在酸性溶液中甲醇与氧作用生成水和二氧化碳。该电池负极发生的反应是( )
A.CH3OH(g)+O2(g)-2e- = H2O(l)+CO2(g)+2H+(aq)
B.O2(g)+4H+(aq)+4e-=2H2O(l)
C.CH3OH(g)+H2O(l)-6e- =CO2(g)+6H+(aq)
D.O2(g)+2H2O(l)+4e- =4OH-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高二下期末化学试卷(解析版) 题型:填空题
下表是元素周期表的一部分.表中所列字母分别代表一种元素.

试回答下列问题:
(1)请画出元素D的基态原子的价电子排布图______________;与D同周期的所有元素的基态原子中最外层电子数与D原子相同的元素有______________种;
(2)A的最简单氢化物的中心原子的杂化形式为______________;C在空气中燃烧产物的分子构型为______________,与其互为等电子体的单质的分子式为______________;
(3)B单质晶体中原子的堆积方式如图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
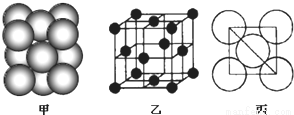
①晶胞中B原子的配位数为______________,其堆积方式______________(填“是或否”)密置堆积。②若B原子的半径为d cm,用NA表示阿伏加德罗常数,M表示B原子的相对原子质量,则该晶体的密度为______________(用字母表示)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高二下期末化学试卷(解析版) 题型:选择题
下列各组物质熔点高低的比较正确的是( )
A.CF4>CCl4>CBr4>CI4
B.Na>Mg>Al
C.SiO2>H2O>CO2
D.晶体硅>SiC>金刚石
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高二下期末化学试卷(解析版) 题型:选择题
可用自由电子与金属离子的碰撞中有能量传递来解释的物理性质是( )
A.金属是热的良导体
B.金属是电的良导体
C.金属有良好的延展性
D.有金属光泽,不透明
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高一下期末化学试卷(解析版) 题型:填空题
工业上采用氨的催化氧化制备硝酸,起反应如下:
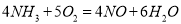
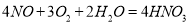
设空气中氧气的体积分数为0.20,氮气的体积分数为0.80
(1)为使NH3恰好完全氧化为NO,氨-空气混合物中氨的体积分数为 (用小数表示,保留2位小数)
(2)1mol NH3完全转化HNO3,若在此过程中不补充水,则所得HNO3溶液的质量分数为 (用小数表示,保留2位小数)
(3)已知NH3完全转化NO的转化率为95%,由NO转化HNO3的转化率为92%.请计算用17吨NH3可制取质量分数为0.63的硝酸溶液为 吨
(4)硝酸工业生产中的尾气可用纯碱溶液吸收,有关的化学反应为:
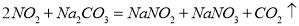 ①
①
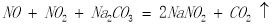 ②
②
若每生产1mol CO2,吸收溶液质量就增加40g。计算吸收液中NaNO2和NaNO3物质的量之比为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高一下期末化学试卷(解析版) 题型:选择题
SF6是一种优良的绝缘气体,分子结构中存在S-F键.已知1molS(s)转化为气态硫原子吸收能量280kJ,断裂1molF-F、S-F键需吸收的能量分别为160kJ、330kJ。则发生反应S(s)+3F2(g)═SF6(g),生成1molSF6时能量变化为( )
A、释放1220KJ B、吸收1780KJ C、 吸收1220KJ D、释放1780KJ
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高一下期末化学试卷(解析版) 题型:选择题
向碘酸钠(NaIO3)的碱性溶液中通入氯气,可以得到钠盐Na2H3IO6.下列有关该反应的说法中错误的是( )
A.在该反应中碘酸钠作还原剂
B.碱性条件下,氯气的氧化性强于高碘酸钠的氧化性
C.反应中氧化产物与还原产物的物质的量之比为2:1
D.反应中生成1 mol Na2H3IO6转移2 mol电子
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省汕头市高一下期末化学试卷(解析版) 题型:填空题
X、Y、Z、W代表短周期的四种元素,有关它们的部分信息如下表所示:
元素 | 部分结构特点 | 部分性质 |
X | X的单质由双原子分子构成,分子中有14个电子 | X有多种氧化物,如XO、XO2等 |
Y | Y原子的次外层电子数等于最外层电子数的一半 | Y元素能形成多种单质 |
Z | Z原子的最外层电子数多于4 | Z元素的最高正化合价与最低负化合价的代数和等于6 |
W | 第三周期元素的简单离子中半径最小 | W的单质化学性质虽较活泼,但只需常温保存 |
请按要求回答下列问题(注意不能用字母X、Y、Z、W作答,请用相应的元素符号或化学式填写):
(1)X的元素名称是 ,X的气态氢化物的电子式是 。
(2)Z元素在周期表中的位置是第 周期,第 族。Z和W形成的化合物属于 化合物(填“离子”或“共价”)。
(3)X、Y、Z、W的原子半径从大到小的顺序是 。
(4)X、Y、Z三种元素的最高价氧化物的水化物的酸性由强到弱的顺序是: 。
(5)铜和X的最高价氧化物的水化物的浓溶液反应的化学方程式: 。
(6)气体分子(YX)2称为拟卤素,性质与卤素类似,请写出(YX)2与NaOH溶液反应的化学方程式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com