
在地壳内,深度每增加1km,压强大约增加25250~30300kPa,在这样的压强下,对固体物质的平衡会发生较大的影响。如:CaAl2Si2O8+Mg2SiO4=CaMg2Al2Si3O12
(钙长石) (镁橄榄石)(钙镁)石榴子石
摩尔质量(g/mol) 278 140.6 413.6
密度(g/cm3) 2.70 3.22 3.50
在地壳区域变质的高压条件下,有利于
A.钙长石生成 B.镁橄榄石生成
C.钙长石和镁橄榄石共存 D.(钙镁)石榴子石生成
科目:高中化学 来源:2014-2015学年河南省英文学校高二10月月考化学试卷(解析版) 题型:填空题
(8分)煤燃烧的反应热可通过以下两种途径来利用:
a.利用煤在充足的空气中直接燃烧产生的反应热;
b.先使煤与水蒸气反应得到氢气和一氧化碳,然后使得到的氢气和一氧化碳在充足的空气中燃烧。这两个过程的热化学方程式为:a.C(s)+O2(g)===CO2(g) ΔH=E1①,b.C(s)+H2O(g)===CO(g)+H2(g) ΔH=E2②,H2(g)+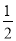 O2(g)===H2O(g) ΔH=E3③,CO(g)+
O2(g)===H2O(g) ΔH=E3③,CO(g)+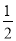 O2(g)===CO2(g) ΔH=E4④
O2(g)===CO2(g) ΔH=E4④
回答:(1)与途径a相比途径b有较多的优_______________________________
(2)上述四个热化学方程式中的哪个反应ΔH>0________。
(3)等质量的煤分别通过以上两条不同的途径产生的可利用的总能量关系正确的是________。
A.a比b多 B.a比b少[来源C.a与b在理论上相同
(4)根据能量守恒定律,E1、E2、E3、E4之间的关系为______________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省南阳市上学期10月月考高二化学试卷(解析版) 题型:填空题
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:

(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式为 .
②Y电极上的电极反应式为 ,
③该反应的总反应方程式是: ﹣
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是 ,电极反应式是 .
②Y电极的材料是 ,电极反应式是 .
(3)若a为CuSO4溶液,则电解时的化学反应方程式为 、 通过一段时间后,向所得溶液中加入0.2molCu(OH)2粉末,恰好恢复电解前的浓度和pH,则电解过程中转移的电子的物质的量为 .
(4)若电解含有0.04molCuSO4和0.04molNaCl的混合溶液400ml,当阳极产生的气体672mL(标准状况下)时,溶液的C(H+)= (假设电解后溶液体积不变).
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省南阳市上学期10月月考高二化学试卷(解析版) 题型:选择题
①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池,①②相连时,外电路电流从②流向①;①③相连时,③为正极;②④相连时,②上有气泡逸出;③④相连时,③的质量减少.据此判断这四种金属活动性由强到弱的顺序是( )
A.①③②④ B. ①③④② C. ③④②① D. ③①②④
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南周口市高二上第一次月考化学(解析版) 题型:选择题
对已达化学平衡的下列反应 2X(g)+ Y(g)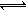 2Z(g),减小压强时,对反应产生的影响是
2Z(g),减小压强时,对反应产生的影响是
A .逆反应速率增大,正反应速率减小,平衡向逆反应方向移动
B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动
C.正、逆反应速率都减小,平衡向逆反应方向移动
D .正、逆反应速率都增大,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南周口市高二上第一次月考化学(解析版) 题型:选择题
一定条件反应N2+3H2 2NH3达平衡,当单独改变下述条件后有关叙述错误
2NH3达平衡,当单独改变下述条件后有关叙述错误
A.加催化剂,v(正)和v (逆)都发生变化,且变化的倍数相等
B.加压, v (正)和v (逆)都增大,且v (正)增加倍数大于v (逆)增加倍数
C.降温, v (正)和v (逆)都减少,且v (正)减少倍数大于v (逆)减少倍数
D.增加N2的浓度, v (正)和v (逆)都增大,且v (正)增加倍数大于v (逆)增加倍数
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南周口市高二上第一次月考化学(解析版) 题型:选择题
下列说法正确的是
A.其他条件不变,增大某一反应物浓度,反应物的转化率一定都增大
B.对于有气体参加的反应,其他条件不变增大压强,体积缩小,体系中各气体的浓度一定增大
C.对于有气体参加的反应,改变压强使平衡向右移动,生成的气体的浓度一定增大
D.增大反应物的浓度,平衡向右移动,生成物的体积分数一定增大
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高一上学期第二次月考化学试卷(解析版) 题型:选择题
下列各组物质,按化合物、单质、混合物顺序排列的是
A、烧碱、液态氧、碘酒
B、生石灰、白磷、纯碱
C、干冰、铁、氯化氢
D、空气、氦气、胆矾
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高二上学期第三次月考化学试卷(解析版) 题型:填空题
(13分)碳、硫的含量影响钢铁性能。碳、硫含量的一种测定方法是将钢样中的碳、硫转化为气体,再用测碳、测硫装置进行测定。
(1)采用装置A,在高温下将x g钢样中的碳、硫转化为CO2、SO2。
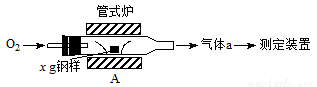
①气体a的成分是______。
②若钢样中硫以FeS形式存在,A中反应:3FeS+5O2 1________+3________。
1________+3________。
(2)将气体a通入测硫装置中(如图),采用滴定法测定硫的含量。
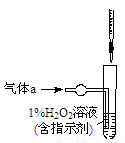
①H2O2氧化SO2的化学方程式:__________________。
②用NaOH溶液滴定生成的H2SO4,消耗z mL NaOH溶液。若消耗1 mL NaOH溶液相当于硫的质量为y g,则该钢样中硫的质量分数:________。
(3)为了减少空气中SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料。已知:2H2(g)+O2(g)=2H2O(g) ΔH1=-d kJ·mol-1;
2C(s)+O2(g)=2CO(g) ΔH2=-e kJ·mol-1;
碳的燃烧热为f kJ·mol-1(d、e、f均大于0);
写出CO与水蒸气反应生成CO2和H2的热化学方程式:_______________________。
②将含SO2的烟气通过洗涤剂Y,再加入稀硫酸,既可以回收SO2,同时又可以得到化肥,上述洗涤剂Y可以是_______(填序号)。
a.Ca(OH)2 b.CaCl2 c.K2CO3 d.NaHSO3 e.NH3·H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com