
【题目】实验室回收废水中的苯酚的过程如图所示。下列说法正确的是
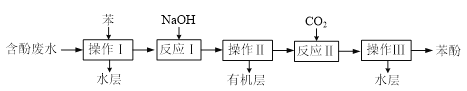
A.操作I为蒸馏B.反应Ⅰ也可加入Na2CO3
C.操作Ⅱ所得有机层可循环利用D.操作Ⅲ所得水层为Na2CO3溶液
 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:
【题目】甲烷是最简单的烷烃,乙烯是最简单的烯烃,下列物质中,不能用来鉴别二者的是( )
A. 溴水B. 水C. 溴的四氯化碳溶液D. 酸性高锰酸钾溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确的是( )

A. 反应CH4+H2O![]() 3H2+CO,每消耗1molCH4转移12mol 电子
3H2+CO,每消耗1molCH4转移12mol 电子
B. 电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O
C. 电池工作时,CO32-向电极B移动
D. 电极B上发生的电极反应为:O2+2CO2+4e-=2CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 酒越陈越香与酯化反应有关
B. 油脂是高分子化合物
C. 乙烯和聚氯乙烯都能使溴的四氯化碳溶液褪色
D. 甲烷与足量氯气在光照下反应可生成难溶于水的油状液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知我们所学的烃和烃的衍生物具有下列转化关系,请回答有关问题

(1)写出以上三个反应的化学方程式(需注明反应所需的条件)
②_______________________________________________________
③_______________________________________________________
④_______________________________________________________
(2)在有机反应类型分类中,反应①属于__________,;
(3)含有4个碳原子,与C2H6互为同系物的物质的分子式为______,写出该组成互为同分异构体的化合物的结构简式________,________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠是重要的防腐剂,某化学兴趣小组以铜和稀硝酸为起始原料,设计如下装置利用NO与Na2O2反应制备NaNO2。(夹持装置已略)

(1)A中反应的化学方程式为_____。
(2)B装置的作用是_____,装置D的作用是_____。
(3)为防止生成其他杂质,B、C装置间还应接入装有_____(填试剂名称)的_____(填仪器名称)。
(4)测定C装置中NaNO2的质量分数的过程如下:准确称取装置C中反应后的固体0.600 g于锥形瓶中,先加水溶解,再向其中滴加0.1000 mol·L-1酸性KMnO4溶液,恰好完全反应时,消耗酸性KMnO4溶液24.00 mL。计算装置C中所得固体中NaNO2的质量分数___________(请写出计算过程)。已知测定过程中发生反应的方程式为MnO4-+NO2-+H+—Mn2++NO3-+H2O(未配平)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校学生为探究苯与溴发生反应的原理,用如图装置进行实验。

根据相关知识回答下列问题:
(1)装置Ⅱ中发生反应的化学方程式为__________
(2)实验开始时,关闭K2,开启K1和分液漏斗活塞,滴加苯和液溴的混合液,反应开始。过一会儿,在Ⅲ中可能观察到的现象是__________
(3)整套实验装置中能防止倒吸的装置有__________(填装置序号)。
(4)冷凝管的作用是__________
(5)你认为通过该实验后,有关苯跟溴反应的原理方面能得出的结论是__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L密闭容器中,800℃时反应2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.01 | 0.005 | 0.004 | 0.0035 | 0.0035 | 0.0035 |
(1)化学平衡常数K=________________________,K值越大,表示____________,已知:该反应K(300℃)>K(350℃),判断该反应是_____________________,(答“放热反应”或“吸热反应”)。
(2)利用表中数据,用NO表示从0~2s内该反应的平均速率v=___________________。
(3)当反应达到平衡后的t2时刻,将混合气体通过“分子筛”,可以及时将产物NO2分离出平衡体系,该操作对__________(填“正反应”或者“逆反应”)的反应速率影响大,请根据平衡移动原理,在下图中画出t2时刻后平衡移动的示意图:______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NA是阿伏加德罗常数的值,下列说法正确的是
A.2 g氦气(He)含有的氦原子数为NA
B.0.1 mol/L硫酸钠溶液中,含有0.2NA个Na+
C.100g质量分数为46%的乙醇(C2H5OH)水溶液,含有4NA个氧原子
D.16.25g FeCl3溶于水形成的Fe(OH)3胶体粒子数为0.1NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com