
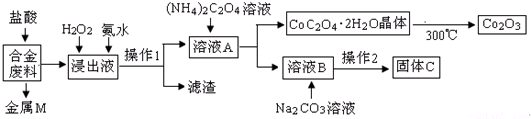
| 温度℃ | 10 | 30 | 60 | 90 |
| 浓度(mol/L) | 0.21 | 0.17 | 0.14 | 0.10 |
分析 合金废料(主要含Fe、Cu、Co、Li等,已知Co、Fe都是中等活泼金属)加入盐酸过滤得到金属M为不与盐酸反应的铜,浸出液中加入过氧化氢氧化亚铁离子为铁离子,加入氨水调节溶液PH使铁离子转化为氢氧化铁沉淀,通过操作Ⅰ过滤得到溶液A中加入草酸铵溶液沉淀钴离子过滤得到溶液B主要是锂离子的溶液,加入碳酸钠沉淀锂离子,过滤得到碳酸锂;结晶析出CoC2O4•2H2O足量空气煅烧得到氧化钴,以此解答该题.
解答 解:合金废料(主要含Fe、Cu、Co、Li等,已知Co、Fe都是中等活泼金属)加入盐酸过滤得到金属M为不与盐酸反应的铜,浸出液中加入过氧化氢氧化亚铁离子为铁离子,加入氨水调节溶液PH使铁离子转化为氢氧化铁沉淀,通过操作Ⅰ过滤得到溶液A中加入草酸铵溶液沉淀钴离子过滤得到溶液B主要是锂离子的溶液,加入碳酸钠沉淀锂离子,过滤得到碳酸锂;结晶析出CoC2O4•2H2O足量空气煅烧得到氧化钴,
(1)上述分析判断金属M为Cu,操作Ⅰ为过滤操作,故答案为:Cu;过滤;
(2)加入H2O2的作用是氧化亚铁离子为铁离子,反应的离子方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O;加入氨水的作用是调节溶液PH使Fe3+转化为Fe(OH)3沉淀,
故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;调节溶液的pH使Fe2+转化为Fe(OH)3沉淀;
(3)CoC2O4焙烧生成Co2O3、CO2和水,反应的化学方程式为4CoC2O4?2H2O+3O2$\frac{\underline{\;高温\;}}{\;}$2Co2O3+8 H2O+8CO2,
故答案为:4CoC2O4•2H2O+3O2$\frac{\underline{\;高温\;}}{\;}$2Co2O3+8H2O+8CO2;
(4)Li2CO3微溶于水,溶解度随温度升高而降低,为减少Li2CO3的溶解损失,蒸发浓缩后必须趁热过滤,90℃时c(Li2CO3)的浓度为0.10mol/L,则c(Li+)=0.20mol/L,c(CO32-)=0.10mol/L,则Ksp(Li2CO3)=0.20×0.20×0.10=4.0×10-3,
故答案为:减少Li2CO3的溶解损失;4.0×10-3.
点评 本题主要考查物质的分离提纯的综合应用,为高频考点,侧重于学生的分析能力和实验能力、计算能力的考查,综合性强,注意把握实验的流程和原理,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏大 | |
| B. | 将25 g CuSO4•5H2O溶于100 mL蒸馏水配制100 mL 1.0 mol•L-1 CuSO4溶液 | |
| C. | 配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出 | |
| D. | 配制100 mL 0.100 0 mol•L-1 K2Cr2O7溶液所选择的装置或仪器(夹持装置已略去)是 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ④癸烷⑤CH3COOH ⑥
④癸烷⑤CH3COOH ⑥ ⑦
⑦ ⑧
⑧ ⑨丙烷
⑨丙烷 ;
; ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子核内有8个中子的碳原子${\;}_{8}^{14}$C | |
| B. | 基态氧原子核外电子的轨道表示式: | |
| C. | HClO的结构式为H-Cl-O | |
| D. | Ca2+的结构示意图为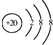 ,NH4Cl的电子式为 ,NH4Cl的电子式为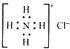 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | R的氧化物都能溶于水 | |
| B. | R的最高价氧化物对应的水化物都是H2RO4 | |
| C. | R一定是非金属元素 | |
| D. | R的最高价氧化物都能与NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu$→_{△}^{O_{2}}$CuO$\stackrel{稀H_{2}SO_{4}}{→}$CuSO4溶液$\stackrel{蒸发、结晶}{→}$CuSO4•5H2O | |
| B. | Fe$\stackrel{Cl_{2}}{→}$FeCl3$\stackrel{过量氨水}{→}$Fe(OH)3$\stackrel{灼烧}{→}$Fe2O3 | |
| C. | NaOH溶液$\stackrel{SO_{2}}{→}$Na2SO3$\stackrel{SO_{2}}{→}$NaHSO3$→_{灼烧}^{蒸干}$Na2SO4 | |
| D. | Al$→_{△}^{O_{2}}$Al2O3$\stackrel{HCl}{→}$AlCl3溶液$→_{△}^{蒸干}$AlCl3晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com