
| A、①②⑤ | B、③④⑤ |
| C、②④⑥ | D、③⑤⑥ |


科目:高中化学 来源: 题型:
| 化学式 | HF | HCN | H2C2O4 | |
| 电离常数 | Ka=3.5×10-4 | Ka=5.0×10-10 | Ka1=5.9×10-2 | Ka2=6.4×10-5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
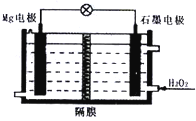 Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如图,该电池工作时,下列说法不正确的是( )
Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如图,该电池工作时,下列说法不正确的是( )| A、Mg电极是该电池的负极 |
| B、H2O2在石墨电极上的反应式:H2O2+2e-═2OH- |
| C、若隔膜为阳离子交换膜,则正极区有白色沉淀 |
| D、溶液中Cl-向石墨电极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含R元素的盐溶液可能显酸性,也可能显碱性 |
| B、Y分别与X和Z形成化合物,这些化合物的晶体类型相同 |
| C、Y元素氢化物的沸点比W元素氢化物的沸点低 |
| D、原子半径从小到大:X<Y<R<W |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、焓变是指1 mol物质参加反应时的能量变化 |
| B、反应放热时,△H>0;反应吸热时,△H<0 |
| C、在一个确定的化学反应关系中,反应物的总焓与生成物的总焓一定不同 |
| D、在一个确定的化学反应关系中,反应物的总焓总是高于生成物的总焓 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 橡皮筋在拉伸和收缩状态时结构如图,在其拉伸过程中有放热现象,反之吸热.25℃、101kPa时,下列化学反应的焓变、熵变和自发性与橡皮筋从拉伸状态到收缩状态一致的是( )
橡皮筋在拉伸和收缩状态时结构如图,在其拉伸过程中有放热现象,反之吸热.25℃、101kPa时,下列化学反应的焓变、熵变和自发性与橡皮筋从拉伸状态到收缩状态一致的是( )| A、Ba(OH)2?8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O |
| B、2H2+O2=2H2O |
| C、CaCO3=CaO+CO2↑ |
| D、2Na2O2+2H2O=4NaOH+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、二氧化硅与氢氧化钠溶液反应:SiO2+2Na++2OH-=NaSiO3+H2O |
| B、向Ba(OH)2溶液中逐滴滴入NaHSO4溶液至溶液刚好呈中性:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| C、过氧化钠固体与水反应:2O22-+2H2O=4OH-+O2↑ |
| D、向碳酸氢钠溶液中滴入少量石灰水:2HCO3-+Ca2++2OH-=CaCO3↓+2H2O+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、..向某无色溶液中加入BaCl2溶液有白色沉淀出现,再加入稀盐酸,沉淀不消失,则该溶液中一定含有SO
| ||
| B、.检验Na2CO3固体中是否混有NaHCO3,可向固体滴加稀盐酸,观察是否产生气体 | ||
| C、.焰色反应试验中,透过蓝色钴玻璃,可观察到Na+离子火焰呈黄色 | ||
| D、用丁达尔效应可鉴别FeCl3溶液和Fe(OH)3胶体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com