
ClO2是一种消毒杀菌效率高、二次污染小的水处理剂.实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4 2ClO2↑+K2SO4+2CO2↑+2H2O.下列说法正确的是( )
2ClO2↑+K2SO4+2CO2↑+2H2O.下列说法正确的是( )
|
| A. | KClO3在反应中得到电子 |
|
| B. | ClO2是氧化产物 |
|
| C. | H2C2O4在反应中被还原 |
|
| D. | 1mol KClO3参加反应有2 mol电子转移 |
考点:
氧化还原反应.
专题:
氧化还原反应专题.
分析:
2KClO3+H2C2O4+H2SO4 2ClO2↑+K2SO4+2CO2↑+2H2O(O均为﹣2价)中,Cl元素的化合价由+5价降低为+4价,C元素的化合价由+3价升高到+4价,以此来解答.
2ClO2↑+K2SO4+2CO2↑+2H2O(O均为﹣2价)中,Cl元素的化合价由+5价降低为+4价,C元素的化合价由+3价升高到+4价,以此来解答.
解答:
解:A.Cl元素的化合价由+5价降低为+4价,所以氯酸钾得电子为氧化剂,故A正确;
B.Cl元素的化合价由+5价降低为+4价,所以氯酸钾对应的产物ClO2是还原产物,故B错误;
C.H2C2O4为还原剂,在反应中被氧化,故C错误;
D.1molKClO3参加反应有1mol×(5﹣4)=1mol,故D错误;
故选A.
点评:
本题考查氧化还原反应,明确元素的化合价变化是解答本题的关键,并注意氧化剂、还原剂中元素的变化来解答,难度不大.


科目:高中化学 来源: 题型:
工业上生产硫酸时,利用催化氧化反应将SO2 转化为SO3是一个关键步骤。压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为: SO2 7% ,O2 11%,N2 82%):
SO2 7% ,O2 11%,N2 82%):
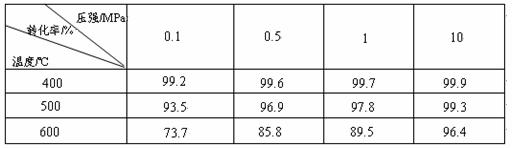
(1)已知SO2的氧化是放热反应,如何利用表中数据推断此结论?
;
(2)在大400~500℃时,SO2的催化氧化采用常压而不是高压,主要原因是:
;
(3)选择适宜的催化剂,是否可以提高SO2的转化率? (填“是”或“否”),是否可以增大该反应所放出的热量? (填“是”或“否”);
(4)为提高SO3吸收率,实际生产中用 吸收SO3;
(5)已知:2SO2(g)+O2(g)=2SO3(g);△H=-196.6kJ·mol-1,计算每生产1万吨98%硫酸所需要的SO3质量和由SO2生产这些SO3所放出的热量。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质在水溶液中的电离方程式错误的是( )
|
| A. | NaHCO3═Na++H++CO32﹣ | B. | NaHSO4═Na++H++SO42﹣ |
|
| C. | MgCl2═Mg2++2Cl﹣ | D. | Ba(OH)2═Ba2++2OH﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应属于非氧化还原反应的是( )
|
| A. | Fe2O3+3CO | B. | NH4NO3 |
|
| C. | CaCO3 | D. | 4CuO |
查看答案和解析>>
科目:高中化学 来源: 题型:
吸进人体内的氧有2%转化为氧化性极强的活性氧,这些活性氧能加速人体衰老,被称为“生命杀手”,中国科学家尝试用Na2SeO3清除人体内的活性氧,则Na2SeO3的作用是( )
|
| A. | 还原剂 | B. | 氧化剂 |
|
| C. | 既是氧化剂又是还原剂 | D. | 以上均不是 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)请按照下面的实验步骤制备氢氧化铁胶体,检验胶体的性质,首先用烧杯取少量蒸馏水,用酒精灯加热至沸腾,然后逐滴向烧杯中滴加FeCl3饱和溶液,并继续煮沸至液体呈透明的红褐色即得氢氧化铁胶体.写出制备Fe(OH)3胶体的化学方程式 ,怎样检验你是否制得了胶体?(写出具体操作) .
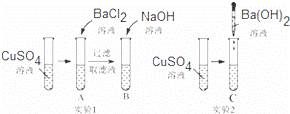
(2)仔细分析如图中的实验:
A、B、C试管中的现象如下表所示:
| A | B | C |
| 产生白色沉定,溶液仍为蓝色 | 产生蓝色沉定,溶液变为无色 | 产生蓝色沉淀,溶液为无色 |
写出A、B、C试管中发生反应的离子方程式:
A. ;B. .C. .
查看答案和解析>>
科目:高中化学 来源: 题型:
基态铬原子的电子排布式是( )
|
| A. | 1S22S22p63S23p64S14p5 | B. | 1S22S22p63S23p63d6 |
|
| C. | 1S22S22p63S23p64S23d4 | D. | 1S22S22p63S23P63d54S1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 工业上回收利用某合金废料(主要含Fe、Cu、Co、Li等,已知Co、Fe都是中等活泼金属)的工艺流程如下:
工业上回收利用某合金废料(主要含Fe、Cu、Co、Li等,已知Co、Fe都是中等活泼金属)的工艺流程如下:
| |
(2)加入H2O2的作用是(用离子方程式表示) ,加入氨水的作用是 。
(3)充分焙烧的化学方程式为 。
(4)已知Li2CO3微溶于水,其饱和溶液的浓度与温度关系见下表。90℃时Ksp(Li2CO3)的值为 。
| 温度/℃ | 10 | 30 | 60 | 90 |
| 浓度/mol·L-1 | 0.21 | 0.17 | 0.14 | 0.10 |
(5)用惰性电极电解熔融Li2CO3制取锂,阳极生成两种气体,则阳极的电极反应式为
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com