
 氮可形成多种氧化物,如NO、NO2、N2O4等.已知NO2和N2O4的结构式分别是
氮可形成多种氧化物,如NO、NO2、N2O4等.已知NO2和N2O4的结构式分别是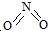 和
和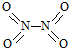 .实验测得N-N键键能为167kJ•mol-1,NO2中氮氧键的平均键能为466kJ•mol-1,N2O4中氮氧键的平均键能为438.5kJ•mol-1.
.实验测得N-N键键能为167kJ•mol-1,NO2中氮氧键的平均键能为466kJ•mol-1,N2O4中氮氧键的平均键能为438.5kJ•mol-1.| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.050 | n2 | 0.080 | 0.080 |
分析 (1)化学反应的反应热=反应物的总键能-生成物的总键能,注明物质的聚集状态与放热反应书写热化学方程式;
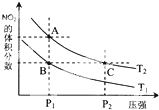
(2)A.压强越高,反应速率越快;
B.B、C两点的二氧化氮体积分数相同,为等效平衡;
C.A、C点温度相同,C的压强增大,体积缩小,气体颜色加深;
D.B的二氧化氮体积分数小于A点,该反应是吸热反应,温度升高,平衡正向移动,二氧化氮的体积分数增大,所以T2>T1;
(3)①从反应开始直至20 s时,N2O4(g)的物质的量增加0.05mol,则二氧化氮的物质的量减少0.1mol,浓度减少0.1mol÷2L=0.05mol/L,再根据v=$\frac{△c}{△t}$计算v(NO2);
②60s和80s时四氧化二氮的物质的量相同,说明反应达到平衡状态,所以二氧化氮的物质的量不变;
四氧化二氮平衡时的浓度为0.08mol÷2L=0.04mol/L,二氧化氮的平衡浓度为0.40mol÷2L-2×0.04mol/L=0.12mol/L,再根据K=$\frac{c({N}_{2}{O}_{4})}{{c}^{2}(N{O}_{2})}$计算平衡常数;
二氧化氮生成四氧化二氮的反应是放热反应,所以升高温度,平衡逆向移动,平衡常数减小;
③若在相同情况下最初向该容器充入的是N2O4气体,要达到上述同样的平衡状态,即为等效平衡状态,则将0.4mol的二氧化氮完全转化为四氧化二氮的物质的量是0.2mol.
解答 解:(1)根据化学反应的反应热=反应物的总键能-生成物的总键能,所以N2O4(g)?2NO2(g)的反应热△H=438.5 kJ•mol-1×4+167kJ•mol-1-466 kJ•mol-1×4=+57 Kj,•mol-1,所以N2O4转化为NO2的热化学方程式为:N2O4(g)?2NO2(g)△H=+57 kJ•mol-1,
故答案为:N2O4(g)?2NO2(g)△H=+57 kJ•mol-1;
(2)A.C点压强大于A点,所以C点的反应速率快,故A错误;
B.B、C两点的二氧化氮体积分数相同,为等效平衡,则气体的平均相对分子质量相同,故B错误;
C.A、C点温度相同,C的压强增大,体积缩小,气体颜色加深,尽管平衡逆向移动,但最终气体的颜色比原平衡时深,则A浅,C深,故C错误;
D.B的二氧化氮体积分数小于A点,该反应是吸热反应,温度升高,平衡正向移动,二氧化氮的体积分数增大,所以T2>T1,A、B压强相同,则由状态B到状态A,可以用加热的方法,故D正确,
故选:D;
(3)①在上述条件下,该反应为2NO2(g)?N2O4(g),从反应开始直至20 s时,N2O4(g)的物质的量增加0.05mol,则二氧化氮的物质的量减少0.1mol,浓度减少0.1mol÷2L=0.05mol/L,二氧化氮的平均反应速率为0.05mol/L÷20s=0.0025mol•(L•s)-1,
故答案为:0.0025mol•(L•s)-1;
②60s和80s时四氧化二氮的物质的量相同,说明反应达到平衡状态,所以二氧化氮的物质的量不变,则n3=n4;四氧化二氮平衡时的浓度为0.08mol÷2L=0.04mol/L,二氧化氮的平衡浓度为0.40mol÷2L-2×0.04mol/L=0.12mol/L,则平衡常数K=$\frac{c({N}_{2}{O}_{4})}{{c}^{2}(N{O}_{2})}$=$\frac{0.04}{0.1{2}^{2}}$=2.8;
二氧化氮生成四氧化二氮的反应是放热反应,所以升高温度,平衡逆向移动,平衡常数减小,
故答案为:=;2.8;减小;
③若在相同情况下最初向该容器充入的是N2O4气体,要达到上述同样的平衡状态,即为等效平衡状态,则将0.4mol的二氧化氮完全转化为四氧化二氮的物质的量是0.2mol,则四氧化二氮的起始浓度为0.20mol÷2L=0.10mol/L,
故答案为:0.10.
点评 本题考查反应速率、平衡常数的计算、反应热的计算、平衡移动的判断、化学平衡图象、等效平衡的应用等,难度中等,注意对等效平衡的理解掌握.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | H+、NH4+、I-、Fe3+ | B. | K+、Ag+、Cl-、NO3- | ||
| C. | ClO-、Fe2+、SO42-、Na+ | D. | Ba2+、Na+、OH-、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
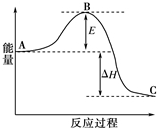 合成氨反应N2(g)+3H2(g)?2NH3(g),反应过程的能量变化如图所示.已知N2(g)与H2(g)反应生成17g NH3(g),放出46.1kJ的热量.
合成氨反应N2(g)+3H2(g)?2NH3(g),反应过程的能量变化如图所示.已知N2(g)与H2(g)反应生成17g NH3(g),放出46.1kJ的热量.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氨水导电能力比BaSO4的水溶液强,所以氨水是强电解质,BaSO4是弱电解质 | |
| B. | 已知H2C2O4是弱酸,其电离方程式为:H2C2O4?2H++C2O42- | |
| C. | 若反应C(s)+CO2(g)?2CO(g)在常温下不能自发,则该反应的△H>0 | |
| D. | 工业合成氨温度控制在500℃,目的是为了提高产率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | [HCN]<[CN-] | B. | [Na+]<[CN-] | ||
| C. | [HCN]-[CN-]=[OH-] | D. | [HCN]+[CN-]=0.1mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
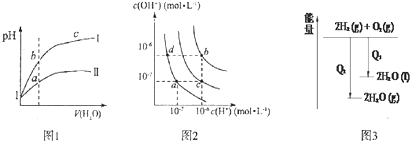
| A. | 图l表示同温度下,pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强 | |
| B. | 图2中纯水仅升高温度,就可以从a点变到c点 | |
| C. | 图2中在b点对应温度下,将pH=2的H2SO4与pH=10的NaOH溶液等体积混合后,溶液显中性 | |
| D. | 图3表示氢气与氧气反应中的能量变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 在X点时,由H2O电离出的c(H+)相等,c(M+)=c(R+) | |
| B. | 稀释前,c(ROH)=10c(MOH) | |
| C. | 稀释前的ROH与等体积pH=1的H2SO4混合后所得溶液显酸性 | |
| D. | 等体积等浓度的MOH和HCl混合后,溶液中离子浓度大小关系:c(Cl-)>c(M+)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷与氯气反应生成一氯甲烷 | B. | 苯与氢气反应生成环己烷 | ||
| C. | 乙烯与溴反应生成1,2-二溴乙烷 | D. | 乙醇与氧气反应生成乙醛 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com