
 .P元素属于p区元素,
.P元素属于p区元素,
分析 X、Y、Z、M、N、Q、P为元素周期表前四周期的7种元素,X原子核外的M层中只有两对成对电子,核外电子排布应为1s22s22p63s23p4,X为S元素;Y原子核外的L层电子数是K层的两倍,Y有2个电子层,最外层电子数为4,故Y为C元素;Z是地壳内含量最高的元素,为O元素;M的内层电子数是最外层电子数的9倍,M只能处于第四周期,最外层电子数只能为2,内层电子总数为18,核外电子总数为20,故M为Ca元素;N的原子序数比M小1,则N为K元素;Q在元素周期表的各元素中电负性最大,Q为F元素;P元素的第三电子层处于全充满状态,第四电子层只有一个电子,原子核外电子数=2+8+18+1=29,则P为Cu元素,据此解答.
解答 解:X、Y、Z、M、N、Q、P为元素周期表前四周期的7种元素,X原子核外的M层中只有两对成对电子,核外电子排布应为1s22s22p63s23p4,X为S元素;Y原子核外的L层电子数是K层的两倍,Y有2个电子层,最外层电子数为4,故Y为C元素;Z是地壳内含量最高的元素,为O元素;M的内层电子数是最外层电子数的9倍,M只能处于第四周期,最外层电子数只能为2,内层电子总数为18,核外电子总数为20,故M为Ca元素;N的原子序数比M小1,则N为K元素;Q在元素周期表的各元素中电负性最大,Q为F元素;P元素的第三电子层处于全充满状态,第四电子层只有一个电子,原子核外电子数=2+8+18+1=29,则P为Cu元素,
(1)X为S元素,元素在周期表中的位置是:第三周期ⅥA族,外围电子排布为3s23p4,它的外围电子的电子排布图为 ,最后1个电子填充p能级,属于p区元素,
,最后1个电子填充p能级,属于p区元素,
故答案为:第三周期ⅥA族; ;p;
;p;
(2)SO2分子中S原子价层电子对数=2+$\frac{6-2×2}{2}$=3,S原子含有1对孤电子对,故其立体结构是V型,CO2分子C原子呈2个σ键、没有孤电子对,C的杂化轨道类型为sp杂化,SO2为极性分子,CO2为非极性分子,H2O为极性溶剂,极性分子易溶于极性溶剂,故SO2的溶解度较大,
故答案为:V型;sp杂化;SO2;SO2为极性分子,CO2为非极性分子,H2O为极性溶剂,极性分子易溶于极性溶剂,故SO2的溶解度较大;
(3)含有K元素的盐的焰色反应为紫色,许多金属盐都可以发生焰色反应,其原因是电子由较高能级跃迁到较低能级时,以光的形式释放能量,
故答案为:紫;电子由较高能级跃迁到较低能级时,以光的形式释放能量;
(4)元素Ca与元素F形成晶体,晶胞中蓝色球数目=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4、蓝色球为8个,故化学式为CaF2,该化合物的摩尔质量为D g/mol,晶胞质量=4×$\frac{D}{N{\;}_{A}}$g,晶胞边长为a pm,则晶胞体积=(a×10-10 cm)3=a3××10-30 cm3,则晶胞密度=$\frac{4×\frac{D}{{N}_{A}}}{a{\;}^{3}×10{\;}^{-30}cm{\;}^{3}}$=$\frac{4×10{\;}^{30}×D}{a{\;}^{3}×N{\;}_{A}}$g/cm3,
故答案为:$\frac{4×10{\;}^{30}×D}{a{\;}^{3}×N{\;}_{A}}$;
(5)三聚氰胺分子中处于环上的N原子成2个σ键,有1对孤电子对,采取sp2杂化,氨基中N原子成3个σ键,含有1对孤电子对,N原子采取sp3杂化,单键为σ键,双键含有1个σ键、1个π键,故1个三聚氰胺分子含有15个σ键,则1mol三聚氰胺分子中σ键的数目为15NA,
故答案为:sp2、sp3;15NA.
点评 本题是对物质结构的考查,涉及核外电子的排布、分子结构与性质、晶胞计算等,(4)中注意利用均摊法计算晶胞的质量,难度中等.


 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 单位时间里生成n mol C,同时生成1.5n mol D | |
| B. | 增大压强正反应速率增大,逆反应速率减小 | |
| C. | 单位时间里有4n mol A消耗,同时有5n mol B生成 | |
| D. | 容器里A、B、C、D的浓度比是4:5:4:6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 鉴别乙烷与乙烯或除去乙烷中的少量乙烯杂质都可用高锰酸钾酸性溶液 | |
| B. | 某同学需用480 mL 2.0 moI•L-1氢氧化钠溶液进行实验,则配制该溶液时他称取氢氧化钠固体质量一定是38.4 g | |
| C. | 向含Fe3+的溶液中加入KSCN溶液时一定有红褐色沉淀产生 | |
| D. | 硝酸钾和稀硫酸的混合溶液中加入铜粉后,溶液会慢慢变蓝 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 容器编号 | 实验条件 | 平衡时反应中的能量变化 |
| Ⅰ | 恒温恒容 | 放热Q1kJ |
| Ⅱ | 恒温恒压 | 放热Q2kJ |
| Ⅲ | 恒容绝热 | 放热Q3kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
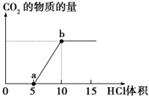 钠是活泼的碱金属元素,钠及其化合物在生产和生活中有广泛应用.
钠是活泼的碱金属元素,钠及其化合物在生产和生活中有广泛应用.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 物质A在一定条件下反应制得新型纤维酸类降脂药克利贝特,其结构简式如图所示,下列有关叙述正确的是( )
物质A在一定条件下反应制得新型纤维酸类降脂药克利贝特,其结构简式如图所示,下列有关叙述正确的是( )| A. | 物质A分子中含有2个手性碳原子 | |
| B. | 物质A分子中所有碳原子可能位于同一平面内 | |
| C. | 1 mol物质A最多可以与含4molBr2的溴水反应 | |
| D. | 物质A可以发生加成反应、氧化反应、水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁的冶炼过程是通过置换反应得到单质铁 | |
| B. | 太阳能电池可采用硅材料制作,其应用有利于环保、节能 | |
| C. | 化学家采用玛瑙研钵磨擦固体反应物进行溶剂合成,玛瑙的主要成分是硅酸盐 | |
| D. | 包装食品里常有硅胶、生石灰、还原铁粉三类小包,其作用相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com