
【题目】下列装置图或曲线图与对应的叙述相符的是
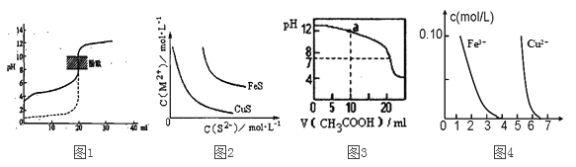
A. 如图1所示,用0.1mol/LNaOH溶液分别滴定相同物质的量浓度、相同体积的盐酸和醋酸,其中实线表示的是滴定盐酸的曲线
B. 某温度下FeS、CuS的沉淀溶解平衡曲线如图2所示,纵坐标c(M2+)代表Fe2+或Cu2+的浓度,横坐标c(S2—)代表S2—浓度。在物质的量浓度相等的Fe2+和Cu2+的溶液中滴加硫化钠溶液,首先沉淀的离子为Fe2+
C. 如图3所示,用0.1mol/LCH3COOH溶液滴定20mL0.1mol/LNaOH溶液的滴定曲线,当pH=7时:c(Na+)=c(CH3COO—)>c(OH—)=c(H+)
D. 据图4,若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH在5.5左右
【答案】C
【解析】A.用0.1mol/LNaOH溶液滴定醋酸时,随着加入氢氧化钠的量的增加,醋酸会电离出一部分氢离子,所以出现的pH值突越要缓慢,故A错误;B.依据图象分析可知,硫化铜溶度积小于硫化亚铁,同浓度Fe2+和Cu2+的溶液中滴加硫化钠溶液,先析出的沉淀是硫化铜,故B错误;C.反应后溶液pH=7,依据溶液中电荷守恒分析,用0.1mol/LCH3COOH溶液滴定20ml0.1mol/LNaOH溶液,反应生成醋酸钠,溶液呈中性,溶液中存在电荷守恒,c(H+)+c(Na+)=c(OH-)+c(CH3COO-),c(H+)=c(OH-),则c(CH3COO-)=c(Na+),得到当pH=7时:c(Na+)=c(CH3COO-)>c(OH-)=c(H+),故C正确;D.分析图象可知铁离子完全沉淀的pH为3.7,加入氧化铜会调节溶液pH,到pH=5.5时铜离子会沉淀,应调节溶液pH小于5.5,故D错误;故选C。


科目:高中化学 来源: 题型:
【题目】如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。现用该浓硫酸配制450mL 1mol/L的稀硫酸。可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平。

请回答下列问题:
(1)配制稀硫酸时,上述仪器中不需要使用的有______(选填序号),还缺少的仪器有______(写仪器名称);
(2)经计算,配制上述稀硫酸时需要用量筒量取上述浓硫酸的体积为______mL(保留一位小数)。
(3)接下来的操作是将上述所取浓硫酸进行稀释,稀释的操作是________________、__________________。
(4)在溶液配制过程中,下列操作会引起所配置硫酸的浓度偏低的有_________(填序号)
A.用量筒量取浓硫酸读数时仰视刻度线;
B.转移稀释的硫酸溶液后未洗涤烧杯和玻璃棒;
C.浓硫酸稀释后未经冷却即转移到容量瓶中;
D.容量瓶未干燥就用来配置溶液;
E.定容后摇匀溶液,发现液面低于刻度线,再加入少量水使液面与刻度线相平;
F.定容时仰视刻度线。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某主族元素R的最高正化合价与最低负化合价的代数和为4,由此可以判断( )
A.R一定是第四周期元素
B.R一定是ⅣA族元素
C.R的气态氢化物比同周期其他元素气态氢化物稳定
D.R气态氢化物化学式为H2R
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)6.02×1022个Na+ 的物质的量为_________________;
(2)标准状况下8.96L CO2的物质的量为_________________;
(3)在同温同压下,相同体积的O2和CH4,原子数目之比为______________;
(4)质量分数为98%的浓硫酸(溶液密度为1.84g/cm3)中H2SO4的物质的量浓度为__________;
(5)27.75 g某+2价金属的氯化物(MCl2)中含有3.01×1023个Cl-,则M的相对原子质量为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝与过量的稀盐酸反应,为了加快反应速率,同时几乎不影响生成的氢气总量,不可以采取的措施是( )
A.加热,升高溶液温度
B.加入适量的水
C.加入少量CuSO4溶液
D.加入浓度较大的盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锗![]() 是典型的半导体元素,在电子、材料等领域应用广泛
是典型的半导体元素,在电子、材料等领域应用广泛![]() 回答下列问题:
回答下列问题:
(1)基态Ge原子的核外电子排布式为![]() ______,有______个未成对电子.
______,有______个未成对电子.
(2)![]() 与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键
与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键![]() 从原子结构角度分析,原因是______.
从原子结构角度分析,原因是______.
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因______.
|
|
| |
熔点 |
| 26 | 146 |
沸点 |
| 186 | 约400 |
(4)光催化还原![]() 制备
制备![]() 反应中,带状纳米
反应中,带状纳米![]() 是该反应的良好催化剂
是该反应的良好催化剂![]() 、Ge、O电负性由大至小的顺序是______
、Ge、O电负性由大至小的顺序是______
![]() 单晶具有金刚石型结构,其中Ge原子的杂化方式为______微粒之间存在的作用力是______.
单晶具有金刚石型结构,其中Ge原子的杂化方式为______微粒之间存在的作用力是______.
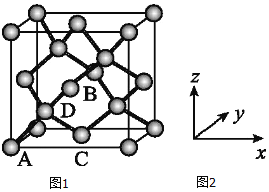
(6)晶胞有两个基本要素: ![]() 原子坐标参数,表示晶胞内部各原子的相对位置,如图
原子坐标参数,表示晶胞内部各原子的相对位置,如图![]() 、
、![]() 为Ge单晶的晶胞,其中原子坐标参数A为
为Ge单晶的晶胞,其中原子坐标参数A为![]() ;B为
;B为![]() ;C为
;C为![]() 则D原子的坐标参数为______.
则D原子的坐标参数为______.
![]() 晶胞参数,描述晶胞的大小和形状,已知Ge单晶的晶胞参数
晶胞参数,描述晶胞的大小和形状,已知Ge单晶的晶胞参数![]() ,其密度为______
,其密度为______ ![]() 列出计算式即可
列出计算式即可![]() .
.
查看答案和解析>>
科目:高中化学 来源: 题型:
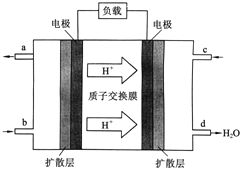
【题目】中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆![]() 甲醇燃料电池的工作原理如图所示.
甲醇燃料电池的工作原理如图所示.
![]() 该电池工作时,b口通入的物质为______,c口通入的物质为______.
该电池工作时,b口通入的物质为______,c口通入的物质为______.
![]() 该电池负极的电极反应式为:______.
该电池负极的电极反应式为:______.
![]() 工作一段时间后,当
工作一段时间后,当![]() 甲醇完全反应生成
甲醇完全反应生成![]() 时,有______
时,有______![]() 个电子转移.
个电子转移.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,某溶液中由水电离产生的c(H+)等于10-13mol·L-1,该溶液的溶质不可能是( )
A. NaHSO4 B. NaCl C. HCl D. Ba(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯环结构中,不存在单双键交替结构可以作为证据的事实是
①苯不能使酸性高锰酸钾溶液褪色
②苯能在一定条件下跟氢气发生加成反应生成环己烷
③经实验测得邻二甲苯(![]() )只有一种结构
)只有一种结构
④苯在FeBr3存在下同液溴可发生取代反应,但不随溴水褪色
A. ②③④ B. ①②④ C. ①③④ D. ①②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com