
| A、2Na+2H2O=H2↑+2NaOH |
| B、Cl2+NaOH=NaCl+NaClO+H2O |
| C、SO2+Cl2+2H2O=2HCl+H2SO4 |
| D、2F2+2H2O=4HF+O2 |


科目:高中化学 来源: 题型:
| A、常温下,正丁烷的燃烧热为-2878.0kJ/mol |
| B、相同质量的丙烷和正丁烷分别完全燃烧,前者需要的氧气多,产生的热量也多 |
| C、常温下,CO的燃烧热为566.0 kJ/mol |
| D、人类利用的能源都是通过化学反应获得的 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、天然药物无毒副作用,所以,多多益善 |
| B、氯气可用作消毒剂和漂白剂,是因为氯气与水反应生成的次氯酸具有强氧化性 |
| C、酸雨指pH值小于7的降水 |
| D、误食重金属盐会中毒,是因为重金属盐能使蛋白质盐析 |
查看答案和解析>>
科目:高中化学 来源: 题型:
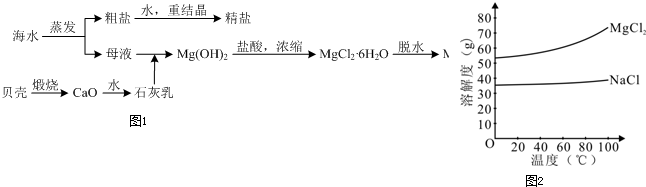
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、此反应可在瞬间产生大量高温气体,推动火箭飞行 |
| B、此反应是氧化还原反应,N2O4是氧化剂 |
| C、每生成1mol N2,该反应转移电子8mol |
| D、此反应中R的分子式为C2H8N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N2既是氧化产物又是还原产物 |
| B、当x=1时,每生成2.5 mol N2,被氧化的气体有3 mol |
| C、当x=2时,有1 mol气体被还原,转移电子4 mol |
| D、反应通式配平表示为:6NOx+4xNH3═(3+2x)N2+6xH2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③④ | B、②③ |
| C、②③④ | D、全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.24g | B、0.64g |
| C、0.4g | D、1.2g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com