
甲、乙、丙、丁为四种主族元素,甲元素与乙、丙、丁三种元素相邻,甲、乙的原子序数之和等于丙的原子序数;这四种元素原子的最外层电子数之和为20。下列判断正确的是
A.原子半径:丙>乙>甲>丁
B.气态氢化物的稳定性:甲>丙
C.最高价氧化物对应的水化物的酸性:丁>甲
D.乙和甲、乙和丁所能形成的化合物都是剧毒物质
| |
科目:高中化学 来源: 题型:
下列指定反应的离子方程式正确的是( )
A.Cu溶于稀HNO3:
Cu+2H++NO ===Cu2++NO2↑+H2O
===Cu2++NO2↑+H2O
B.(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制
Fe(OH)2:Fe2++2OH-===Fe(OH)2↓
C.用CH3COOH溶解CaCO3:
CaCO3+2H+===Ca2++H2O+CO2↑
D.向NaAlO2溶液中通入过量CO2制Al(OH)3:
CO2+AlO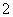 +2H2O===Al(OH)3↓+HCO
+2H2O===Al(OH)3↓+HCO
查看答案和解析>>
科目:高中化学 来源: 题型:
关于乙醇的说法不正确的是( )
A.乙醇是具有特殊气味的液体
B.乙醇分子里含有6个氢原子,它们的性质是完全一样的
C.乙醇易挥发,与水任意比互溶
D.乙酸的熔沸点比乙醇高
查看答案和解析>>
科目:高中化学 来源: 题型:
M、N为短周期的两种元素,M元素原子的最外层电子数≤4,N元素原子的最外层电子数>4,下列对其中说法正确的是
A.M、N可能为金属
B.若M、N为同周期元素,则原子半径M<N
C.M、N元素的单质可能与水发生置换反应
D.M、N形成的离子化合物不能体现强氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
能正确表示下列反应的离子方程式为
A.硫化亚铁溶于稀硝酸中:FeS+2H+=Fe2++H2S↑
B.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O
C.硫代硫酸钠溶液中滴入稀盐酸:S2O32-+2H+=S↓+SO2↑+H2O
D.在NaHSO4溶液中滴加Ba(OH)2至中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)生产甲醇的原料CO、H2可由下列反应制取:CH4(g)+H2O(g)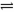 CO(g)+3H2(g),试回答下列问题。
CO(g)+3H2(g),试回答下列问题。
①已知:CH4(g)+3/2O2(g)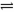 CO(g)+2H2O(g) △H1
CO(g)+2H2O(g) △H1
H2(g)+1/2O2(g)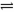 H2O(g) △H2
H2O(g) △H2
 则CH4(g)+H2O(g)
则CH4(g)+H2O(g)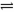 CO(g)+3H2(g)的△H=_____(用含△H1、△H2的式子表示)
CO(g)+3H2(g)的△H=_____(用含△H1、△H2的式子表示)
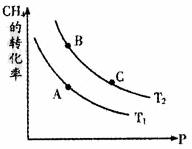
②一定条件下反应CH4(g)+H2O(g)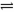 CO+3H2(g)中CH4的平衡转化率与温度、压强的关系如图,且T2>T1,则上述反应的△H________0(填“<”、“>”、“=”,下同),A、B处对应平衡常数(KA、KB)的大小关系为KA________KB。
CO+3H2(g)中CH4的平衡转化率与温度、压强的关系如图,且T2>T1,则上述反应的△H________0(填“<”、“>”、“=”,下同),A、B处对应平衡常数(KA、KB)的大小关系为KA________KB。
③维持温度T2,将0.04mol CH4(g)和0.04mol H2O(g)通入容积为1L的定容密闭容器中发生反应,平衡时达到B点,测得CH4的转化率为50%,该反应在此温度下的平衡常数KB=___________,下列现象能说明该反应已经达到平衡状态的是___________(填写序号)

④在上述B点平衡基础上,向容器中再通入a mol CH4和a mol H2O气体,使之在C点重新达平衡,此时测得CO有0.03 mol,则a=______________。
(2)汽车尾气中的一氧化碳是大气污染物,可通过反应:CO(g)+1/2O2(g)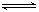 CO2(g)降低其浓度。
CO2(g)降低其浓度。
①某温度下,在两个容器中进行上述反应,容器中各物质的起始浓度及正逆反应速率关系如下表所示。请填写表中的空格。
| 容器编号 | c(CO)/mol·L-1 | c(O2)/mol·L-1 | c(CO2)/mol·L-1 | v (正)和v (逆)比较 |
| I | 2.0×10-4 | 4.0×10-4 | 4.0×10-2 | v (正)= v (逆) |
| Ⅱ | 3.0×10-4 | 4.0×10-4 | 5.0×10-2 | v (正)_____v (逆) |
②相同温度下,某汽车尾气中CO、CO2的浓度分别为1.0×10-5mol/L和1.0×10-4mol/L。若在汽车的排气管上增加一个补燃器,不断补充O2并使其浓度保持为1.0×10-4mol/L,则最终尾气中CO的浓度为________________mol/L(请保留两位有效数字)。
(3)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10-4mol/L ,则生成沉淀所需CaCl2溶液的最小浓度为____________ mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列溶液中不能大量共存的离子组是( )
①NH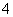 、Ag+、PO
、Ag+、PO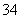 、Cl-
、Cl-
②Fe3+、H+、I-、HCO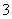
③Al3+、Mg2+、SO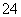 、CO
、CO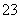
④在pH=12的溶液中,K+、Cl-、HCO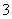 、Na+
、Na+
⑤在pH=0的溶液中,Na+、NO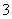 、SO
、SO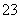 、K+
、K+
A.仅①③④ B.仅①②③
C.全部 D.仅①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关溶液组成的描述合理的是( )
A.无色溶液中可能大量存在Al3+、NH 、Cl-、S2-
、Cl-、S2-
B.酸性溶液中可能大量存在Na+、ClO-、SO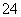 、I-
、I-
C.弱碱性溶液中可能大量存在Na+、K+、Cl-、HCO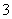
D.中性溶液中可能大量存在Fe3+、K+、Cl-、SO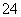
查看答案和解析>>
科目:高中化学 来源: 题型:
某地煤矸石经预处理后含SiO2(63%)、Al2O3(25%)、Fe2O3(5%)及少量钙镁的化合物等,一种综合利用煤矸石的工艺流程如图K72所示。
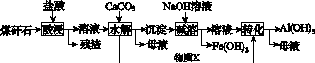
图K72
(1)写出“酸浸”过程中主要反应的离子方程式:
________________________________________________________________________、
________________________________________________________________________。
(2)“酸浸”时铝浸出率的影响因素可能有________________、________________。(写出2个)
(3)物质X的化学式为________。“碱溶”时反应的离子方程式为__________________________。
(4)已知Fe3+开始沉淀和沉淀完全的pH分别为2.1和3.2,Al3+开始沉淀和沉淀完全的pH分别为4.1和5.4。
为了获得Al(OH)3产品,从煤矸石的盐酸浸取液开始,若只用CaCO3一种试剂,后续的操作过程是________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(5)以煤矸石为原料还可以开发其他产品,例如在煤矸石的盐酸浸取液除铁后,常温下向AlCl3溶液中不断通入HCl气体,可析出大量AlCl3·6H2O晶体。结合化学平衡移动原理解释析出晶体的原因:________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com