
A��B��C��D��E����Ԫ�أ�����ԭ�ӵĺ˵�������ε����Ҿ�С��18��AԪ��ԭ�Ӻ���ֻ��1�����ӣ�C�ǵؿ��к�������Ԫ�أ�B��C���γ����ֻ�����BC��BC2��B���������������۾���ֵ��ȣ�BC�ж���BC2���������DԪ�ص�����������������Ӳ���������֮һ��E��������Arԭ����ͬ�ĵ��Ӳ�ṹ��
��1��д��A��C����Ԫ�صķ��ţ�A �� C ��
��2��д��Dԭ�Ӻ�E�����ӵĽṹʾ��ͼ��Dԭ�� ��E������ ��
��3����A��B��C��D����Ԫ����ɵij���������Ļ�ѧʽΪ ��
����뷽��ʽΪ ��
��4��д��A��C��D����Ԫ����ɵij����������ϡ��Һ�������º�E�ĵ��ʷ�Ӧ�Ļ�ѧ����ʽ ��
��1��H�� O��
��2�� 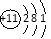
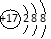
��3��NaHCO3 �� NaHCO3 = Na+ + HCO3�� ��
��4��Cl2 + 2NaOH = NaCl + NaClO +H2O��
��������
���������AԪ��ԭ�Ӻ���ֻ��1�����ӣ�����ΪHԪ�أ�C�ǵؿ��к�������Ԫ�أ�ΪOԪ�أ�B��C���γ����ֻ�����BC��BC2��B���������������۾���ֵ��ȣ�BC�ж���BC2�������������BΪ̼Ԫ�أ�DԪ�ص�����������������Ӳ���������֮һ��Ϊ��Ԫ�أ�E��������Arԭ����ͬ�ĵ��Ӳ�ṹ������Ϊ��Ԫ�ء���3����A��B��C��D����Ԫ����ɵij���������Ļ�ѧʽΪNaHCO3��HCO3��Ϊ��Ԫ�������ʽ�������ܲ���4�������ͼ���绯��Ӧ��
���㣺����Ԫ�ؼ��仯������ƶϡ�


 �ľ�ͼ���ʱ�ȷ�ϵ�д�
�ľ�ͼ���ʱ�ȷ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ�˴��и�һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
��1����״���£�1.92 gij��������Ϊ672 mL������������Է�������Ϊ________��
��2����25����101 kPa�������£�ͬ������CH4��A��������֮����15��8����A��Ħ������Ϊ________��
��3��A��B����������ɵĻ������8.6 g���ڱ�״�������Ϊ8.96 L����֪A��B�����ʵ���֮��Ϊ3��1����Է�������֮��Ϊ14��1���ɴ˿��ƶ�B������________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ��һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���и������ʣ�����������ʡ�������˳�����е��ǣ� ��
A���ɱ��������Ȼ��� B����ʯ�ҡ����ס���ʯ��
C���ռҺ̬������� D������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ������У��һ��ѧ����ĩ������ѧ�Ծ��������棩 ���ͣ�ѡ����
���и���������ָ��������һ���ܴ���������ǣ�������
A���ڼ��������ܲ�����������Һ�У�Al3���� Fe2+��SO42����NO3��
B��0��1 mol��L-1NaAlO2 ��Һ: H����Na����Cl����SO42��
C���ں��д��� Fe3������Һ�У�NH4+��Na����Cl����SCN��
D��0.1 mol��L-1 CuSO4 ��Һ��H����K����NO3����Br-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ������У��һ��ѧ����ĩ������ѧ�Ծ��������棩 ���ͣ�ѡ����
���������ʳ�û����ͻ�����ˮ���㽫�������к�����ѷ����������� �� ��
A�����ˡ��� ��B������ ����C����Һ�� ����D����ȡ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ��ѧ�����п��Ը�һ��ѧ�Ծ��������棩 ���ͣ�ѡ����
���й����������������ȷ����
A���ܺ�ǿ����Һ��Ӧ����������Ǽ���������
B�����ܸ��Ӧ��������һ���ܺ��ᷴӦ
C������������һ���Ǽ���������
D�����������ﲻһ��������ˮ��Ӧ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ��ѧ�����п��Ը�һ��ѧ�Ծ��������棩 ���ͣ�ѡ����
���з�Ӧ������������ԭ��Ӧ�������ڻ��Ϸ�Ӧ�ĵ���
A��2Fe��3Cl2 2FeCl3 B��Fe2O3��3CO
2FeCl3 B��Fe2O3��3CO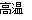 2Fe��3CO2
2Fe��3CO2
C��CaO��CO2 =CaCO3 D��H2SO4��2NaOH = Na2SO4��2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ�����н�ѧЭ�����һ��ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
��NA��ʾ�����ӵ�������ֵ������˵���������ǣ� ��
A���ڱ�״����22��4L H2�к�������ӵĸ���Ϊ2NA
B��24g Mg��ΪMg2+ʱʧȥ�ĵ�����Ϊ2NA
C��32g O2�к�����ԭ�ӵĸ���Ϊ2NA
D��1L 1mol/L NaCl��Һ�к��������ӵĸ���ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ̩���н�������һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����ᴿ����ѧ��ѧ����Ҫʵ��֮һ�����з�����ᴿ���ʵķ�����ȷ����
A��������ķ�����ȡ����ˮ
B���ù��˵ķ�����ȥNaCl��Һ�к��е�����Na2SO4
C�����ܽ⡢���˵ķ����ᴿ��������BaSO4��BaCO3
D���ü��ȡ������ķ������Գ�ȥNaCl�е�CaCl2��MgCl2������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com