
| 组分 | CO | CO2 | H2 |
| 体积分数 | 20% | 5% | 75% |
分析 (1)电解饱和食盐水是生产H2的方法之一,溶液质量减轻就是氯化氢的质量,所以n(H2)=$\frac{n(HCl)}{2}$=$\frac{\frac{0.365g}{36.5g/mol}}{2}$=0.005mol,根据V=nVm,计算体积;
(2)由反应方程式:2CH4$\stackrel{高温}{→}$3H2+C2H2,生成0.27m3氢气,则分解甲烷的物质的量为:$\frac{0.27×2}{3}$=0.18m3;
(3)设出反应产物的总体积及甲烷、乙烷的总体积,根据碳元素、氧元素、氢元素守恒分别列式计算,再根据相同条件下气体的体积之比等于其物质的量之比计算出原混合气体中甲烷与乙烷的物质的量之比;
(4)CH4的体积分数为0.112%,所以CH4的体积为:2000m3×0.112%=2.24m3,则反应后混合气体的体积为:$\frac{2.24{m}^{3}}{2.8%}$=80m3,所以气体体积减少量为:2000m3-80m3=1920m3,则氨气的物质的量为:$\frac{1920×1{0}^{3}L}{22.4L/mol}$×$\frac{1}{2}$=4.28×104mol,所以质量为:4.28×104mol×17g/mol=0.728t,由此解答.
解答 解:(1)电解饱和食盐水是生产H2的方法之一,溶液质量减轻就是氯化氢的质量,所以n(H2)=$\frac{n(HCl)}{2}$=$\frac{\frac{0.365g}{36.5g/mol}}{2}$=0.005mol,所以V=nVm═0.005mol×22.4L/mol=112ml,故答案为:112;
(2)由反应方程式:2CH4$\stackrel{高温}{→}$3H2+C2H2,生成0.27m3氢气,则分解甲烷的物质的量为:$\frac{0.27×2}{3}$=0.18m3,甲烷的裂解率为$\frac{0.18{m}^{3}}{1{m}^{3}}×100%$=18%,故答案为:18;
(3)设反应后气体总体积为V,甲烷的体积为x、乙烷的体积为y,
则含有CO体积而为0.2V,二氧化碳为0.05V,氢气为0.75V,
根据碳元素守恒可得:①x+2y=0.2V+0.05V=0.25V,
根据氧元素守恒可知,参加反应的水的物质的量为:0.2V+0.05V×2=0.3V,根据H元素守恒,水分子中H生成氢气体积为0.3V,则甲烷和乙烷分子中含有氢元素生成的氢气体积为:0.75V-0.3V=0.45V,即:②$\frac{1}{2}$(4x+6y)=0.45V,
联立①②解得:x=0.15V、y=0.05V,
相同条件下气体体积之比等于其物质的量之比,
所以原混合气体中甲烷与乙烷的物质的量之比为:0.15V:0.05V=3:1,
答:原混合气体中甲烷与乙烷的物质的量之比3:1;
(4)CH4的体积分数为0.112%,所以CH4的体积为:2000m3×0.112%=2.24m3,则反应后混合气体的体积为:$\frac{2.24{m}^{3}}{2.8%}$=80m3,所以气体体积减少量为:2000m3-80m3=1920m3,则氨气的物质的量为:$\frac{1920×1{0}^{3}L}{22.4L/mol}$×$\frac{1}{2}$=4.28×104mol,所以质量为:4.28×104mol×17g/mol=0.728t,答:分离出液氨为0.73t.
点评 本题考查了混合物反应的计算,题目难度中等,根据氧元素守恒计算出甲烷和乙烷分子中氢元素的量为解答关键,注意明确质量守恒定律在化学计算中的应用,试题侧重考查学生的分析、理解能力及化学计算能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
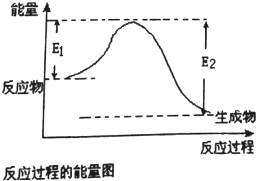 已知E1=2218kJ•mol-1、E2=2752kJ•mol-1,按要求回答问题:
已知E1=2218kJ•mol-1、E2=2752kJ•mol-1,按要求回答问题: ,已知断裂1mol化学键所需的能量(kJ):N≡N为942、O=O为500、N-N为154、O-H为460,则断裂1mol N-H键所需的能量(kJ)是391kJ.
,已知断裂1mol化学键所需的能量(kJ):N≡N为942、O=O为500、N-N为154、O-H为460,则断裂1mol N-H键所需的能量(kJ)是391kJ.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 红磷在氯气中反应,1mol红磷失去的电子数一定为5NA | |
| B. | 标准状况下22.4L C3H8中含中子数为18NA | |
| C. | 1L 1mol/L的葡萄糖溶液中,含有的分子数为NA个 | |
| D. | 常温下78 g过氧化钠和122 g水混合,所得溶液质量分数为40% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ②③④ | C. | ①②③④ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
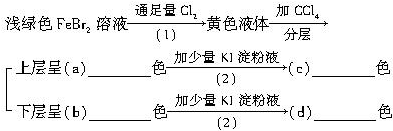
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶质的质量分数为ω=$\frac{a}{{V}_{ρ}-a}$×100% | |
| B. | 溶质的物质的量浓度c=$\frac{1000a}{17V}$mol•L-1 | |
| C. | 溶液中c(OH-)=$\frac{1000b}{V}$mol•L-1+c(H+) | |
| D. | 上述溶液中再加入VmL水后,所得溶液的质量分数大于0.5ω |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 溶液与胶体属于包含关系 | |
| B. | 化合物与氧化物属于包含关系 | |
| C. | 电解质与化合物属于交叉关系 | |
| D. | 氧化还原反应与化合反应属于并列关系 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠久置于空气中,先变暗,再变白,又“出汗”,最后变成白色固体 | |
| B. | 由海水制备金属镁和游离态的溴 | |
| C. | 工业上用石灰石、石英、纯碱制玻璃 | |
| D. | 高温下用二氧化硅和碳反应制备粗硅 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com