
| A. | 聚氯乙烯的结构简式为: | B. | 乙醇的官能团的电子式为: | ||
| C. | S2-的结构示意图为: | D. | 乙酸的实验式为C2H4O2 |
分析 A.聚氯乙烯为氯乙烯通过加聚反应生成的,为高分子化合物;
B.乙醇的官能团是羟基,羟基不带电;
C.S为16号元素,S2-的质子数为16,核外电子数为18,各层电子数分别为2、8、8;
D.乙酸的实验式:CH2O.
解答 解:A.聚氯乙烯为氯乙烯通过加聚反应生成的,聚氯乙烯的结构简式为: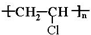 ,故A正确;
,故A正确;
B.乙醇的官能团是羟基,羟基不带电,电子式为 ,故B错误;
,故B错误;
C.S为16号元素,S2-的质子数为16,核外电子数为18,各层电子数分别为2、8、8,硫离子结构示意图为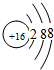 ,故C错误;
,故C错误;
D.乙酸的实验式是:CH2O,C2H4O2属于乙酸的化学式,故D错误;
故选A.
点评 本题考查了常见化学用语的表示方法,题目难度不大,涉及电子式、原子结构示意图、分子式和结构简式等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的规范答题能力.


科目:高中化学 来源: 题型:解答题
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
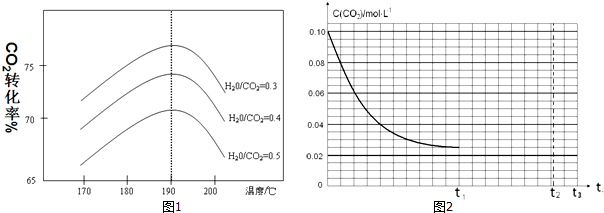
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 400mL10 mol•L-1的浓盐酸与足量的MnO2反应 | |
| B. | 2molCu与200g98%的浓硫酸反应 | |
| C. | 65gZn与足量的硝酸反应 | |
| D. | H2O(g)和CO2混合气体2mol与足量的Na2O反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2具有氧化性,可用于漂白纸浆 | |
| B. | 医用消毒酒精中乙醇的浓度为95% | |
| C. | 用灼烧的方法可以区分蚕丝和人造纤维 | |
| D. | 硅胶作袋装食品的干燥剂时发生了化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 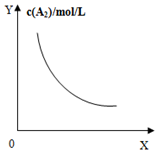 对于反应:A2(g)+3B2(g)?2AB2(g),图①中的横轴x可以表示压强 | |
| B. | 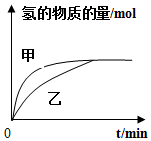 如图表示其他条件相同时,甲、乙两份等质量锌粉分别与足量稀硫酸反应,甲中加入少量铜粉 | |
| C. | 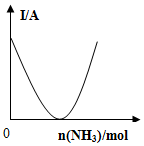 如图可表示乙酸溶液中通入氨气至过量时溶液导电性的变化 | |
| D. | 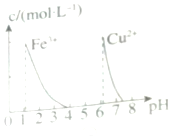 据图,若除去0.1mol•L-1CuSO4溶液中的Fe3+,可向溶液中加入适量NaOH至pH约为7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径大小顺序:r(W)>r(Z)>r(Y)>r(X) | |
| B. | 沸点:XW2>Y2W | |
| C. | 最高价氧化物对应的水化物的酸性:X>Z | |
| D. | 简单氢化物的热稳定性:Z<W |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通人H2S,有黄色沉淀 | |
| B. | 加入铜粉,溶液变为蓝色 | |
| C. | 加人锌粉,溶液棕黄色逐渐消失 | |
| D. | 滴加NaHCO3溶液,有气体和红棕色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
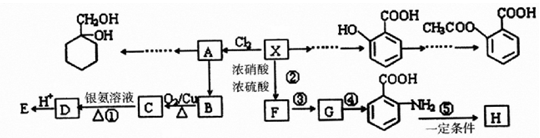
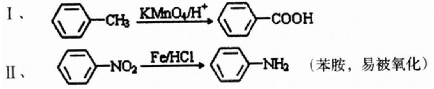
 ;
;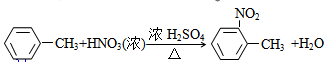 ;
;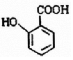 有多种同分异构体,写出符合下列条件的所有结构简式:
有多种同分异构体,写出符合下列条件的所有结构简式: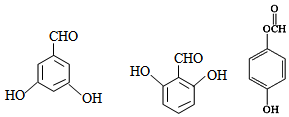 ;
;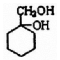 的合成路线(无机试剂任选)
的合成路线(无机试剂任选)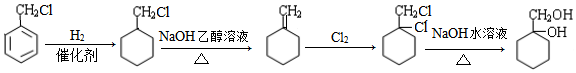 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com