
0.2mol有机物和0.4mol O2在密闭容器中燃烧后的产物为CO2、CO和H20(气),产物通过浓硫酸,浓硫酸质量增加10.8g;再通过灼热CuO,充分反应后,CuO质量减轻3.2g;最后气体再通过碱石灰被完全吸收,碱石灰质量增加17.6g.
(1)试推断该有机物的分子式.
(2)若0.2mol该有机物恰好与9.2g金属钠完全反应,试确定该有机物的结构简式并命名.
考点: 有机物实验式和分子式的确定.
专题: 烃及其衍生物的燃烧规律.
分析: (1)浓硫酸增重10.8g为反应生成的水的质量,通过灼热氧化铜,由于发生反应CuO+CO Cu+CO2,固体质量减轻了3.2g,结合方程式利用差量法可计算CO的物质的量,通过碱石灰时,碱石灰的质量增加了17.6g可计算总CO2的物质的量,减去CO与CuO反应生成的CO2的质量为有机物燃烧生成CO2的质量,根据元素守恒计算有机物中含有C、H、O的物质的量,进而求得化学式;
Cu+CO2,固体质量减轻了3.2g,结合方程式利用差量法可计算CO的物质的量,通过碱石灰时,碱石灰的质量增加了17.6g可计算总CO2的物质的量,减去CO与CuO反应生成的CO2的质量为有机物燃烧生成CO2的质量,根据元素守恒计算有机物中含有C、H、O的物质的量,进而求得化学式;
(2)结合分子式、与钠反应生成氢气的体积,判断分子中官能团,据此书写结构简式并命名.
解答: 解:(1)有机物燃烧生成水10.8g,物质的量为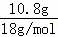 =0.6mol,
=0.6mol,
设有机物燃烧生成的CO为x,则:
CuO+CO Cu+CO2,固体减少△m
Cu+CO2,固体减少△m
28g 16g
x 3.2g
所以x=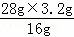 =5.6g,CO的物质的量为
=5.6g,CO的物质的量为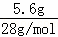 =0.2mol.
=0.2mol.
根据碳元素守恒可知CO与CuO反应生成的CO2的物质的量为0.2mol,质量为0.2mol×44g/mol=8.8g.
有机物燃烧生成的CO2的质量为17.6g﹣8.8g=8.8g,物质的量为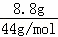 =0.2mol,
=0.2mol,
根据碳元素守恒可知,1mol有机物含有碳原子物质的量为2mol,
根据氢元素守恒可知,1mol有机物含有氢原子物质的量为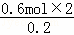 =6mol
=6mol
根据氧元素守恒可知,1mol有机物含有氧原子物质的量为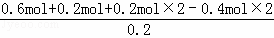 =2mol.
=2mol.
所以有机物的分子式为C2H6O2,
答:有机物的分子式为C2H6O2;
(2)9.2g金属钠的物质的量为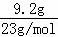 =0.4mol,与0.2mol该有机物恰好完全反应,故该有机物分子中含有2个羟基,该有机物的结构简式为HOCH2CH2OH,名称为乙二醇,
=0.4mol,与0.2mol该有机物恰好完全反应,故该有机物分子中含有2个羟基,该有机物的结构简式为HOCH2CH2OH,名称为乙二醇,
答:该有机物的结构简式为HOCH2﹣CH2OH,名称为乙二醇.
点评: 本题考查利用燃烧法确定有机物分子式、有机物结构的判断、官能团的性质等,题目难度中等,注意掌握原子守恒判断有机物的分子式方法.


科目:高中化学 来源: 题型:
一定温度下,反应X(g)+3Y(g)⇌2Z(g)达到化学平衡状态的标志是( )
|
| A. | X、Y、Z的分子数比为1:3:2 |
|
| B. | 单位时间生成amolX,同时生成3a molY |
|
| C. | X、Y、Z的浓度相等 |
|
| D. | 3v正(X)=v逆(Y) |
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下氨气和氧化铜可以发生如下反应:2NH3+3CuO 3Cu+N2+3H2O,下列对此反应的分析中合理的是()
3Cu+N2+3H2O,下列对此反应的分析中合理的是()
A. 该反应属于置换反应
B. CuO是氧化剂
C. 反应体现了金属铜的还原性
D. 每生成1molH2O就伴随着1mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
柠橡稀是一种食用香料,其结构为; 有关柠檬烯的分析正确的是()
有关柠檬烯的分析正确的是()
A. 柠檬烯的一氯代物有9种
B. 柠檬烯和丁基苯( )互为同分异构体
)互为同分异构体
C. 柠檬烯的分子中所有的碳原子可能在同一个平面上
D. 一定条件下,柠檬烯可以发生加成、取代、氧化等反应
查看答案和解析>>
科目:高中化学 来源: 题型:
A~G是几种烃的分子球棍模型(如图)

据此回答下列问题:
(1)常温下含碳量最高的气态烃是 (填对应字母).
(2)能够发生加成反应的烃有(填数字) 种.
(3)一卤代物种类最多的是(填对应字母) .
(4)写出实验室制取C的化学方程式 .
(5)写出F发生溴代反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
在下图点滴板上进行四个溶液间反应的小实验,其对应反应的离子方程式书写正确的是 ( )。
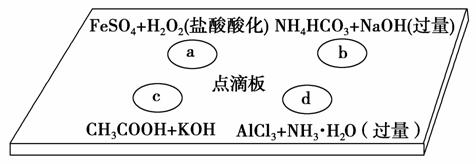
A.a反应:Fe2++2H++H2O2===Fe3++2H2O
B.b反应:HCO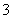 +OH-===CO
+OH-===CO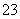 +H2O
+H2O
C.c反应:H++OH-===H2O
D.d反应:Al3++3NH3·H2O===Al(OH)3↓+3NH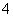
查看答案和解析>>
科目:高中化学 来源: 题型:
离子反应是中学化学中重要的反应类型。回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在有________(填序号)。
①单质 ②氧化物 ③电解质 ④盐 ⑤化合物
(2)可用图示的方法表示不同反应类型之间的关系。如分解反应和氧化还原反应可表示为下图。请在下面的方框中画出离子反应、置换反应和氧化还原反应三者之间的关系。
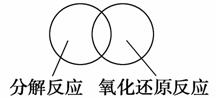
(3)离子方程式是重要的化学用语。下列是有关离子方程式的一些错误观点,请在下列表格中用相应的“离子方程式”否定这些观点。
| ①所有的离子方程式均可以表示一类反应 | |
| ②酸碱中和反应均可表示为H++OH-===H2O | |
| ③离子方程式中凡是难溶性酸、碱、盐均要标“↓”符号 |
(4)试列举出三种不同类别的物质(酸、碱、盐)之间的反应,它们对应的离子方程式都可用“Ba2++SO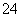 ===BaSO4↓”来表示,请写出有关反应的化学方程式(3个):
===BaSO4↓”来表示,请写出有关反应的化学方程式(3个):
①_______________________________________________________________;
②_______________________________________________________________;
③_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
有关合金的性质叙述不正确的是 ( )。
A.合金的熔点比它的各成分金属的熔点低
B.合金一定是金属熔合而成的
C.合金的硬度和强度一般比纯金属高
D.硬铝、黄铜、钢均为合金
查看答案和解析>>
科目:高中化学 来源: 题型:
下列图示与对应的叙述相符的是
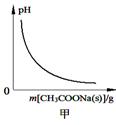
A.图甲表示向CH3COOH溶液中逐步加入CH3COONa固体后,溶液pH的变化
B.图乙表示向CH3COOH溶液中加水时溶液的导电性变化,则CH3COOH溶液的pH:a>b
C.图丙表示催化剂能改变化学反应的焓变
D.图丁表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:
2NO2(g)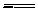 N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com