
| ��Ӧʱ��/min | n��MgSO4��/mol | n��CO��/mol | n��SO2��/mol |
| 0 | 2.0 | 2.0 | 0 |
| 2 | 0.8 | ||
| 4 | 1.2 | ||
| 6 | 1.2 | 2.8 |
| A�� | 0��2 min�ڵ�ƽ������Ϊ�� ��CO��=0.6 mol/��L•min�� | |
| B�� | 4 min��ƽ���ƶ���ԭ��������������м�����2.0 mol��SO2 | |
| C�� | �������¶ȣ���Ӧ��ƽ�ⳣ����Ϊ1.0��������ӦΪ���ȷ�Ӧ | |
| D�� | �����������䣬����ʼʱ������MgSO4��CO��Ϊ1.0 mol����ƽ��ʱn��SO2��=0.6 mol |
���� A���ɱ���ʱ���֪��0��2min��CO�����ʵ����仯��Ϊ2mol-0.8mol=1.2mol���ɷ���ʽ��֪SO2�����ʵ����仯��ҲΪ1.2mol������v=$\frac{\frac{��n}{V}}{��t}$����v��SO2����
B���ɱ������ݽ�Ϸ���ʽ��֪��0��2min��CO��CO2��SO2�����ʵ����仯��Ϊ2mol-0.8mol=1.2mol��4��6minʱ���仯��0.4mol���ݴ˷�����
C��������¶�ʱ��Ӧƽ�ⳣ�������������¶�ƽ�ⳣ���ı仯�ж�ƽ���ƶ����ݴ˽��
D�����������������䣬��ʼʱ�������г���1.00mol MgSO4��1.00molCO����ЧΪԭƽ���������һ��������ѹǿ��ƽ�����������ƶ����ݴ˷������
��� �⣺A���ɱ���ʱ���֪��0��2min��CO�����ʵ����仯��Ϊ2mol-0.8mol=1.2mol����v��CO��=$\frac{\frac{1.2mol}{2L}}{2min}$=0.3 mol•L-1•min-1����A����
B���ɱ������ݽ�Ϸ���ʽ��֪��0��2min��CO��CO2��SO2�����ʵ����仯��Ϊ2mol-0.8mol=1.2mol��4��6minʱ���仯��0.4mol������ƽ���ƶ���ԭ��������������м�����2.0 mol��SO2����B��ȷ��
C���ɱ���ʱ���֪��MgSO4��s��+CO��g��$\frac{\underline{\;��ȼ\;}}{\;}$MgO��s��+CO2��g��+SO2��g��
��ʼ��mol����2 0 0
�仯��mol����1.2 1.2 1.2
ƽ�⣨mol����0.8 1.2 1.2
�ʸ��¶���ƽ�ⳣ��k=$\frac{\frac{1.2}{2}��\frac{1.2}{2}}{\frac{0.8}{2}}$=0.9���������¶ȣ���Ӧ��ƽ�ⳣ����Ϊl��00����ƽ��������Ӧ�����ƶ�����������ӦΪ���ȷ�Ӧ����C����
D�����������������䣬��ʼʱ�������г���1.00mol MgSO4��1.00molCO����ЧΪԭƽ���������һ��������ѹǿ��ƽ�����������ƶ����ʵ���ƽ��ʱn��CO2����0.60mol����D����
��ѡB��
���� ���⿼�鷴Ӧ���ʼ��㡢Ӱ�컯ѧƽ�����ء���ѧƽ�ⳣ���ȣ��Ѷ��еȣ�ע�����֪ʶ�Ļ��ۣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

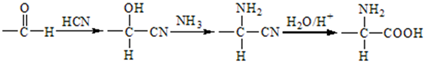
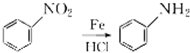
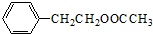 +HNO3��Ũ��$��_{��}^{Ũ����}$
+HNO3��Ũ��$��_{��}^{Ũ����}$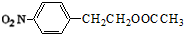 +H2O��
+H2O��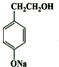 ��
��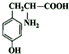 ��
��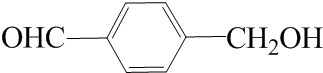 ��д�ṹ��ʽ����
��д�ṹ��ʽ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��˿ȼ�� | B�� | ������ȼ | C�� | ȼ�ű��� | D�� | �ɱ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
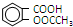 ����������Ӧ����㷺�Ľ��ȡ���ʹҩ���������������ǻ���������ҵ����ˮ���ᣨ
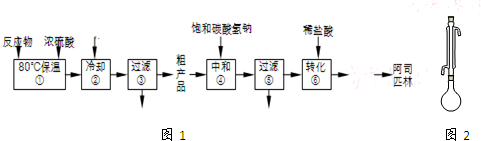
����������Ӧ����㷺�Ľ��ȡ���ʹҩ���������������ǻ���������ҵ����ˮ���ᣨ 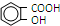 ����������[��CH3CO��2O]Ϊ��Ҫԭ�Ϻϳɰ�˾ƥ�֣��ֲ�Ʒ����Ҫ�ĸ�������ˮ����������һ���ᴿ����Ӧԭ������������������£�
����������[��CH3CO��2O]Ϊ��Ҫԭ�Ϻϳɰ�˾ƥ�֣��ֲ�Ʒ����Ҫ�ĸ�������ˮ����������һ���ᴿ����Ӧԭ������������������£� +��CH3CO��2O$?_{��}^{Ũ����}$
+��CH3CO��2O$?_{��}^{Ũ����}$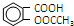 +CH3COOH
+CH3COOH| ���� | ������״̬ | ˮ���ܽ��� |
| ������ | Һ | ��ˮ��Ӧ |
| ��˾ƥ�� | �� | ��ˮ���ܣ���ˮ������ |
| ˮ�������� | �� | ���� |
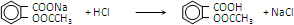 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
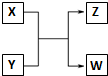 ��֪X��Y��Z��W�ֱ����ɶ�����Ԫ����ɵ�������������֮������ͼ��ʾ��ת����ϵ����X��һ�ֺ���18���ӵ�����Z��һ�ֺ���10���ӵ�������ش��������⣺
��֪X��Y��Z��W�ֱ����ɶ�����Ԫ����ɵ�������������֮������ͼ��ʾ��ת����ϵ����X��һ�ֺ���18���ӵ�����Z��һ�ֺ���10���ӵ�������ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
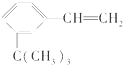 ���������ʣ�
���������ʣ�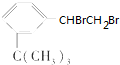 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ֻ�Т٢� | B�� | ֻ�Тڢ� | C�� | ֻ�Тۢ� | D�� | �٢ڢۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
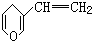 ��Ϊͬ���칹�壬������FeCl3��Һ��Ϻ���ɫ�Ͳ���ɫ������ֱ��У�������
��Ϊͬ���칹�壬������FeCl3��Һ��Ϻ���ɫ�Ͳ���ɫ������ֱ��У�������| A�� | 2�ֺ�1�� | B�� | 2�ֺ�3�� | C�� | 3�ֺ�2�� | D�� | 3�ֺ�1�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2CH3CH2OH+${\;}_{\;}^{18}$O2$��_{��}^{Cu}$2CH3CH${\;}_{\;}^{18}$O+2H2O | |
| B�� | CH3COOC2H5+H2${\;}_{\;}^{18}$O$��_{��}^{H+}$CH3COOH+CH3CH2${\;}_{\;}^{18}$OH | |
| C�� | 2KMnO4+5H2${\;}_{\;}^{18}$O2+3H2SO4=K2SO4+2KMnSO4+5${\;}_{\;}^{18}$O2��+8H2O | |
| D�� | 2Na2${\;}_{\;}^{18}$O2+2H2O=4Na${\;}_{\;}^{18}$OH+O2�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com