
| 编号 | 改变的条件 | 生成的SO3的速率 |
| ① | 降低温度 | 减小 |
| ② | 升高温度 | 增大 |
| ③ | 增大O2的浓度 | 增大 |
| ④ | 恒容下充入Ne | 不变 |
| ⑤ | 压缩体积 | 增大 |
| ⑥ | 使用催化剂 | 增大 |
科目:高中化学 来源: 题型:选择题
| A. | HCl的电子式 | B. | Cl-的结构示意  | ||
| C. | CO2的电子式  | D. | 质量数为37的氯原子 ${\;}_{37}^{17}$Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题


 ),莽草酸分子中有3个手性碳原子.
),莽草酸分子中有3个手性碳原子.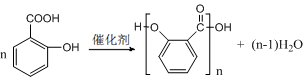 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| Zn2+ | Mn2+ | Fe2+ | Fe3+ | Al3+ | |
| pH | 8.0 | 10.1 | 9.0 | 3.2 | 4.7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com