
有A、B两种烃,所含碳元素的质量分数相同,关于A和B叙述中正确的是( )
A.二者不可能是同系物
B.二者一定是同分异构体
C.二者最简式相同
D.将等质量的A和B分别燃烧生成CO2的质量一定相等
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
正误判断,正确的划“√”,错误的划“×”
(1)臭氧变成氧气是物理变化( )
(2)将蓝色的硫酸铜晶体放入浓硫酸中发生物理变化( )
(3)冰变成水是物理变化( )
(4)通电发光是物理变化( )
(5)煤的“气化”、煤的“液化”、煤的“干馏”都是物理变化( )
(6)分馏、蒸馏、蒸发、萃取、分液、过滤都属于物理变化( )
(7)加热I2,固体从试管底部跑到上部属于物理变化( )
(8)加热NH4Cl晶体,固体从试管底部跑到上部属于物理变化( )
(9)向蛋白质溶液中滴加CuSO4溶液产生沉淀属于化学变化( )
(10)向蛋白质溶液中滴加Na2SO4溶液产生沉淀属于化学变化( )
(11)紫色石蕊溶液中加入活性炭褪色是化学变化( )
(12)用铂丝蘸取NaCl溶液进行焰色反应是化学变化( )
(13)化学变化中一定存在化学键的断裂和形成,有化学键断裂或形成的变化也一定是化学变化( )
(14)金属熔化、从NaCl溶液中结晶析出NaCl晶体、从浓盐酸中挥发出HCl气体均属于物理变化( )
(15)核裂变、核聚变均有新物质生成,均属于化学变化( )
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与人类生产,生活密切相关。下列有关说法不正确的是
A.“海水淡化”可以解决“淡水供应危机”,向海水中加入净水剂明矾可以使海水淡化
B.福尔马林可浸制标本,利用了其使蛋白质变性的性质
C.医用酒精使用淀粉类植物发酵经蒸馏制成,浓度通常为75%
D.绚丽缤纷的烟花中添加了含钾,钙,钠,铜等金属元素化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
高锰酸钾(KMnO4)和过氧化氢(H2O2)是两种典型的氧化剂。
(1)H2O2的结构式为________________。
(2)下列物质中能使酸性KMnO4溶液褪色的是________(填选项字母)。
A.臭碱(Na2S) B.小苏打(NaHCO3)
C.水玻璃(Na2SiO3) D.酒精(C2H5OH)
(3)高锰酸钾、双氧水、活性炭常用于饮用水的处理,但三者联合作用时必须有先后顺序。①在稀硫酸中,KMnO4和H2O2能发生氧化还原反应:
氧化反应:H2O2-2e-―→2H++O2↑
还原反应:MnO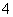 +5e-+8H+―→Mn2++4H2O
+5e-+8H+―→Mn2++4H2O
写出该氧化还原反应的离子方程式_____________________________。
②在处理饮用水时,活性炭应在高锰酸钾反应结束后投加,否则会发生反应:KMnO4+C+H2O―→MnO2+X+K2CO3(未配平),其中X的化学式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化合物分子中,在核磁共振氢谱图中能给出二种信号的是( )
A.CH3CH2CH3 B.CH3COCH2CH3 C.CH3CH2OH D.CH3OCH3
查看答案和解析>>
科目:高中化学 来源: 题型:
通过粮食发酵可获得某含氧有机化合物X,其相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13.0% .
(1)X的电子式是 ;
(2)X与金属钠反应放出氢气,反应的化学方程式是 (有机物用结构简式表达);
(3)X与空气中的氧气在铜或银催化下反应生成Y,Y的结构简式是 ;
Y能发生银镜反应,Y与银氨溶液的反应的化学方程式是:
查看答案和解析>>
科目:高中化学 来源: 题型:
对于常温下pH为1的硝酸溶液,下列叙述正确的是( )
A.该溶液1 mL稀释至100 mL后,pH等于3
B.向该溶液中加入pH为13的氢氧化钡溶液恰好完全中和
C.该溶液中硝酸电离出的c(H+)与水电离出的c(H+)之比值为10-12
D.该溶液中水电离出的c(H+)是pH为3的硝酸中水电离出的c(H+)的100倍
查看答案和解析>>
科目:高中化学 来源: 题型:
 在5L的密闭容器中进行下述反应4NH3(g)+5O2(g)
在5L的密闭容器中进行下述反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g) 30S内,NO增加了0.3mol,则在30S内,该反应的平均反应速率正确的是( )
4NO(g)+6H2O(g) 30S内,NO增加了0.3mol,则在30S内,该反应的平均反应速率正确的是( )
A.V(O2 )=0.01mol·L-1·s-1 B. V(NO )=0.08mol·L-1·s-1
C. V(H2O)=0.01mol·L-1·s-1 D. V(NH3)=0.002mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)对于下列反应:2SO2(g) + O2(g) 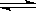 2SO3(g) , 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,用SO2浓度变化来表示的化学反应速率为____________,用O2浓度变化来表示的反应速率为_____________。如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L·min),那么2min时SO2的浓度为 。
2SO3(g) , 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,用SO2浓度变化来表示的化学反应速率为____________,用O2浓度变化来表示的反应速率为_____________。如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L·min),那么2min时SO2的浓度为 。
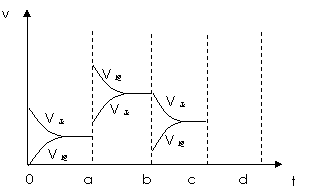
(2)下图表示在密闭容器中反应:2SO2+O2 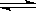 2SO3 △H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a~b过程中改变的条件可能是 ;b~c过程中改变的条件可能是 ; 若增大压强时,反应速度变化情况画在c~d处。
2SO3 △H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a~b过程中改变的条件可能是 ;b~c过程中改变的条件可能是 ; 若增大压强时,反应速度变化情况画在c~d处。
 |
(3)以上反应达平衡后,
若此时只将容器的体积扩大为原来的2倍,达新平衡时,容器内温度将降低(容器不与外界进行热交换),则该反应正向为 反应(填“放热”或“吸热”);达新平衡时,容器内混合气体的平均相对分子质量
比原平衡时 (填“增大”、“减小”或“相等”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com