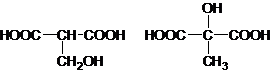请按要求回答下列问题:
(1)硅在无机非金属材料中一直扮演着重要角色,被誉为无机非金属材料的主角.
①下列物品用到硅单质的是______;
A.玻璃制品;B.石英钟表;C.计算机芯片;D.光导纤维;E.太阳能电池
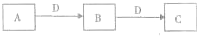
②硅酸盐组成复杂,往往用氧化物的形式表示,某硅酸盐其主要化学成分为Ca2Mg5Si8O22(OH)2.把它写成氧化物的形式为:______;
(2)Cl2和SO2都具有漂白性,但将这两种气体按体积比1:1通入水中得到的溶液却几乎没有漂白性,写出Cl2和SO2 1:1通入水中发生的离子反应方程式:______;
(3)写出二氧化硫与双氧水反应的化学方程式,并标出电子转移方向和数目:______.
解:(1)①A.玻璃制品的成分二氧化硅,不是单质硅,故A错误;
B.石英钟表的构成材料为二氧化硅,不是单质硅,故B错误;
C.计算机芯片的主要成分为单质硅,故C正确;
D.光导纤维的主要成分为二氧化硅构,不是单质硅,故D错误;
E.太阳能电池的主要成分是硅单质,故E正确.
故答案为:C、E;
②硅酸盐改写成氧化物的形式为:活泼金属氧化物?较活泼金属氧化物?SiO2?H2O,同时要遵循原子守恒,故写成:2CaO?5MgO?8SiO
2?H
2O,
故答案为:2CaO?5MgO?8SiO
2?H
2O;
(2)氯气具有氧化性,二氧化硫具有还原性,二者1:1发生氧化还原反应生成硫酸和盐酸;反应离子方程式Cl
2+SO
2+2H
2O═2Cl
-+SO
42-+4H
+,
故答案为:Cl
2+SO
2+2H
2O═2Cl
-+SO
42-+4H
+;
(3)在二氧化硫与双氧水的反应中,化合价升高数=化合价降低数=转移电子数=2,电子转移情况为:
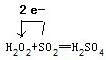
,故答案为:
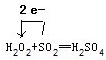
.
分析:(1)①硅位于金属和非金属分界线附近,常用作半导体材料,为无机非金属材料的主角,而二氧化硅具有熔点高、硬度大的特点,常用于制备耐高温材料和光导纤维;
②根据化学式改写成相应的氧化物的形式,按照活泼金属氧化物,较活泼金属氧化物,SiO
2.H
2O的顺序来书写,并要遵守原子守恒来分析解答;
(2)氯气具有氧化性,二氧化硫具有还原性,二者1:1发生氧化还原反应生成硫酸和盐酸;
(3)元素失去电子化合价升高,化合价升高数=化合价降低数=转移电子数.
点评:本题考查硅单质的用途、硅酸盐的表示方法,氧化还原反应电子的转移,难度不大,注意在氧化还原反应中化合价升高数=化合价降低数.

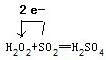 ,故答案为:
,故答案为: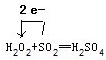 .
.