
| A. | 由同种元素组成的物质一定属于纯净物 | |
| B. | NaHCO3在水中电离:NaHCO3═Na++H++CO32- | |
| C. | 含金属元素的离子不一定都是阳离子 | |
| D. | 具有相同质子数的微粒都属于同种元素 |
分析 A.氧气与臭氧的混合物;
B.碳酸氢根离子为多元弱酸根离子,不能拆;
C.高锰酸根离子含有金属锰元素;
D.氢氧根离子含有9个质子,氟离子含有9个质子.
解答 解:A.氧气与臭氧组成的物质只含有1种元素,但是属于混合物,故A错误;
B.NaHCO3在水中电离,电离方程式:NaHCO3═Na++HCO3-,故B错误;
C.高锰酸根离子含有金属锰元素,但是高锰酸根离子是阴离子,故C正确;
D.具有相同质子数的微粒不一定都属于同种元素,如氢氧根离子与氟离子,具有相同质子数的原子为同种元素,故D错误;
故选:C.
点评 本题考查了纯净物概念、电解质电离方程式书写、同种元素的概念,题目难度不大,明确相关概念是解题关键.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
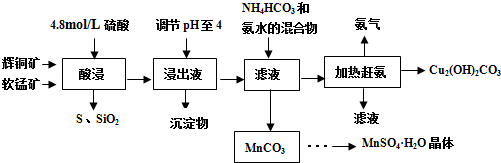
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶质物质的量浓度大于9.2mol/L | B. | 溶液体积为20mL | ||
| C. | 溶质质量分数为49% | D. | 溶质质量分数小于49% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 取KOH、Ba(OH)2、Ca(OH)2溶液分别与酚酞试液作用,观察溶液颜色 | |
| B. | 测定NaOH的溶解度,证明其易溶于水,并观察溶液的颜色 | |
| C. | 取NaCl溶液与酚酞试液作用,观察溶液颜色 | |
| D. | 向滴有酚酞的NaOH溶液中加入盐酸,观察溶液的颜色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将氢氧化钠固体放在滤纸上称量 | |
| B. | 用10mL量筒量取8.58mL蒸馏水 | |
| C. | 制取氯气时,用二氧化锰与浓盐酸在常温下反应,并用排水集气法收集 | |
| D. | 过滤时玻璃棒的末端应轻轻靠在三层的滤纸上 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
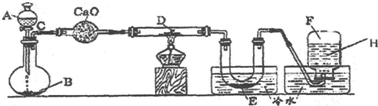
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com