
| A. | NH4HCO3溶液中加入足量的NaOH浓溶液:NH4++OH-═NH3↑+H2O | |
| B. | 向FeBr2溶液中滴加少量氯水:2Fe2++Cl2═2Fe3++2Cl- | |
| C. | 用电子式表示HCl的形成过程: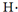 + +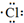 → →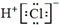 | |
| D. | 硫磺在空气中燃烧:2S+3O2$\frac{\underline{\;点燃\;}}{\;}$ 2SO3 |
分析 A.氢氧化钠足量,铵根离子、碳酸氢根离子都与氢氧根离子反应;
B.二价铁离子还原性强于溴离子,氯水少量,只氧化二价铁离子;
C.氯化氢为共价化合物;
D.不符合反应客观事实.
解答 解:A.NH4HCO3溶液加入足量NaOH溶液共热生成碳酸钠、氨气和水,则离子反应为HCO3-+NH4++2OH-═NH3↑+H2O+CO32-,故A错误;
B.向FeBr2溶液中滴加少量氯水,离子方程式:2Fe2++Cl2═2Fe3++2Cl-,故B正确;
C.HCl属于共价化合物,氢原子最外层电子与Cl最外层电子形成一对共用电子对,其形成过程可写为: ,故C错误;
,故C错误;
D.硫磺在空气中燃烧生成二氧化硫:S+O2$\frac{\underline{\;点燃\;}}{\;}$ SO2,故D错误;
故选:B.
点评 本题考查了离子方程式、化学方程式的书写,明确反应实质是解题关键,注意离子反应、化学反应遵循客观事实,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
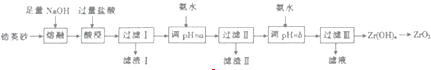
| 离子 | Fe3+ | AP+ | ZrO2+ |
| 开始沉淀pH | 1.9 | 3.3 | 6.2 |
| 完仝沉淀pH | 3.2 | 5.2 | 8.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烷和乙酸 | B. | 淀粉和纤维素 | ||
| C. | CH3CH2CH2CH3和CH3CH2CH3 | D. | 乙醇和二甲醚 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .其反应类型为消去反应.检验生成的乙烯要将气体先后通入氢氧化钠溶液、酸性高锰酸钾溶液或溴水中.(填试剂名称)
.其反应类型为消去反应.检验生成的乙烯要将气体先后通入氢氧化钠溶液、酸性高锰酸钾溶液或溴水中.(填试剂名称)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数:X<Y<Z<W | B. | 单质的熔点:W>Z | ||
| C. | 热稳定性:H2Y>HX | D. | 碱性:W(OH)2>ZOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | C | D | F | |||||
| 三 | B | E | G | R | ||||
| 四 | A | H |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯用途之一:可作为植物生长调节剂 | |
| B. | CH4与Cl2以体积比1:4混合,光照时可制得纯净的CCl4 | |
| C. | 苯能在一定条件下跟H2加成生成环己烷 | |
| D. | 工业上可用乙烯与水在一定条件下进行加成反应制取酒精 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O很稳定,是因为水分子之间存在氢键 | |
| B. | 由于F非金属性最强,HF的氢键键能最大,所以HF的熔、沸点最高 | |
| C. | 卤素单质从上到下熔沸点升高,是因为它们的组成结构相似,从上到下其摩尔质量增大,分子间的范德华力增大 | |
| D. | 氨气极易溶于水,与氢键没有关系 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
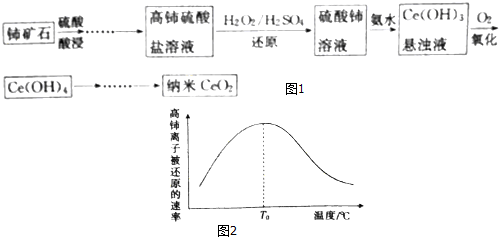
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com