
| A£® | ČČĪČ¶ØŠŌ£ŗPH3£¼NH3 | B£® | ½šŹōŠŌĒæČõ£ŗNa£¾Mg£¾Al | ||
| C£® | ĖįŠŌĒæČõ£ŗHF£¾HCl£¾HBr£¾HI | D£® | Ō×Ó°ė¾¶£ŗK£¾Si£¾Cl£¾F |
·ÖĪö A£®·Ē½šŹōŠŌŌ½Ē棬Ēā»ÆĪļŌ½ĪČ¶Ø£»
B£®Ķ¬ÖÜĘŚŌŖĖŲ“Ó×óµ½ÓŅ½šŹōŠŌÖš½„¼õČõ£»
C£®Ķ¬Ö÷×åŌŖĖŲµÄ·Ē½šŹōŠŌŌ½Ē棬¶ŌÓ¦Ēā»ÆĪļµÄĖįŠŌŌ½Čõ£»
D£®Ķ¬ÖÜĘŚŌŖĖŲ£¬ĖęŌ×ÓŠņŹżŌö“ó£¬Ō×Ó°ė¾¶¼õŠ”£»Ķ¬Ö÷×å×ŌÉĻ¶ųĻĀŌ×Ó°ė¾¶Ōö“ó£®
½ā“š ½ā£ŗA£®·Ē½šŹōŠŌN£¾P£¬·Ē½šŹōŠŌŌ½Ē棬Ēā»ÆĪļŌ½ĪČ¶Ø£¬¹ŹAÕżČ·£»
B£®Ķ¬ÖÜĘŚŌŖĖŲ“Ó×óµ½ÓŅ½šŹōŠŌÖš½„¼õČõ£¬Ōņ½šŹōŠŌNa£¾Mg£¾Al£¬¹ŹBÕżČ·£»
C£®·Ē½šŹōŠŌF£¾Cl£¾Br£¾I£¬Ķ¬Ö÷×åŌŖĖŲµÄ·Ē½šŹōŠŌŌ½Ē棬¶ŌÓ¦Ēā»ÆĪļµÄĖįŠŌŌ½Čõ£¬ŌņĖįŠŌĒæČõ£ŗHI£¾HBr£¾HCl£¾HF£¬¹ŹC“ķĪó£»
D£®Ķ¬ÖÜĘŚŌŖĖŲ£¬ĖęŌ×ÓŠņŹżŌö“ó£¬Ō×Ó°ė¾¶¼õŠ”£»Ķ¬Ö÷×å×ŌÉĻ¶ųĻĀŌ×Ó°ė¾¶Ōö“ó£¬ŌņŌ×Ó°ė¾¶K£¾Si£¾Cl£¾F£¬¹ŹDÕżČ·£®
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éŌŖĖŲÖÜĘŚ±ķŗĶÖÜĘŚĀɵÄ×ŪŗĻÓ¦ÓĆ£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕŌŖĖŲµÄĪ»ÖĆ”¢ŠŌÖŹ”¢ŌŖĖŲÖÜĘŚĀÉĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėÓ¦ÓĆÄÜĮ¦µÄ漲飬ĢāÄæÄŃ¶Č²»“ó£®


 æŖŠÄĮ·Ļ°æĪæĪĮ·Óėµ„ŌŖ¼ģ²āĻµĮŠ“š°ø
æŖŠÄĮ·Ļ°æĪæĪĮ·Óėµ„ŌŖ¼ģ²āĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½šøÕŹÆŗĶC60 | B£® | 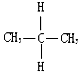 Óė Óė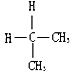 | ||
| C£® | 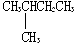 Óė Óė 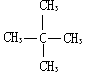 | D£® | CH3CH3ÓėCH3CH2CH2CH3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
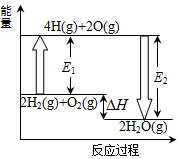 ŅŃÖŖ²šæŖ1molĒāĘųÖŠ»Æѧ¼üŠčŅŖĪüŹÕ436kJČČĮ棬²šæŖ1molŃõĘųÖŠµÄ»Æѧ¼üŠčŅŖĪüŹÕ496kJµÄČČĮ棬ŠĪ³É1molH-O¹²¼Ū¼ü·Å³ö463kJµÄČČĮ森·“Ó¦2H2£Øg£©+O2£Øg£©ØT2H2O£Øg£©µÄÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
ŅŃÖŖ²šæŖ1molĒāĘųÖŠ»Æѧ¼üŠčŅŖĪüŹÕ436kJČČĮ棬²šæŖ1molŃõĘųÖŠµÄ»Æѧ¼üŠčŅŖĪüŹÕ496kJµÄČČĮ棬ŠĪ³É1molH-O¹²¼Ū¼ü·Å³ö463kJµÄČČĮ森·“Ó¦2H2£Øg£©+O2£Øg£©ØT2H2O£Øg£©µÄÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | 2H£Øg£©”śH2£Øg£©”÷H£¾0 | B£® | Ķ¼ÖŠE1=932kJ | ||
| C£® | Ķ¼ÖŠE2=926 kJ | D£® | 2H2£Øg£©+O2£Øg£©ØT2H2O£Øg£©”÷H=-484 kJ•mol-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 ĮŖ°±N2H4£ØČŪµć£ŗ1.4”ę£¬·Šµć£ŗ113.5”ę£©ŹĒŅ»ÖÖĪŽÉ«µÄæÉČ¼ŅŗĢ壬æÉÓĆ×÷»š¼żŗĶČ¼ĮĻµē³ŲµÄČ¼ĮĻ£®½įŗĻĮŖ°±µÄ½į¹¹ÅŠ¶ĻĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
ĮŖ°±N2H4£ØČŪµć£ŗ1.4”ę£¬·Šµć£ŗ113.5”ę£©ŹĒŅ»ÖÖĪŽÉ«µÄæÉČ¼ŅŗĢ壬æÉÓĆ×÷»š¼żŗĶČ¼ĮĻµē³ŲµÄČ¼ĮĻ£®½įŗĻĮŖ°±µÄ½į¹¹ÅŠ¶ĻĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | ĮŖ°±µÄ¾§ĢåŹĒŌ×Ó¾§Ģå | |
| B£® | ĮŖ°±Ņ×ČÜÓŚĖ® | |
| C£® | 1 molĮŖ°±·Ö×ÓÖŠŗ¬ÓŠ5NAøö¦Ņ¼üŗĶNAøö¦Š¼ü | |
| D£® | ĮŖ°±·Ö×ÓŹĒ·Ē¼«ŠŌ·Ö×Ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
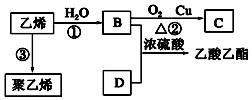 ŅŃÖŖŅŅĻ©ÄÜ·¢ÉśŅŌĻĀ×Ŗ»Æ£ŗ
ŅŃÖŖŅŅĻ©ÄÜ·¢ÉśŅŌĻĀ×Ŗ»Æ£ŗ £¬ĮŠ¾Ł¾ŪŅŅĻ©µÄŅ»ÖÖÓĆĶ¾ÖĘĖÜĮĻ£®
£¬ĮŠ¾Ł¾ŪŅŅĻ©µÄŅ»ÖÖÓĆĶ¾ÖĘĖÜĮĻ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2.24 L CH4ÖŠŗ¬Ģ¼Ō×ÓŹżÄæŹĒ0.1 NA | |
| B£® | 0.1 mol•L-1 NaNO3ČÜŅŗÖŠŗ¬Na+ŹżÄæŹĒ0.1 NA | |
| C£® | 1 mol Cl2Óė×ćĮæµÄĢśĶźČ«·“Ó¦Ź±µĆµ½µÄµē×ÓŹżÄæŹĒ2 NA | |
| D£® | ±ź×¼×“æöĻĀ£¬22.4 L±½ÖŠŗ¬·Ö×ÓŹżÄæŹĒNA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  | B£® |  | C£® |  | D£® |  |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½šøÕŹÆ£¾¾§Ģå¹č£¾¶žŃõ»Æ¹č£¾Ģ¼»Æ¹č | B£® | CI4£¾CBr4£¾CCl4£¾CF4 | ||
| C£® | NH3£¾H2O£¾N2£¾CO | D£® | HF£¾HCl£¾HBr£¾HI |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com