
【题目】下列分散系中,具有丁达尔效应的是( )
A. 碳酸钠溶液
B. 硝酸钾溶液
C. 蔗糖溶液
D. Fe(OH)3胶体
 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:高中化学 来源: 题型:
【题目】分子式为C5H7Cl的有机物,其结构不可能是( )
A.只含有1个双键的直链有机物
B.含2个双键的直链有机物
C.含1个双键的环状有机物
D.含一个三键的直链有机物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶液的酸碱性可用酸度(AG)表示AG=lg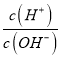 。室温下,某化学兴趣小组的同学用 0.01 mol·L-1的氢氧化钠溶液滴定20.00 mL 0.01 mol·L-1醋酸,滴定结果如下图所示,下列有关叙述中正确的是
。室温下,某化学兴趣小组的同学用 0.01 mol·L-1的氢氧化钠溶液滴定20.00 mL 0.01 mol·L-1醋酸,滴定结果如下图所示,下列有关叙述中正确的是
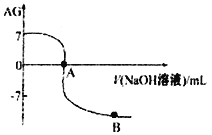
A. 水的电离程度A点小于B点
B. A点时加入的氢氧化钠溶液的体积恰好为20.00 mL
C. 室温0.01 mol·L-1醋酸溶液的电离平衡常数Ka=l0-5
D. 若B点时所加NaOH溶液的体积为40.00 mL,此时溶液中c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W为短周期主族元素,在周期表中的相对位置如图,下列说法正确的是( )

A. 若HmXOn为强酸,则X的氢化物溶于水一定显酸性(m、n均为正整数)
B. 若四种元素均为金属,则Z的最高价氧化物对应的水化物一定为强碱
C. 若四种元素均为非金属,则W的最高价氧化物对应的水化物一定为强酸
D. 若四种元素中只有一种为金属,则Z与Y两者的最高价氧化物对应的水化物能反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是
A. 如图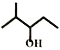 所示的有机物的名称为:2-甲基戊醇
所示的有机物的名称为:2-甲基戊醇
B. 乙烯能使酸性高锰酸钾溶液褪色,聚乙烯也能使酸性高锰酸钾褪色
C. 蛋白质能发生水解反应,水解生成的氨基酸能和酸反应,也能和碱反应
D. 分子式为C4H9Cl的氯代烃有4种,C4H10O的醇有4种,C4H8O的酸也有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学的实用性表现在它与人们的生活紧密联系。下列常用物质的主要化学成分溶于水后对水的电离有抑制作用的是
A. 明矾 B. 苏打 C. 84消毒液 D. 洁厕灵
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表中常见非金属元素形成的化合物与新能源和新环境问题密切相关。
(1)我国于2016年10月17日由长征号FY11运载火箭发射神舟十号飞船,其推力能量主要是压缩成液体燃料(CH3)2N-NH2和氧化剂N2O4,该燃料组燃烧后产生巨大能量,释放产物为无毒无害的气体。298K时,10g燃料完全燃烧释放的能量为425kJ,请写出该反应的热化学方程式
_____________。
(2)二氧化硫、氮氧化物以及可吸入颗粒物(PM2.5 等)这三项是雾霾主要组成。其中炭还原法处理氮氧化物是一种方法。T℃时反应C(s)+2NO(g)![]() N2(g) + CO2(g),反应始终从反应物投料开始,测定各时间点的物质浓度图像如下:
N2(g) + CO2(g),反应始终从反应物投料开始,测定各时间点的物质浓度图像如下:

① 第一次平衡前,CO2的平均反应速率v (CO2)=____________;
② 若反应在T℃进行,只改变起始反应物投料,某时刻测得C(NO)=4 mol/L, C(N2) =4mol/L,则此时V(正)_____V(逆)(填“>”、“<”或“=”) ;
③ 根据图像判断,40min时改变的条件可能是__________;
A.恒压条件下通入NO; B.升高温度; C.(恒容条件)通入NO; D.压缩体积;
E.恒压时加入活性炭; F.使用新型催化剂。
(3)新能源应用探索中,可以用下图装置于净化处理厕所排放废水中的尿素(H2NCONH2),同时产生电能。请写出负极电极反应式:_____________;

(4)工业上使用氨碱吸收SO2,然后使之转化成NH4HSO4,可作分析试剂使用,现用0.1mol/LKOH来滴定100mL0.1mol/L NH4HSO4,反应过程的滴定曲线如下图:
已知:常温时NH3·H2O的电离常数K=1.8×10-5,忽略溶液混合后体积变化,请根据图中给出的5个点的字母回答相关问题。

①滴定过程中以上5个点中,_________点水电离程度最小;
②滴定过程中Z点溶液中各离子浓度由大到小的排列顺序是_________;
③滴定过程中M点的pH大约是(填整数)___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚(![]() ),同时利用此装置的电能在铁上镀铜,下列说法错误的是
),同时利用此装置的电能在铁上镀铜,下列说法错误的是

A. 铁电极应与Y相连接
B. 反应过程中甲中右边区域溶液pH逐渐升高
C. A极的电极反应式为![]() +2e-+H+=Cl-+
+2e-+H+=Cl-+![]()
D. 当外电路中有0.2 mole-转移时,A极区增加的H+的个数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将汽车尾气中含有的CO利用不仅能有效利用资源.还能防治空气污染。工业上常用CO与H2在由Al、Zn、Cu等元索形成的催化剂作用下合成甲醇。
(1)图l是某同学画出CO分子中权原子的核外电子排布图。

请判断该排布图____(填“正确”或“错误”) ,理由是________ (若判断正确,该空不用回答)。
(2)写出两种与CO互为等电子体的离子________。
(3)往硫酸铜溶液中通入过量的NH3,可生成配离子[Cu(NH3 )4]2+,但NF3不易与Cu2+形成配离子,其原因是_________,在配离子[Cu(NH3 )4]2+中所含配位键是通过配体分子的_____给出孤电子对,____接受电子对形成。
(4)甲醇与乙烷的相对分子质量相近,故二者分子间的作用力(范德华力)相近,但是二者沸点的差距却很大,造成该差异的原因是______;在甲醇分子中碳原子轨道的杂化类型为_____。
(5)甲醛与新制Cu(OH)2悬浊液加热可得砖红色沉淀Cu2O,已知Cu2O晶胞的结构如图2所示。
①在该晶胞中,Cu+的配位数是_____。
②若该晶胞的边长为apm,则Cu2O的密度为_____g·cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com