
| A、②⑤⑥ | B、①④⑤ |
| C、①④⑦ | D、①④⑤⑦ |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| 实验 | 温度/℃ | 起始量/mol | 平衡量/mol | |||
| CO | H2O | CO2 | H2 | CO2 | ||
| 1 | 650 | 2.0 | 1.0 | 0 | 0 | 0.8 |
| 2 | 800 | 2.0 | 2.0 | 0 | 0 | 1.0 |
| A、正反应为吸热反应 | ||
| B、实验1中,CO的转化率为80% | ||
C、650℃时,化学平衡常数K=
| ||
| D、实验1再加入1.0 mol H2O,重新达到平衡时,n(CO2)为1.6 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③ | B、②⑥ | C、③④ | D、④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A. | 不同温度下,取 0.1 mol?L-1KI 溶液,向其中先加入 0.1 mol?L-1 的硫酸,再加入淀粉溶液,发生反应 4H++O2+4I-=2I2+2H2O | 探究溶液出现蓝色的时间 与温度的关系 |
| B. | 相同温度下,测定等浓度的 Na2CO3 和 NaClO 的 pH | 比较 H2CO3 和 HClO 的酸 性 |
| C. | 在加热搅拌的条件下向溶液中加入 MgCO3,过滤后, 再向滤液中加入适量盐酸 | 除去 MgCl2 酸性溶液中的 Fe3+ |
| D. | 向 5mL0.1 mol?L-1AgNO3 溶 液 中 滴 加 几 滴 0.1mol?L-1 NaCl 溶液,生成白色沉淀,再滴加几滴 0.1 mol?L-1KI 溶液,观察沉淀颜色变化 | 探究 AgCl 沉淀能否转化 为 AgI 沉淀 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,水的电离程度相同 |
| B、常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H<0 |
| C、常温下,将pH=10的氨水稀释,溶液中所有离子浓度都减小 |
| D、常温下,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+)增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
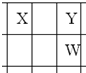 X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素.其中只有Z是金属,W的单质是黄色固体,X、Y、W在周期表中的相对位置关系如图所示.下列说法正确的是( )
X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素.其中只有Z是金属,W的单质是黄色固体,X、Y、W在周期表中的相对位置关系如图所示.下列说法正确的是( )| A、五种元素中,原子半径最大的是W |
| B、Y的简单阴离子比W的简单阴离子还原性强 |
| C、Y与Z形成的化合物都可以和盐酸反应 |
| D、X与Q形成的化合物是离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| A、增加压强 |
| B、升高温度 |
| C、增大H2O的浓度 |
| D、更换催化剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com