
【题目】设NA为阿伏加德罗常数的值,下列说法不正确的是( )
A.46 g C2H6O中含有的C-H键数一定为5NA
B.常温常压下,17g甲基(-14CH3)所含电子总数为9NA
C.标准状况下,11.2 L CO2和乙炔的混合气体所含![]() 键数目为NA
键数目为NA
D.CO2气体与足量的Na2O2反应,固体增重28g时转移了NA个电子
【答案】A
【解析】
A. 46 g C2H6O的物质的量n(C2H6O)=46 g ÷ 46 g/mol=1 mol,而C2H6O表示的物质可能为乙醇,也可能为二甲醚,当为二甲醚时,1 mol C2H6O含6 molC-H键,A错误;
B.—14CH3的摩尔质量为17 g/mol,1个甲基中含有9个电子,17 g甲基(—14CH3)的物质的量n(—14CH3)=17g ÷ 17 g/mol=1 mol,所以1 mol甲基含9 mol电子,B正确;
C. 标况下,11.2 LCO2和乙炔的混合气体的物质的量n=11.2 L ÷22.4 L/mol=0.5 mol,而1 mol CO2和乙炔中均含2 molπ键,故0.5 mol混合气体中含1 mol π键,C正确;
D. CO2气体与Na2O2反应,产生Na2CO3和O2,增重的质量等于CO的质量,且每有2 mol CO2气体参与反应,增重2 mol CO的质量,转移2mol电子,故当增重28g时,增重的是CO的物质的量n(CO)=1 mol,转移了1 mol电子,D正确;
故合理选项是A。


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:
【题目】有机化学中的反应类型较多,现有如下反应:
①乙醛发生银镜反应 ②由乙炔制氯乙烯 ③乙醇与浓氢溴酸混合共热④甲苯使酸性高锰酸钾溶液褪色⑤溴乙烷和氢氧化钠的乙醇溶液共热 ⑥苯酚与浓溴水的反应
(1)其中属于取代反应的是_____________,(填序号,下同)属于氧化反应的是__________________,属于加成反应的是__________________,属于消去反应的是_______________________.
(2)写出反应①的方程式_________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环丁基甲酸是有机合成中一种有用的中间体。某研究小组以丙烯醛为原料,设计了如下路线合成环丁基甲酸(部分反应条件、产物已省略)。
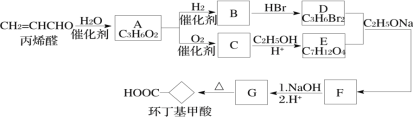
已知:
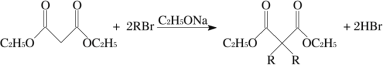
(1)
(2)![]()
请回答下列问题:
(1)由丙烯醛生成化合物A的反应类型为____________。
(2)化合物C的结构简式是________________________。
(3)下列说法中正确的是___________(填字母代号)。
A.丙烯醛可以发生银镜反应 B.化合物B和C能形成高聚物
C.化合物G的化学式为C6H8O4 D.1mol化合物B与足量金属钠反应能生成1mol氢气
(4)写出D+E→F的化学方程式:__________________________________________。
(5)符合下列条件的G的同分异构体有____________种,写出其中在1H-NMR谱上显示两组峰且面积比为3∶1的结构简式:______________________。
①能使Br2/CCl4溶液褪色;②1mol G与1mol Na2CO3反应可以生成1mol CO2
(6)以1,3-丁二烯和化合物E为原料可制备![]() ,请选用必要的试剂设计合成路线____________________。
,请选用必要的试剂设计合成路线____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水的电离过程为H2O![]() H++OH-,在25℃和35℃时其离子积分别为1.0×10-14、2.1×10-14。下列说法正确的是( )
H++OH-,在25℃和35℃时其离子积分别为1.0×10-14、2.1×10-14。下列说法正确的是( )
A.水的电离过程是吸热过程
B.c(H+)随着温度升高而降低
C.水的电离度α(35℃)>α(25℃)
D.在25℃时,纯水中c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值,下列说法正确的是( )
A.标准状况下,22.4 L庚烷的分子数约为NA
B.1 L0.1mol/L的Na2S溶液中S2-和HS-的总数为0.1NA
C.4.0 g![]() 与D2O的混合物中所含中子数为2NA
与D2O的混合物中所含中子数为2NA
D.50 mL12mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业用强氧化剂PbO2来制备KClO4的工业流程如下:
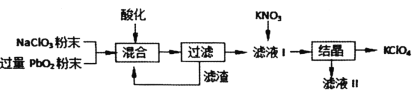
根据流程推测,下列判断不正确的是( )
A.“酸化”的试剂是稀硝酸或浓盐酸
B.“滤渣”主要成分是PbO2粉末,可循环使用
C.NaClO3与PbO2反应的离子方程式为![]()
D.在KNO3、KClO4、NaClO4、NaNO3中,常温下溶解度小的是KClO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯胺(NCl3)是一种饮用水二级消毒剂,可由以下反应制备:
Ⅰ.![]()
![]()
回答下列问题:
(1)已知:Ⅱ.![]()
![]()
Ⅲ.![]()
![]()
则![]() =________(用含
=________(用含![]() 和
和![]() 的代数式表示)。
的代数式表示)。
(2)向容积均为2L的甲乙两个恒温密闭容器中分别加入4mol NH3和4mol Cl2,发生反应Ⅰ,测得两容器中n(Cl2)随反应时间的变化情况如下表所示:
时间/min | 0 | 40 | 80 | 120 | 160 |
容器甲(T1) | 4.0 | 3.0 | 2.2 | 1.6 | 1.6 |
容器乙(T2) | 4.0 | 2.9 | 2.0 | 2.0 | 2.0 |
①0~80min内,容器甲中v(NH3)=________________。
②反应Ⅰ的![]() ________0(填“>”或“<”),其原因为________________________。
________0(填“>”或“<”),其原因为________________________。
③关于容器乙,下列说法正确的是________(填选项字母)。
A.容器内![]() ,说明反应达到平衡状态
,说明反应达到平衡状态
B.反应进行到70min时,v正一定大于v逆
C.容器内气体平均相对分子质量在增大,说明平衡在正向移动
D.达平衡后,加入一定量NCl3(l),平衡逆向移动
E.达平衡后,按原投料比再充入一定量反应物,平衡后NH3的转化率增大
④温度为T1时HCl(g)的平衡体积分数=________,该温度下,若改为初始体积为2L的恒压容器,平衡时容器中n(Cl2)________(填“>”、“=”或“<”)1.6mol。
⑤温度为T2时,该反应的平衡常数K=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列相关实验的描述正确的是( )
A.可用CCl4萃取碘酒中的碘
B.做焰色反应实验时,透过蓝色钴玻璃,观察到火焰颜色为紫色,证明被检验物为一定为钾盐
C.不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上2%~5%的硼酸溶液
D.室温下,浓度为0.1molL-1Na2S2O3和H2SO4溶液,分别取5mL与10mL混合,10mL与10mL混合,可验证Na2S2O3浓度对反应速率的影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷化硼是一种超硬耐磨涂层材料。下图为其晶体结构中最小的重复结构单元,其中的每个原子均满足8电子稳定结构。下列有关说法正确的是( )

A.磷化硼晶体的化学式为BP,属于离子晶体
B.磷化硼晶体的熔点高,且熔融状态下能导电
C.磷化硼晶体中每个原子均形成4条共价键
D.磷化硼晶体结构微粒的空间堆积方式与氯化钠相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com