
【题目】硝酸与金属反应,浓度不同生成的还原产物也可能不同。某兴趣小组进行了如下实验探究。
[查阅资料]
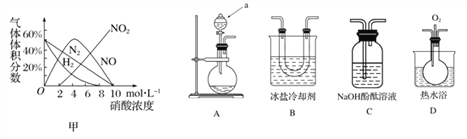
a.镁与硝酸反应生成各气体产物成分及含量随HNO3浓度变化曲线如图甲所示
b.NO2沸点:21 ℃;NO沸点:-151 ℃
c.2NO2+2OH-===NO![]() +NO
+NO![]() +H2O,NO+NO2+2OH-===2NO
+H2O,NO+NO2+2OH-===2NO![]() +H2O
+H2O
(1)请写出Mg放入10 mol·L-1硝酸中反应的化学方程式:______________________;
[实验探究] 该小组拟选用如图A B C D所示装置探究镁与4 mol·L-1硝酸反应的产物。连接装置A→B→C→D→C,检查气密性,按图示加入试剂,D中通入的O2微过量。
(2)a仪器的名称是_____________。
(3)前一个C装置的作用是_______,证明气体产物中有NO生成的实验现象是______。
(4)从后一个C装置中逸出的气体是________。
(5)某同学测想A溶液中可能还有一种还原产物NH4NO3,请设计实验验证他的猜想_____。
【答案】 Mg+4HNO3===Mg(NO3)2+2H2O+2NO2↑ 分液漏斗 吸收未被冷却的二氧化氮 C中酚酞溶液不褪色,D装置中有红棕色气体出现 氮气和氢气 取少量A中溶液于试管中,加入过量浓氢氧化钠溶液,将湿润的红色石蕊试纸放在试管口,微热试管,如果红色石蕊试纸变蓝,则可证明有铵根离子产生,产物中含硝酸铵
【解析】(1)根据图象可知,Mg放入10mol/L硝酸中产生二氧化氮,反应的化学方程式为Mg+4HNO3=Mg(NO3)2+2H2O+2NO2↑;(2)根据装置图可知仪器a的名称为分液漏斗;(3)前一个C装置是吸收未被冷却的二氧化氮,防止其对后面一氧化氮的检验产生影响,一氧化氮为无色气体,遇到空气中的氧气能被氧化成红棕色的二氧化氮,所以看到C中酚酞溶液不褪色,D装置中有红棕色气体出现,则证明体产物中有NO生成;(4)在D装置中一氧化氮被氧化成二氧化氮,二氧化氮被氢氧化钠吸收,氢气和氮气不能被吸收,所以从后一个C装置中逸出的气体主要是氮气和氢气;(5)硝酸铵是铵盐,与强碱反应生成氨气,氨气是碱性气体,所以检验硝酸铵的实验方案是:在所得溶液中加入浓氢氧化钠溶液并微热,用湿润的红色石蕊试纸检验,如果红色石蕊试纸变蓝,则可证明的铵根离子产生,产物中含有硝酸铵。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列各选项中的物质均能发生丁达尔效应的是( )
A. 雾、含灰尘颗粒的空气、有色玻璃 B. 酒、生理盐水、花生油
C. 水晶、金刚石、冰 D. 大理石、高岭石、电石
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为实验室某浓硫酸试剂瓶的标签,试根据标签上的有关数据回答下列问题:
硫酸
分子式:H2SO4
相对分子质量:98
密度:1.84g/mL
H2SO4的质量分数:98%
(1)该浓硫酸中H2SO4的物质的量浓度为_________。
(2)某学生欲用上述浓硫酸和蒸馏水配制100mL物质的量浓度为0.8 mol·L-1的稀硫酸,该学生需要量取_________mL上述浓硫酸进行配制。
(3)为配制(2)中的稀硫酸,除了量筒、烧杯、胶头滴管外,还缺少的玻璃仪器是_________。
(4)在配制过程中,下列实验操作可能导致配制的硫酸溶液浓度偏高的是_________(填序号)。
a.定容时俯视观察
b.定容后经振荡、摇匀、静置后,发现液面下降,再加适量的蒸馏水
c.浓硫酸在烧杯中加水稀释后,未冷却就向容量瓶中转移
d.容量瓶未干燥即用来配制溶液
e.往容量瓶转移时,有少量液体溅出;
f.未洗涤稀释浓硫酸的烧杯;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在标准状况下,有物质①4gH2,②33.6LCH4, ③1molH2O,④3.01×1023个O2,含分子数最多的是(填序号,下同)______________,质量最大的是______,体积最小的________,密度由大到小的顺序为:________________________。
(2)在无土栽培中,配制1 L内含5 mol NH4Cl、1.6 mol KCl、2.4 mol K2SO4的某营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需这三种固体的物质的量分别为________、_________ 、_____________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组元素,按原子半径依次减小,元素第一电离能逐渐升高的顺序排列的是( )
A. K、Na、Li B. N、O、C C. Cl、S、P D. Al、Mg、Na
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应2X(g)+Y(g)![]() 2Z(g);△H<0,在不同温度(T1和T2)下,产物Z的物质的量n与反应时间t的关系如图所示,则下列判断中正确的是( )
2Z(g);△H<0,在不同温度(T1和T2)下,产物Z的物质的量n与反应时间t的关系如图所示,则下列判断中正确的是( )
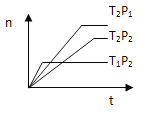
A. T1<T2,P1<P2 B. T1<T2,P1>P2
C. T1>T2,P1>P2 D. T1>T2,P1<P2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用 63%的浓 HNO3 (其密度为 1.4 g·mL -1)配制 240 mL 0.50 mol·L-1 稀 HNO3,若实验仪器有:
A.10 mL 量筒 B.50 mL 量筒 C.托盘天平 D.玻璃棒 E.100 mL 容量瓶 F.250 mL 容量瓶 G.500 mL 容量瓶 H.胶头滴管 I.200mL 烧杯
(1)此浓硝酸的物质的量浓度为_____mol·L -1。
(2)应量取 63%的浓硝酸_____mL,应选用_____(填仪器的字母编号)。
(3)实验时还需选用的仪器有 D、I、______(填序号)。
(4)配制过程中,下列操作会使配制的稀硝酸溶液浓度偏高的是(填序号)______。
①量取浓硝酸的量筒用蒸馏水洗涤 2~3 次,并把洗涤液转入容量瓶
②容量瓶使用时未干燥
③溶解后未经冷却就移液
④定容时不小心有少量蒸馏水滴到瓶外
⑤定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[选修5:有机化学基础](20分)
Ⅰ(6分)
香茅醛(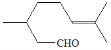 )可作为合成青蒿素的中间体,关于香茅醛的叙述正确的有
)可作为合成青蒿素的中间体,关于香茅醛的叙述正确的有
A.分子式为C10H18O B.不能发生银镜反应
C.可使酸性KMnO4溶液褪色 D.分子中有7种不同化学环境的氢
Ⅱ(14分)
当醚键两端的烷基不相同时(R1-O-R2,R1≠R2),通常称其为“混醚”。若用醇脱水的常规方法制备混醚,会生成许多副产物:
R1—OH+ R2—OH ![]() R1—O—R2+ R1—O—R1+ R2—O—R2+H2O
R1—O—R2+ R1—O—R1+ R2—O—R2+H2O
一般用Williamson反应制备混醚:R1—X+ R2—ONa→R1—O—R2+NaX,某课外研究小组拟合成![]() (乙基苄基醚),采用如下两条路线进行对比:
(乙基苄基醚),采用如下两条路线进行对比:
Ⅰ:![]()
Ⅱ:①![]()
②![]()
③![]()
回答下列问题:
(1)路线Ⅰ的主要副产物有______________、______________。
(2)A的结构简式为______________。
(3)B的制备过程中应注意的安全事项是______________。
(4)由A和B生成乙基苄基醚的反应类型为______________。
(5)比较两条合成路线的优缺点:______________。
(6)苯甲醇的同分异构体中含有苯环的还有________种。
(7)某同学用更为廉价易得的甲苯替代苯甲醇合成乙基苄基醚,请参照路线Ⅱ,写出合成路线______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】仅用下表提供的玻璃仪器(非玻璃仪器任选)或实验装置就能达到相应实验目的的是
选项 | A | B | C | D |
实验目的 | 除去KCl中少量MnO2 | 用10 mol·L-1盐酸配制100mL0.1 mol·L-1盐酸 | 用含有少量NH4Cl杂质的NaCl溶液制备氯化钠晶体 | 制乙炔的发生装置 |
实验仪器或装置 | 烧杯、玻璃棒、分液漏斗 | 100 mL容量瓶、玻璃棒、烧杯 |
|
|
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com