
某学生用实验方法来分析碳酸钠的纯度。该同学设计出如图②所示的实验装置(各符号代表的仪器如图①所示),其中A中盛有一定量的碳酸钠样品,分液漏斗内盛装稀硫酸,B内为碱石灰固体。他利用碱石灰的增重求出纯净的碳酸钠质量,再求纯度。重复正确操作3次,结果出现较大的偏差。
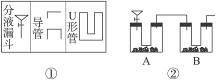
通过仔细分析,该同学重新设计了一套装置(如下图所示)(实验室可供选择的试剂和药品有锌片、浓硫酸、氢氧化钙溶液、碳酸钙固体、蒸馏水)。
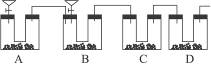
完成下列问题:
(1)请分析在实验改进前,实验中出现较大偏差的原因:______________________________。
(2)在改进后的实验中,A装置分液漏斗中所盛的液体为__________,U形管内盛有。在整套装置中,A的作用是__________________________;D装置中U形管内盛有__________,D装置在整套装置中的作用是_____________________。
(3)该同学新设计的实验装置(如上图所示)是否完整?如果不完整,请画出应该补充的装置简图,并在图中标明所用药品或试剂。
(1)①U形管A中产生的CO2不可能全部进入U形管B中;②U形管A中产生CO2的同时还会带出水蒸气进入U形管B中;③空气中的CO2和水蒸气会进入U形管B中。由于存在上述3种原因,碱石灰增重的质量就不等于CO2 的质量,因此在测量过程中将会出现较大的偏差
(2)稀硫酸 锌片 产生氢气,把B装置中产生的二氧化碳气体全部通入后面装置中,确保二氧化碳被
充分吸收 碱石灰 吸收空气中的CO2和H2O,避免进入装置C中
(3)不够完整。必须在装置B、C之间加入一个干燥装置(如图所示)
![]()
本题的实验原理很简单:让待测的碳酸钠样品与硫酸反应,用碱石灰吸收反应产生的气体,通过称量吸收装置的质量确定反应放出的CO2的量,进而求得碳酸钠的质量和纯度。原理虽然很简单,但实验设计过程中必须排除水蒸气、空气等因素的干扰。
实验改进前,装置仅由二氧化碳产生装置A以及二氧化碳吸收装置B组成,仅从实验原理的角度来看是可行的。结合实验操作实际,就会发现如下问题:(1)装置A中留住部分CO2;(2)产生CO2的同时,必然会带出水蒸气;(3)吸收装置B的导管直接暴露在空气中,会吸收空气中的CO2、水蒸气。由于这些因素的存在,测量过程中必将出现较大的偏差。
正是由于存在上述问题,因此实验装置必须进行改进。结合上面分析,很容易推断出改进后实验装置中盛放的药品和它们对应的作用,其中B是二氧化碳的发生装置(碳酸钠样品和硫酸反应),而装置A的作用就是把装置B产生的二氧化碳全部排出以利于充分吸收,装置D的作用是避免空气带来的实验干扰(即避免空气中的CO2和水蒸气被吸收二氧化碳的装置C所吸收),装置C的作用显然是吸收二氧化碳。明确装置的作用,就可确定各装置所装的药品,其中A中的药品为稀硫酸和锌片,B中的药品为稀硫酸和碳酸钠样品,C和D中的样品均为碱石灰。
通过对上述实验原理的分析,可以发现改进后的装置仍然存在问题:随碳酸钠与硫酸反应产生的CO2带出的水蒸气没有处理。因此还需对“改进”了的实验装置进一步改进,即在B、C装置之间再安装一个吸收水蒸气的装置。


科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:
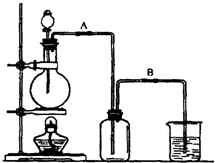 某校化学研究性学习小组用浓盐酸与二氧化锰加热反应来制取并收集氯气,装置如下:
某校化学研究性学习小组用浓盐酸与二氧化锰加热反应来制取并收集氯气,装置如下:查看答案和解析>>
科目:高中化学 来源:黄冈重点作业·高二化学(下) 题型:022
某学生设计了下述五个实验步骤来分馏石油:
①将蒸馏烧瓶固定在铁架台上,在蒸馏烧瓶上塞好带温度计的橡皮塞.
②连接好冷凝管,把冷凝管固定在铁架台上,将冷凝管进水口橡皮管的另一端和水龙头连接,将连接出水口的橡皮管的另一端放在水池中.
③把酒精灯放在铁架台上,根据酒精灯的高度确定铁圈的高度,放好石棉网.
④向蒸馏烧瓶中放入几片碎瓷片,再用漏斗向烧瓶中加入原油,塞好带温度计的橡皮塞,把连接器连接在冷凝管的末端,并伸入收集装置(如锥形瓶)中.
⑤检查气密性(通过对固定装置微热的方法).
(1)正确的操作顺序是________________________.
(2)向蒸馏烧瓶中放入几片碎瓷片的作用是________________,温度计水银球的位置应在________________.
(3)本实验在60℃~150℃收集的馏分是________,在150℃~300℃收集的馏分是________.
查看答案和解析>>
科目:高中化学 来源: 题型:

通过仔细分析,该同学重新设计了一套装置(如下图所示)(实验室可供选择的试剂和药品有锌片、浓硫酸、氢氧化钙溶液、碳酸钙固体、蒸馏水)。

完成下列问题:
(1)请分析在实验改进前,实验中出现较大偏差的原因:______________________________。
(2)在改进后的实验中,A装置分液漏斗中所盛的液体为__________,U形管内盛有。在整套装置中,A的作用是__________________________;D装置中U形管内盛有__________,D装置在整套装置中的作用是_____________________。
(3)该同学新设计的实验装置(如上图所示)是否完整?如果不完整,请画出应该补充的装置简图,并在图中标明所用药品或试剂。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com