
| A. | 任何可逆反应都有一定的限度,且限度是可以改变的 | |
| B. | 对任何化学反应来说,反应速率越大,则现象越明显 | |
| C. | 决定化学反应速率的主要因素是温度、浓度、压强 | |
| D. | 铁与稀硫酸反应制氢气时,改用98.3%的浓硫酸,对增大化学反应速率明显有效 |
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
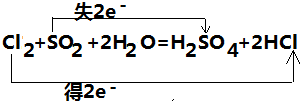
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用丁达尔效应区分溶液和胶体 | |
| B. | 向沸水中滴加饱和的FeCl3溶液制取Fe(OH)3胶体 | |
| C. | 用渗析的方法除去胶体中的离子或分子 | |
| D. | 用滤纸过滤除去溶液中的胶体粒子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

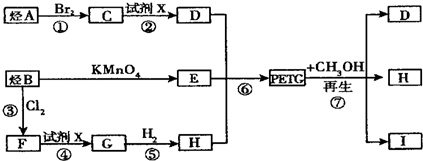
 $\stackrel{KMnO_{4}}{→}$
$\stackrel{KMnO_{4}}{→}$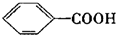
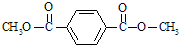 .
.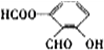 、
、 、
、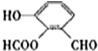 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
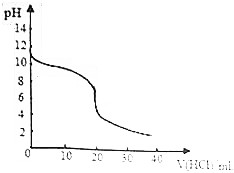 常温下,向20.00mL0.1000mol/L的氨水中逐滴加入0.1000mol/L的盐酸,pH随盐酸体积的变化如图所示.下列说法正确的是( )
常温下,向20.00mL0.1000mol/L的氨水中逐滴加入0.1000mol/L的盐酸,pH随盐酸体积的变化如图所示.下列说法正确的是( )| A. | 滴加盐酸10mL 时,c(Cl-)>c(NH4+)>c(NH3•H2O)>c(OH-)>c(H+) | |
| B. | 滴加盐酸20m时,c(H+)=c(OH-)+c(NH3•H2O) | |
| C. | 滴加盐酸10 mL时溶液的导电能力与滴加盐酸20mL时溶液的导电能力相同 | |
| D. | pH<7时,消耗盐酸的体积一定大于20.00mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若n(Cu2+):n(IO3-)=1:1,则每生成1molCuI转移6mol电子 | |
| B. | 若n(Cu2+):n(IO3-)=1:2,则每生成1molCuI转移12mol电子 | |
| C. | CuI既是氧化产物又是还原产物 | |
| D. | HI只有还原性没有氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
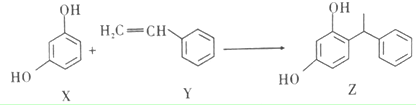
| A. | X、Y和Z均能和NaOH溶液反应 | |
| B. | X和Z均能和Na2CO3溶液反应,但不能和NaHCO3溶液反应 | |
| C. | Y既能发生加聚反应,也能发生缩聚反应 | |
| D. | Y分子中所有原子不可能共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
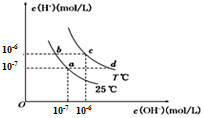 在不同温度下,水溶液中c(H+)与c(OH- )有如图所示关系.下列说法正确的是( )
在不同温度下,水溶液中c(H+)与c(OH- )有如图所示关系.下列说法正确的是( )| A. | c点对应的溶液pH=6,溶液呈弱酸性 | |
| B. | b点对应的溶液中可以大量共存:NH4+、K+、CO32-、Cl- | |
| C. | 若a点表示CH3COOH和CH3COONa的混合溶液,则该溶液中的离子浓度大小为:c(Na+ )>c(CH3COO-)>C(OH- )>c(H + ) | |
| D. | 若d点表示某等浓度、等体积的NH3•H2O和NH4Cl混合溶液,则溶液中的离子浓度存在如下关系:c(NH4+)+2c(H+)═2c(OH-)+c(NH3•H2O) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com