
(12分)
(1) 根据所学化学反应原理填空:
①升高温度时,水的pH (填“增大”“减小”或“不变 ”)
”)
②体积、pH均相同的盐酸 和醋酸溶液,中和等浓度的NaOH溶液时所需体积分别为V1、V2 。则V1 V2(填“<”、“>”或“=”)
和醋酸溶液,中和等浓度的NaOH溶液时所需体积分别为V1、V2 。则V1 V2(填“<”、“>”或“=”)
③某反应放热且熵增加,该反应 自发进行(用“能”或“不能”表示)
(2)依据事实,用化学用语填空:
①1 mol NO2气体与水完全反应生成硝酸溶液和NO气体,放出热量4 6 kJ。该反应的热化学方程式______________________________________。
6 kJ。该反应的热化学方程式______________________________________。
②用离子方程式表示氯化铵溶液的酸碱性:_ 。
③用离子方程式表示向碳酸镁沉淀中加入NaOH溶液后的沉淀转化:
。
科目:高中化学 来源: 题型:阅读理解
 (2011?南开区一模)能源开发、环境保护、资源利用等是当今社会的热门话题.请根据所学化学知识回答下列问题:
(2011?南开区一模)能源开发、环境保护、资源利用等是当今社会的热门话题.请根据所学化学知识回答下列问题:| 物 质 | CO | H2 | CH3OH |
| 浓度/(mol?L-1) | 1.2 | 1.0 | 0.6 |
| c(CH3OH) |
| c(CO)c2(H2) |
| c(CH3OH) |
| c(CO)c2(H2) |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 实验步骤 | 1将一小块金属钠放入滴有酚酞溶液的冷水中; 2将一小段用砂纸打磨后的镁带放入试管中,加入少量水,加热至水沸腾,冷却后,向试管中滴加酚酞溶液; 3将一小段镁带投入稀盐酸中; 4将一小片铝投入稀盐酸中. |
| 实验现象 | A剧烈反应,迅速生成大量的气体 B浮在水面上,熔成小球,不断游动,小球渐小最终消失,溶液变红 C反应不剧烈,产生无色气体 D有气体产生,溶液变成红色 |
| 实验步骤 | 1 | 2 | 3 | 4 |
| 实验现象 | B B |
D D |
A A |
C C |
查看答案和解析>>
科目:高中化学 来源: 题型:
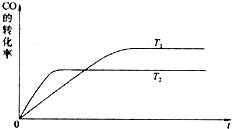
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
+ 4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com