
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ③④ | D. | ③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 75 mL 1 mol•L-1AlCl3溶液 | B. | 75 mL 0.5mol•L-1CaCl2溶液 | ||
| C. | 150 mL 1 mol•L-1 NaCl溶液 | D. | 150 mL 2 mol•L-1 KCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该反应为吸热反应 | |
| B. | 该反应为非氧化还原反应 | |
| C. | NO和CO2的键能总和大于NO2和CO的键能总和 | |
| D. | 1 molNO2(g)和1 mol CO(g)的总能量低于 1mol NO(g)和1 molCO2(g)的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 乙醇发生了还原反应 | B. | 反应中有红黑颜色交替变化的现象 | ||
| C. | 铜是此反应的催化剂 | D. | 生成物是乙醛 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 l2、NaCl、H2O、CO2,写出并配平有关化学方程式,并标出电子转移的方向和数目
l2、NaCl、H2O、CO2,写出并配平有关化学方程式,并标出电子转移的方向和数目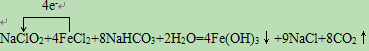 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 弱酸 | HClO2 | HF | HCN | HS |
| Ka/mol•L-1 | 1×10-2 | 6.3×10-4 | 4.9×10-10 | K1=9.1×10-8 K2=1.1×10-12 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

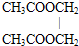 .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com