
【题目】Ⅰ、依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示,
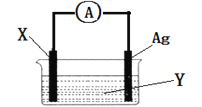
(1)电极X的材料是________________;
电解质溶液Y是_________________;
(2)银电极为电池的______极,发生的电极反应为____________;X电极上发生的电极反应为________________;
(3)外电路中的电子是从____电极流向_____电极。(用电极材料名称作答)
若原来两电极棒质量相等,则当电路中通过0.2mol电子时,两个电极的质量差为__g。
Ⅱ、在一密闭容器中发生反应N2+3H2![]() 2NH3,正反应为放热反应,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:
2NH3,正反应为放热反应,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:
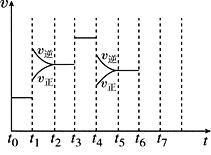
(1)处于平衡状态的时间段是______________(填选项)。
A.t0~t1 B.t1~t2 C.t2~t3
D.t3~t4 E.t4~t5 F.t5~t6
(2)t1、t3、t4时刻分别改变的一个条件是
t1时刻__________;t3时刻_______;t4时刻_______。
A.增大压强 B.减小压强 C.升高温度
D.降低温度 E.加催化剂 F.充入氮气
(3)依据(2)中的结论,下列时间段中,氨的百分含量最高的是_______(填选项)。
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6
(4)如果在t6时刻,从反应体系中分离出部分氨,t7时刻反应达到平衡状态,请在图中画出反应速率的变化曲线。_____
(5)合成氨反应起始只投氮气和氢气,一定条件下,反应达到化学平衡状态时,测得混合气体中氨气的体积分数为20%,则反应后与反应前的混合气体体积之比为_________。
【答案】 铜 AgNO3溶液 正 2Ag++2e-→2Ag Cu→Cu2++2e- 铜 银 28.0g A、C、D、F C E B A 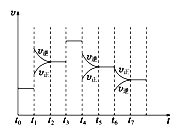 6:5
6:5
【解析】Ⅰ、(1)由反应“2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)”可知,在反应中,Cu被氧化,失电子,应为原电池的负极,Ag+在正极上得电子被还原,电解质溶液为AgNO3 (2)正极为活泼性较Cu弱的Ag,Ag+在正极上得电子被还原,电极反应为Ag++e-=Ag;X电极上发生的电极反应为Cu→Cu2++2e-;(3)外电路中的电子是从铜电极流向银电极。若刚开始Cu电极和银电极的质量相等,当电路中通过0.2mol电子时,正极上生成Ag为0.2mol,即21.6g,负极上Cu溶解的物质的量为0.1mol,即6.4g,所以两个电极的质量差为28.0g
Ⅱ、:(1)根据图示可知,t0~t1、t2~t3、t3~t4、t5~t6时间段内,v正、v逆相等,反应处于平衡状态,故答案为:ACDF;(2)由N2(g)+3H2(g)2NH3(g)△H<0,可知,该反应为放热反应,且为气体体积减小的反应,则由图可知,t1正逆反应速率均增大,且逆反应速率大于正反应速率,改变条件应为升高温度;t3时正逆反应速率均增大,且逆反应速率等于正反应速率,改变条件应为加催化剂; t4时,正逆反应速率均减小,且逆反应速率大于正反应速率,平衡逆向移动,改变条件应为减小压强;答案为C、E、B;(3)由图可知,t1平衡逆向移动,t3不移动,t4平衡逆向移动,均使氨气的含量减少,则t0~t1氨气的含量最大,故选A;(4)如果在t6时刻,从反应体系中分离出部分氨,t7时刻反应达到平衡状态,请在图中画出反应速率的变化曲线。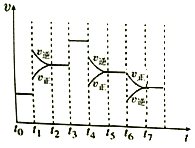 ;
;
(5)设反应前加入a mol N2,b mol H2,达平衡时生成2x mol NH3,
N2(g)+3H2(g)2NH3(g)
起始 a b 0
转化 x 3x2x
平衡 a-x b-3x 2x
则反应后气体总的物质的量=(a+b-2x)mol![]() ,解得:a+b=12x,故反应后与反应前的混合气体体积之比=
,解得:a+b=12x,故反应后与反应前的混合气体体积之比=![]() 。
。


科目:高中化学 来源: 题型:
【题目】CH2=CH-COOCH3是重要的有机合成中间体,可以通过下列反应合成
CH2=CH-COOH+CH3OH![]() CH2=CH-COOCH3+H2O
CH2=CH-COOCH3+H2O
下列说法错误的是( )
A. 该有机合成反应属于取代反应
B. CH2=CH-COOCH3分子中处于同一平面的原子最少有3个
C. CH2=CH-COOH没有官能团相同的同分异构体
D. CH2=CH-COOCH3可以发生加成、氧化、取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸晶体(H2C2O4·xH2O)无色,熔点为101℃,易溶于水,受热易脱水、升华,170℃以上分解,草酸钙难溶于水。某研究性小组按照下图装置,检验草酸晶体的分解产物中含有CO、CO2。已知C、E、H中盛装澄清石灰水,D中盛装浓NaOH溶液,G中盛有CuO。

(1)装置B的主要作用是_______。
(2)装置C中反应的离子方程式为_______。
(3)装置D的作用是_______。
(4)装置F所盛的药品是_______。
(5)能证明草酸晶体分解产物中有CO的现象是_______。
(6)H后连接的尾气处理装置为_______。(从“Ⅰ”“Ⅱ”中选择)
(7)为测定草酸晶体分子式(H2C2O4·xH2O) 中x的值,现做如下实验。
①称取6.3 g草酸晶体,将其配置成100.0 mL水溶液为待测溶液;
②取25.0 mL待测溶液放入锥形瓶中,再加入适量的稀硫酸;
③用浓度为0.4 mol/L的KMnO4标准溶液进行滴定,达到滴定终点时,用去12.50 mL KMnO4溶液。
回答下列问题。
写出H2C2O4和酸性KMnO4溶液反应的化学方程式_______;经计算x=_______。
(8)依据以上实验,写出草酸晶体(H2C2O4·xH2O)受热分解的化学方程式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】假如生长激素由两条多肽链组成,在生长激素的缩合过程中脱掉的水分子相对分子质量为3 384,已知20种氨基酸的平均分子质量为130,此蛋白质的分子量最接近于 ( )
A. 24 700 B. 21 316 C. 24 440 D. 440180
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的化合物应用广泛,但氮氧化物是重要的空气污染物,应降低其排放。
(1)用CO2和NH3可合成氮肥尿素[CO(NH3)2]
已知:①2NH3(g)+CO2(g)=NH2CO2NH4 (s) △H=-159.5 kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) △H=+116.5 kJ·mol-1
③H2O(l)=H2O(g) △H=+44 kJ·mol-1
用CO2和NH3合成尿素(副产物是液态水)的热化学方程式为______________。
(2)工业上常用如下反应消除氮氧化物的污染:
CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g) △H
N2(g)+CO2(g)+2H2O(g) △H
在温度为T1和T2时,分别将0.40molCH4和1.0molNO2充入体积为1L的密闭容器中,n(CH4)随反应时间的变化如右图所示:
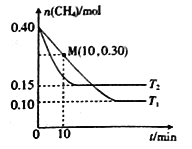
①根据右图判断该反应的△H________0(填“>”、“<”或“=”),理由是______________。
②温度为T1时,0~10min内NO2的平均反应速率v(NO2)=__________,反应的平衡常数K=___(保留三位小数)
③该反应达到平衡后,为在提高反应速率同时提高NO2的转化率,可采取的措施有______(填标号)。
A.改用高效催化剂 B.升高温度
C.缩小容器的体积 D.增加CH4的浓度
(3)利用原电池反应可实现NO2的无害化,总反应为6NO2+8NH3=7N2+12H2O,电解质溶液为NaOH溶液,工作一段时间后,该电池正极区附近溶液pH________(填“增大”、“减小”或“不变”),负极的电极反应式为___________________。
(4)氮的一种氢化物HN3,其水溶液酸性与醋酸相似,则NaN3溶液中各离子浓度由大到小的顺序为________;常温下,将amol·L-1 的HN3与bmol·L-1 的Ba(OH) 2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(N3-),则该混合物溶液呈_______(填“酸”、“碱”或“中”)性,溶液中c(HN3)=_________ mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《化学与生活》模块试题
(1)我国农业因遭受酸雨而造成的损失每年高达15亿多元,酸雨是指pH小于________的雨水,这主要是由人为排放的_______和________(填元素名称)的氧化物等酸性气体转化而成的。为治理酸雨的影响,可将CaCO3粉末撒到受酸雨影响的湖泊中,若用离子方程式表示该反应的本质,请完成如下离子反应:CaCO3+2H+==_____________________________。
主食 | 米饭 |
副食 | 红烧鱼 |
饮品 | 豆浆 |
配菜 | ? |
(2)“民以食为天”,人类生命活动所需的各种营养物质主要来自食物。上表制定的食谱中,主食含有的基本营养物质主要是__________,副食含有的基本营养物质主要是_____________;豆浆所属的分散系为__________________。考虑营养成分的均衡搭配,应补充的配菜是__________________。
(3)水是一种宝贵的自然资源。
①生活污水中,经常包括含__________、___________(填元素符号)的化合物,会造成水体植物营养物质污染。水中的氨在微生物的作用下,可被氧化成HNO2,进而氧化成HNO3,写出这一过程的化学方程式____________________________。
②氧化还原法是处理污水常用的方法。某地工厂排放的污水,经检测,污水中含有0.012 mol/L的游离溴,可用Na2SO3还原除去污水中的溴,请写出其化学方程式:___________________________;处理5 L这种污水,至少需加入0.05 mol/L的 Na2SO3 溶液________L才能将溴全部除去。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z三种元素的原子,其最外层电子排布分别为ns1、3s23p1和2s22p4,由这三种元素组成的化合物的化学式可能是( )
A.XYZ2 B.X2YZ3 C.X2YZ2 D.XYZ3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W为原子序数递增的四种短周期元素,其中Y、Z为金属元素。X、Y、Z、W的最高价氧化物对应的水化物甲、乙、丙、丁之间存在如图所示反应关系(关系图中“—”相连的两种物质能发生反应)。下列判断正确的是

A. X是元素周期表中非金属性最强的元素 B. Z位于元素周期表第3周期IA族
C. 四种原子中,Y原子半径最小 D. W的简单阴离子可能促进水的电离
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com