
| ѡ�� | ������; | ԭ�� |
| A | �ߴ��賣��̫���ܵ�ز��� | ���ǵ�������� |
| B | ��ľ�����̬���ʻ��ʹ������߷�Ч | �����K2CO3��ˮ�з���˫ˮ�⣬������NH3�ݳ� |
| C | Ư�۾���Ư����ɫ����� | 4Fe��NO3��3$\frac{\underline{\;\;��\;\;}}{\;}$2Fe2O3+12NO2��+3O2������ǿ�����ԣ�����ɫ�� |
| D | ��ȼ����һ�־���DZ���������Դ | CH4��ȫȼ�գ��������̳� |
| A�� | A | B�� | B | C�� | C | D�� | D |
���� A��Si�������뵼����ϣ����������غͼ����оƬ��
B����ľ�����̬������ٽ�ˮ�⣻
C��Ư�۾�����Ч�ɷ�ΪCa��ClO��2��ˮ���������Ư���Ե�HClO��
D����ȼ����һ�־���DZ���������Դ����ȼ���ǹ�̬���飬���и���ֵ���ص㣮
��� �⣺A��Si�������뵼����ϣ����������غͼ����оƬ�����ǵ�������壬��A����
B����ľ�����̬������ٽ�ˮ�⣬���ʹ�ý��ͷ�Ч����B����
C��Ư�۾�����Ч�ɷ�ΪCa��ClO��2��ˮ���������Ư���Ե�HClO��������Ҫԭ����Fe��NO3��3���µģ���C����
D����ȼ����һ�־���DZ���������Դ����ȼ���ǹ�̬���飬����ȼ�ղ���CO2��ˮ���������̳�����D��ȷ��
��ѡD��
���� ���⿼�黯ѧ����֪ʶ���ǻ�ѧ����������ϵ�IJ��֣����ǿ�ⷽ��֪ʶ�Ļ��ۺͼ��䣬��Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���տ�����0.4molSO3 | |
| B�� | ��v����O2��=v����SO2��=0ʱһ���ﻯѧƽ�� | |
| C�� | �����¶ȷ�Ӧ���ʼ�С | |
| D�� | ��С�������ѹǿ��Ӧ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

| ʵ���� | ʵ��Ŀ�� | T/K | pH | c/10-3mol•L-1 | |
| H2O2 | Fe2+ | ||||
| I | Ϊ����ʵ�������� | 298 | 3 | 6.0 | 0.30 |
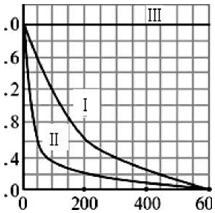
| II | ̽���¶ȶԽ������ʵ�Ӱ�� | �� | �� | �� | �� |
| III | �� | 298 | 10 | 6.0 | 0.30 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��һ������Cl2ͨ��һ��Ũ�ȵĿ��Լ���Һ�У�����ǡ����ȫ��Ӧ����֪��Ӧ���̷��ȣ����������������ֺ���Ԫ�ص����ӣ�����ClO-��ClO3-�������ӵ����ʵ�����n���뷴Ӧʱ�䣨t���ı仯ʾ��ͼ��ͼ��ʾ������˵������ȷ���ǣ�������
��һ������Cl2ͨ��һ��Ũ�ȵĿ��Լ���Һ�У�����ǡ����ȫ��Ӧ����֪��Ӧ���̷��ȣ����������������ֺ���Ԫ�ص����ӣ�����ClO-��ClO3-�������ӵ����ʵ�����n���뷴Ӧʱ�䣨t���ı仯ʾ��ͼ��ͼ��ʾ������˵������ȷ���ǣ�������| A�� | ���Լ���Һ��KOH��������16.8 | |
| B�� | ��Ӧ��ת�Ƶ���0.21mol | |
| C�� | ��������ԭ��0.06molClO-��0.03molClO3- | |
| D�� | ClO3-�������������¶���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��Na2CO3+C6H5COOH ��AlCl3+KOH ��P+Cl2��Cu+HNO3���ڲ�ͬ�����µõ���ͬ������ǣ�������
��Na2CO3+C6H5COOH ��AlCl3+KOH ��P+Cl2��Cu+HNO3���ڲ�ͬ�����µõ���ͬ������ǣ�������| A�� | ���� | B�� | ���ڢ� | C�� | ���ܢ� | D�� | ���ܢݢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.1 molFe��0.1molCu�ֱ���0.1molCl2��ȫ��Ӧ��ת�Ƶĵ�������Ϊ0.2NA�� | |
| B�� | 4.6g�л���C2H6O�ķ��ӽṹ�к��е�C-H����Ŀһ��Ϊ0.5NA | |
| C�� | 1 mol FeCl3 ˮ�����ɵ�Fe��OH��3������ΪNA | |
| D�� | 64 g SO2�������O2��һ�������·�Ӧ���ɵ�SO3������ΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��9��Ԫ����û�зǽ���Ԫ�� | |
| B�� | ֻ�е�2��Ԫ��ԭ���������2������ | |
| C�� | ��16��Ԫ�ؾ�Ϊ�ǽ���Ԫ�� | |
| D�� | ������18��Ԫ���У���3�е�Ԫ��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʽ��ͬ���л���һ����ͬ������ | |
| B�� | ͨʽ��ͬ�IJ�ͬ����һ������ͬϵ�� | |
| C�� | ��Է���������ͬ�IJ�ͬ����һ����ͬ���칹�� | |
| D�� | ͬ���칹��֮���ת��һ���ǻ�ѧ�仯 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com