
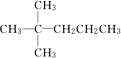
 ,并对其命名2,2-二甲基戊烷.其中另一种同分异构体分子是由烯烃和氢气加成得到,而且该烯烃分子中的碳碳双键只有一种位置,试写出这种烯烃分子的名称3,3-二甲基-1-戊烯.
,并对其命名2,2-二甲基戊烷.其中另一种同分异构体分子是由烯烃和氢气加成得到,而且该烯烃分子中的碳碳双键只有一种位置,试写出这种烯烃分子的名称3,3-二甲基-1-戊烯.分析 (1)根据已知有机物的结构简式可判断,可以通过让两个甲基按照由心到边移动,即可得到同分异构体的结构简式;其中有一种同分异构体的分子,其一氯代物有4种同分异构体,也就是分子结构中有四种氢,写出其结构简式利用烷烃的系统命名法命名;某种烃与H21:1加成得到烷烃,则该烃分子中含有1个碳碳双键,根据加成原理采取逆推法还原C=C双键,烷烃分子中相邻碳原子上均带氢原子的碳原子间是对应烯烃存在碳碳双键的位置.还原双键时注意:先判断该烃结构是否对称,如果对称,只考虑该分子一边的结构和对称线两边相邻碳原子即可;如果不对称,要全部考虑,然后各去掉相邻碳原子上的一个氢原子形成双键;
(2)已知某有机物A在标况下的密度为1.34g/L,摩尔质量为:1.34g/L×22.4L/mol=30g/mol,而取A与氧气反应,得到等物质的量的CO2和H2O,所以最简式为CH2O,由此分析.
解答 解:(1)根据已知有机物的结构简式可判断,可以通过让两个甲基按照由心到边移动,即可得到同分异构体的结构简式,所以共计是4种、分别是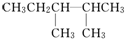 、
、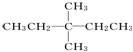 、
、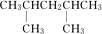 、
、 ,其中有四种不同的氢的是名称分别是2,3二甲基戊烷,另一种同分异构体分子是由烯烃和氢气加成得到,而且该烯烃分子中的碳碳双键只有一种位置,说明相邻碳上有氢,而且对称,则是3,3二甲基戊烷对应的烯烃为:3,3-二甲基-1-戊烯,故答案为:4;
,其中有四种不同的氢的是名称分别是2,3二甲基戊烷,另一种同分异构体分子是由烯烃和氢气加成得到,而且该烯烃分子中的碳碳双键只有一种位置,说明相邻碳上有氢,而且对称,则是3,3二甲基戊烷对应的烯烃为:3,3-二甲基-1-戊烯,故答案为:4; ;2,2-二甲基戊烷; 3,3-二甲基-1-戊烯;
;2,2-二甲基戊烷; 3,3-二甲基-1-戊烯;
(2)已知某有机物A在标况下的密度为1.34g/L,摩尔质量为:1.34g/L×22.4L/mol=30g/mol,而取A与氧气反应,得到等物质的量的CO2和H2O,所以最简式为CH2O,所以分子式为CH2O,作核磁共振氢谱,发现只有一种吸收峰,说明是甲醛,其结构简式为 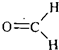 ,结构简式为HCHO,故答案为:CH2O;HCHO.
,结构简式为HCHO,故答案为:CH2O;HCHO.
点评 该题是中等难度的试题,也是高考种的常见考点之一.试题基础性强,贴近高考,注重解题方法的指导与训练,有助于培养学生的逻辑推理能力和逆向思维能力,提高学生分析问题、解决问题的能力.


科目:高中化学 来源: 题型:填空题
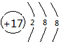 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L1mol/L FeCl3溶液中所含Fe3+的数目为NA | |
| B. | 1mol NaHSO4晶体中所含离子的数目为2NA | |
| C. | 1mol NO2溶于足量水中,转移电子的数目为NA | |
| D. | 常温常压下,22.4L HCHO中所含σ键的数目为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在空气中金属铝表面迅速氧化形成保护层 | |
| B. | 锌与稀硫酸反应时,加入少量NaHSO4固体时,可使反应速率加快 | |
| C. | 红热的铁丝与冷水接触,表面形成蓝黑色保护层 | |
| D. | 镀锌铁表面有划损时,仍然能阻止铁被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 被提纯的物质 | 除杂试剂 | 分离方法 | |
| A | SO2(乙炔) | 溴水 | 洗气 |
| B | 苯(溴) | KI溶液 | 分液 |
| C | 乙醇(乙酸) | 饱和Na2CO3溶液 | 蒸馏 |
| D | 乙烷(乙烯) | KMnO4溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碱金属和卤素单质的熔沸点都逐渐降低 | |
| B. | 碱金属和卤素单质的密度都依次变大 | |
| C. | 卤素的气态氢化物稳定性逐渐增强 | |
| D. | 碱金属单质还原性逐渐增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | baecd | B. | edabc | C. | abdce | D. | ebadc |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源:2017届黑龙江省哈尔滨市高三上学期期中考试化学试卷(解析版) 题型:选择题
某合作学习小组的同学利用下列氧化还原反应设计原电池
2KMnO4+10FeSO4+8H2SO4===2MnSO4+5Fe2(SO4)3+K2SO4+8H2O。盐桥中装有饱和K2SO4溶液,下列叙述中正确的是
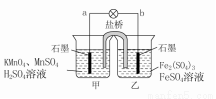
A.乙烧杯中发生还原反应
B.甲烧杯中溶液的pH逐渐减小
C.电池工作时,盐桥中的SO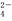 移向甲烧杯
移向甲烧杯
D.外电路的电流方向是从a到b
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com