
 ±ķŹ¾µÄ·Ö×ÓŹ½ĪŖC6H14£»Ćū³ĘŹĒ2-¼×»łĪģĶ飮
±ķŹ¾µÄ·Ö×ÓŹ½ĪŖC6H14£»Ćū³ĘŹĒ2-¼×»łĪģĶ飮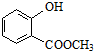 ÖŠŗ¬ÓŠµÄ¹ŁÄÜĶŵÄĆū³ĘĪŖōĒ»ł”¢õ„»ł£®
ÖŠŗ¬ÓŠµÄ¹ŁÄÜĶŵÄĆū³ĘĪŖōĒ»ł”¢õ„»ł£®·ÖĪö £Ø1£©øł¾ŻøĆÓŠ»śĪļµÄ¼üĻߏ½Š“³ö·Ö×ÓŹ½£¬øł¾ŻĻµĶ³ĆüĆū·ØĶź³ÉøĆÓŠ»śĪļµÄĆüĆū£»øł¾ŻÓŠ»śĪļµÄ½į¹¹Š“³ö·Ö×ÓÖŠŗ¬ÓŠµÄ¹ŁÄÜĶÅ£»
£Ø2£©øł¾ŻĶéĢž»łÖ»“ęŌŚĢ¼Į“Ņģ¹¹½įŗĻµČŠ§ĒāŌ×ÓµÄÅŠ¶Ļ·½·ØÖŖŹ¶Ą“»Ų“š£»
£Ø3£©¢ń”¢Ķ¬·ÖŅģ¹¹ĢåŹĒ·Ö×ÓŹ½ĻąĶ¬£¬µ«ŹĒ½į¹¹²»Ķ¬µÄÓŠ»śĪļÖ®¼äµÄ»„³Ę£¬ŗ¬ÓŠČ©»łµÄÓŠ»śĪļæÉŅŌ·¢ÉśŅų¾µ·“Ó¦£®
¢ņ”¢ÓĶÖ¬ŌŚĖįŠŌ»·¾³ĻĀµÄĖ®½ā²śĪļøß¼¶Ö¬·¾Ėį”¢øŹÓĶ£®
½ā“š ½ā£ŗ£Ø1£© £¬·Ö×ÓÖŠŗ¬ÓŠ6øöĢ¼Ō×Ó£¬ŹōÓŚ±„ŗĶĢž£¬·Ö×ÓŹ½ĪŖC6H14£¬øĆÓŠ»śĪļÖ÷Į“ÉĻÓŠ5øöC£¬2ŗÅCŅ»øö¼×»ł£¬ĆüĆūĪŖ£ŗ2-¼×»łĪģĶ飬
£¬·Ö×ÓÖŠŗ¬ÓŠ6øöĢ¼Ō×Ó£¬ŹōÓŚ±„ŗĶĢž£¬·Ö×ÓŹ½ĪŖC6H14£¬øĆÓŠ»śĪļÖ÷Į“ÉĻÓŠ5øöC£¬2ŗÅCŅ»øö¼×»ł£¬ĆüĆūĪŖ£ŗ2-¼×»łĪģĶ飬 ·Ö×ÓÖŠŗ¬ÓŠ¹ŁÄÜĶÅŹĒōĒ»łŗĶõ„»ł£¬¹Ź“š°øĪŖ£ŗC6H14£» 2-¼×»łĪģĶ飻ōĒ»ł”¢õ„»ł£»
·Ö×ÓÖŠŗ¬ÓŠ¹ŁÄÜĶÅŹĒōĒ»łŗĶõ„»ł£¬¹Ź“š°øĪŖ£ŗC6H14£» 2-¼×»łĪģĶ飻ōĒ»ł”¢õ„»ł£»
£Ø2£©Īģ»ł“ęŌŚĢ¼Į“Ņģ¹¹£¬¹²¼ĘÓŠ8ÖÖ½į¹¹£¬¼“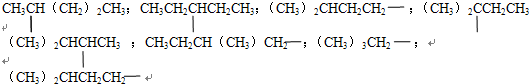 £»ĘäÖŠµÄŗĖ“Ź²ÕńĒāĘ×ÓŠ¶žøöĪüŹÕ·å£¬¼“ŗ¬ÓŠĮ½ÖֵȊ§ĒāŌ×ӵĽį¹¹ŹĒ-CH2C£ØCH3£©3£¬¹Ź“š°øĪŖ£ŗ8”¢-CH2C£ØCH3£©3£®
£»ĘäÖŠµÄŗĖ“Ź²ÕńĒāĘ×ÓŠ¶žøöĪüŹÕ·å£¬¼“ŗ¬ÓŠĮ½ÖֵȊ§ĒāŌ×ӵĽį¹¹ŹĒ-CH2C£ØCH3£©3£¬¹Ź“š°øĪŖ£ŗ8”¢-CH2C£ØCH3£©3£®
£Ø3£©¢ń£®¢Ś¢Ū·Ö×ÓŹ½ĻąĶ¬£¬µ«ŹĒ½į¹¹²»Ķ¬£¬»„ĪŖĶ¬·ÖŅģ¹¹Ģ壬¢ŁĘĻĢŃĢĒ¢ŚĀóŃæĢĒŹĒŗ¬ÓŠČ©»łµÄÓŠ»śĪļ£¬æÉŅŌ·¢ÉśŅų¾µ·“Ó¦£¬¹Ź“š°øĪŖ£ŗ¢Ś¢Ū£»¢Ł¢Ś£»
¢ņ£®ÓĶÖ¬ŌŚĖįŠŌ»·¾³ĻĀµÄĖ®½ā²śĪļĪŖøß¼¶Ö¬·¾Ėį”¢øŹÓĶ£¬¹Ź“š°øĪŖ£ŗøß¼¶Ö¬·¾Ėį”¢øŹÓĶ£®
µćĘĄ ±¾Ģāæ¼²éĮĖÓŠ»śĪļĆüĆū”¢¹ŁÄÜĶŵÄÅŠ¶Ļ£¬ÄŃ¶Č²»“ó£¬ŅŖĒóѧɜĮĖ½āĶéĢžµÄĆüĆū”¢±½µÄĶ¬ĻµĪļµÄĆüĆū¼°¼ņµ„µÄĢžµÄŃÜÉśĪļµÄĆüĆū·½·Ø£¬ŹģĮ·ÕĘĪÕ³£¼ūµÄ¹ŁÄÜĶÅĆū³Ę£®


 æŚĖćŠÄĖćĖŁĖćÓ¦ÓĆĢāĻµĮŠ“š°ø
æŚĖćŠÄĖćĖŁĖćÓ¦ÓĆĢāĻµĮŠ“š°ø Ķ¬²½ĶŲÕ¹ŌĶĮĻµĮŠ“š°ø
Ķ¬²½ĶŲÕ¹ŌĶĮĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | »ÆѧŅ©Ę·×Å»š£¬¶¼ŅŖĮ¢¼“ÓĆĖ®»ņÅŻÄĆš»šĘ÷Ćš»š | |
| B£® | Ć÷·ÆŗĶĘÆ°×·Ū³£ÓĆÓŚ×ŌĄ“Ė®µÄ¾»»Æ£¬µ«Į½ÕßµÄ×÷ÓĆŌĄķ²»ĻąĶ¬ | |
| C£® | Ź³Ę·°ü×°“üÖŠ³£·ÅČėŠ”“üµÄÉśŹÆ»Ņ£¬ÄæµÄŹĒ·ĄÖ¹Ź³Ę·Ńõ»Æ±äÖŹ | |
| D£® | ĻĖĪ¬ĖŲŌŚČĖĢåÄŚæÉĖ®½āĪŖĘĻĢŃĢĒ£¬¹ŹæÉ×÷ČĖĄąµÄÓŖŃųĪļÖŹ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŠĪ³É»Æѧ¼ü | B£® | ĒāĘųČ¼ÉÕ | C£® | ĀĮČČ·“Ó¦ | D£® | µē½āČŪČŚĀČ»ÆÄĘ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·“Ó¦ŗóČÜŅŗÖŠ²»“ęŌŚČĪŗĪ³Įµķ£¬ĖłŅŌ·“Ó¦Ē°ŗóZn2+µÄÅØ¶Č²»±ä | |
| B£® | ³ĮµķČܽāŗ󣬽«Éś³ÉÅäŗĻĄė×Ó[Zn£ØNH3£©4]2+ | |
| C£® | ÓĆĻõĖįŠæČÜŅŗ“śĢęĮņĖįŠæČÜŅŗ½ųŠŠŹµŃ飬ÄܹŪ²ģµ½Ķ¬ŃłµÄĻÖĻó | |
| D£® | ŌŚ[Zn£ØNH3£©4]2+Ąė×ÓÖŠ£¬NH3øų³ö¹Ā¶Ōµē×Ó£¬Zn2+Ģį¹©æÕ¹ģµĄ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
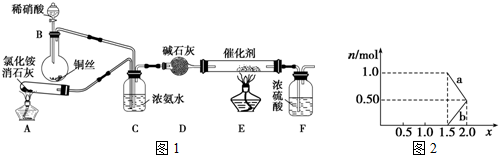
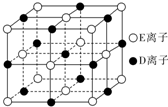 A”¢B”¢C”¢D”¢E”¢FĪŖĒ°ĖÄÖÜĘŚŌŖĖŲĒŅŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬ĘäÖŠAŗ¬ÓŠ3øöÄܼ¶£¬ĒŅĆæøöÄܼ¶Ėłŗ¬µÄµē×ÓŹżĻąĶ¬£»CµÄ×īĶā²ćÓŠ6øöŌĖ¶ÆדĢ¬²»Ķ¬µÄµē×Ó£»DŹĒ¶ĢÖÜĘŚŌŖĖŲÖŠµēøŗŠŌ×īŠ”µÄŌŖĖŲ£»EµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļĖįŠŌ×īĒ棻F³ż×īĶā²ćŌ×Ó¹ģµĄ“¦ÓŚ°ė³äĀś×“Ģ¬£¬ĘäÓąÄÜ²ć¾ł³äĀśµē×Ó£®GŌŖĖŲÓėDŌŖĖŲĶ¬Ö÷×壬ĒŅĻą²ī3øöÖÜĘŚ£®
A”¢B”¢C”¢D”¢E”¢FĪŖĒ°ĖÄÖÜĘŚŌŖĖŲĒŅŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬ĘäÖŠAŗ¬ÓŠ3øöÄܼ¶£¬ĒŅĆæøöÄܼ¶Ėłŗ¬µÄµē×ÓŹżĻąĶ¬£»CµÄ×īĶā²ćÓŠ6øöŌĖ¶ÆדĢ¬²»Ķ¬µÄµē×Ó£»DŹĒ¶ĢÖÜĘŚŌŖĖŲÖŠµēøŗŠŌ×īŠ”µÄŌŖĖŲ£»EµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļĖįŠŌ×īĒ棻F³ż×īĶā²ćŌ×Ó¹ģµĄ“¦ÓŚ°ė³äĀś×“Ģ¬£¬ĘäÓąÄÜ²ć¾ł³äĀśµē×Ó£®GŌŖĖŲÓėDŌŖĖŲĶ¬Ö÷×壬ĒŅĻą²ī3øöÖÜĘŚ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 12ÖÖ | B£® | 10ÖÖ | C£® | 8ÖÖ | D£® | 6ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na2SiO3Ė®ČÜŅŗĖ׳ĘĖ®²£Į§£¬æÉÓĆ×÷ľ²Ä·Ą»š¼Į | |
| B£® | Fe3O4Ė׳ĘĢśŗģ£¬æÉÓĆ×÷ŗģÉ«ĶæĮĻ | |
| C£® | Na2CO3Ė×³Ę“æ¼ī£¬æÉ×÷ĪŖÖĘŌģ²£Į§µÄŌĮĻ | |
| D£® | KAl£ØSO4£©2•12H2OĖ׳ĘĆ÷·Æ£¬æÉ×÷ĪŖ¾»Ė®¼Į |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
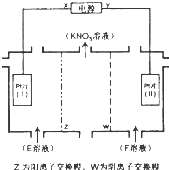
| A£® | XĪŖøŗ¼«£¬FČÜŅŗNaNO3ČÜŅŗ | |
| B£® | µē½āŅ»¶ĪŹ±¼ä£¬ĶłPtʬ£ØI£©ø½½üµĪČė·ÓĢŖ£¬ČÜŅŗ±äŗģ | |
| C£® | µē½ā×Ü·“Ó¦·½³ĢŹ½ĪŖ£ŗ2H2O$\frac{\underline{\;µē½ā\;}}{\;}$2H2”ü+O2”ü | |
| D£® | ĄķĀŪÉĻ£¬µ±µĆµ½0.1molKNO3Ź±£¬Ptʬ£Ø¢ņ£©ÉĻÉś³É±ź×¼×“æöĻĀĪŖ1.12LµÄĘųĢå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com