
”¾ĢāÄæ”æ»ÆŗĻĪļWŹĒŅ©ĪļŗĻ³ÉµÄÖŠ¼äĢ壬ĖüµÄŅ»ÖÖŗĻ³ÉĀ·ĻßČēĻĀ£ŗ

»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)ŹŌ¼ĮaŹĒ___________”£
(2)AµÄĆū³ĘŹĒ___________£»FÖŠ¹ŁÄÜĶŵÄĆū³ĘŹĒ___________”£
(3)ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ___________(ĢīÕżČ·Ń”Ļī±ąŗÅ)”£
a£®CH2= CHCHO²»“ęŌŚĖ³·“Ņģ¹¹Ģå b£®DÄÜ·¢ÉśĖ®½ā·“Ó¦
c£®EµÄ·Ö×ÓŹ½ĪŖC9H14NO2 d£®¢ą·¢ÉśĮĖ»¹Ō·“Ó¦
(4)·“Ó¦¢ŪµÄ»Æѧ·½³ĢŹ½ŹĒ___________”£
(5)G(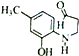 )ÓŠ¶ąÖÖĶ¬·ÖŅģ¹¹Ģ唣ŹōÓŚ¶”Ėįõ„ĒŅ±½»·ÉĻŗ¬Ņ»NH2µÄĶ¬·ÖŅģ¹¹ĢåÓŠ___________ÖÖ£¬ĘäÖŠŗĖ“Ź²ÕńĒāĘ×ĻŌŹ¾ĪŖ6×é·å£¬ĒŅ·åĆ껿֮±ČĪŖ3£ŗ2£ŗ2£ŗ2£ŗ2£ŗ2µÄ½į¹¹¼ņŹ½ĪŖ___________”£
)ÓŠ¶ąÖÖĶ¬·ÖŅģ¹¹Ģ唣ŹōÓŚ¶”Ėįõ„ĒŅ±½»·ÉĻŗ¬Ņ»NH2µÄĶ¬·ÖŅģ¹¹ĢåÓŠ___________ÖÖ£¬ĘäÖŠŗĖ“Ź²ÕńĒāĘ×ĻŌŹ¾ĪŖ6×é·å£¬ĒŅ·åĆ껿֮±ČĪŖ3£ŗ2£ŗ2£ŗ2£ŗ2£ŗ2µÄ½į¹¹¼ņŹ½ĪŖ___________”£
(6)  ŹĒÖĘŅ©ÖŠ¼äĢ壬½įŗĻĢāÖŠĮ÷³ĢŗĶŅŃѧÖŖŹ¶Éč¼ĘÓÉDĪŖĘšŹ¼ŌĮĻŗĻ³É
ŹĒÖĘŅ©ÖŠ¼äĢ壬½įŗĻĢāÖŠĮ÷³ĢŗĶŅŃѧÖŖŹ¶Éč¼ĘÓÉDĪŖĘšŹ¼ŌĮĻŗĻ³É µÄŗĻ³ÉĀ·ĻßĶ¼£ŗ___________(ĪŽ»śŹŌ¼ĮČĪŃ”)”£
µÄŗĻ³ÉĀ·ĻßĶ¼£ŗ___________(ĪŽ»śŹŌ¼ĮČĪŃ”)”£
”¾“š°ø”æÅØĮņĖį”¢ÅØĻõĖį ¶ŌĻõ»ł¼×±½ ōĒ»ł”¢°±»ł ab 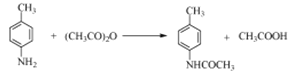 6
6 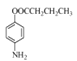

»ņ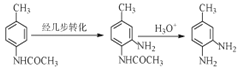
”¾½āĪö”æ
ÓÉŗĻ³ÉĀ·ĻßæÉÖŖ£¬¼×±½ŗĶÅØĮņĖį”¢ÅØĻõĖį¼ÓČČ·¢ÉśĻõ»Æ·“Ó¦¾·ÖĄėµĆµ½¶ŌĻõ»ł¼×±½£»¶ŌĻõ»ł¼×±½ŌŚĢśŗĶŃĪĖįµÄĢõ¼žĻĀ£¬·¢Éś»¹Ō·“Ӧɜ³É¶Ō¼×»ł±½°·£»¶Ō¼×»ł±½°·ŗĶŅŅĖįōū·“Ó¦µĆµ½D£¬D¾¼ø²æ×Ŗ»ÆµĆµ½E£»E¾·“Ó¦¢Ż×Ŗ»ÆĪŖF£»F![]() GŹĒF·Ö×ÓÖŠµÄ-NH2ÓėH2C=CH-CHO·¢ÉśµÄ¼Ó³É·“Ó¦£»G”śQŹĒĻČ¼Ó³ÉŌŁĻūČ„£»×īŗóQ”śW·¢ÉśĻūČ„·“Ó¦µĆµ½W£¬¾Ż“Ė·ÖĪö½ā“š”£
GŹĒF·Ö×ÓÖŠµÄ-NH2ÓėH2C=CH-CHO·¢ÉśµÄ¼Ó³É·“Ó¦£»G”śQŹĒĻČ¼Ó³ÉŌŁĻūČ„£»×īŗóQ”śW·¢ÉśĻūČ„·“Ó¦µĆµ½W£¬¾Ż“Ė·ÖĪö½ā“š”£
(1)øł¾ŻŗĻ³ÉĀ·ĻßĖłøųŠÅĻ¢£¬·“Ó¦¢ŁĪŖ¼×±½ŗĶÅØĮņĖį”¢ÅØĻõĖį¼ÓČČ·¢ÉśĻõ»Æ·“Ó¦£¬ĖłŅŌŹŌ¼ĮaŹĒÅØĮņĖį”¢ÅØĻõĖį£¬
¹Ź“š°øŹĒ£ŗÅØĮņĖį”¢ÅØĻõĖį£»
(2)ÓÉAµÄ½į¹¹¼ņŹ½æÉÖŖ£¬AµÄĆū³ĘŹĒ¶ŌĻõ»ł¼×±½£»FÖŠ¹ŁÄÜĶŵÄĆū³ĘŹĒōĒ»ł”¢°±»ł£¬
¹Ź“š°øŹĒ£ŗ¶ŌĻõ»ł¼×±½£»ōĒ»ł”¢°±»ł£»
(3) a£®CH2= CHCHO·Ö×ÓÖŠĘäÖŠµÄ1øöĢ¼Ō×ÓĮ¬ÓŠĮ½øöĒāŌ×Ó£¬ĖłŅŌ²»“ęŌŚĖ³·“Ņģ¹¹Ģ壬¹ŹaÕżČ·£»
b£®DµÄ½į¹¹¼ņŹ½ĪŖ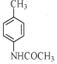 £¬·Ö×ÓÖŠŗ¬ÓŠ-NHCO-£¬ĖłŅŌÄÜ·¢ÉśĖ®½ā·“Ó¦£¬¹ŹbÕżČ·£»
£¬·Ö×ÓÖŠŗ¬ÓŠ-NHCO-£¬ĖłŅŌÄÜ·¢ÉśĖ®½ā·“Ó¦£¬¹ŹbÕżČ·£»
c£®EµÄ½į¹¹¼ņŹ½ĪŖ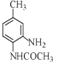 ·Ö×ÓŹ½ĪŖC9H12NO£¬¹Źc“ķĪó£»
·Ö×ÓŹ½ĪŖC9H12NO£¬¹Źc“ķĪó£»
d£®·“Ó¦¢ą·¢ÉśĮĖQ”śW·Ö×ÓÄŚµÄĻūČ„·“Ó¦µĆµ½W£¬Ņ²ŹōÓŚČ„ĒāŃõ»Æ·“Ó¦£¬¹Źd“ķĪó£»
¹Ź“š°øŹĒ£ŗab£»
(4)·“Ó¦¢ŪŹĒ¶Ō¼×»ł±½°·ŗĶŅŅĖįōū·“Ó¦µĆµ½D£¬»Æѧ·½³ĢŹ½ŹĒ £¬
£¬
¹Ź“š°øŹĒ£ŗ £»
£»
(5)G(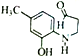 )·Ö×ÓÖŠŗ¬ÓŠČ©»ł°±»łŗĶōĒ»ł£¬Ķ¬·ÖŅģ¹¹ĢåŹōÓŚ¶”Ėįõ„ĒŅ±½»·ÉĻŗ¬Ņ»NH2µÄĶ¬·ÖŅģ¹¹ĢåÓŠ£ŗ-NH2ÓėCH3CH2CH2CO-”¢£ØCH3£©2CH CO-·Ö±š“¦ÓŚĮŚ”¢¼ä”¢¶Ōø÷3ÖÖ£¬¹²6ÖÖ£»
)·Ö×ÓÖŠŗ¬ÓŠČ©»ł°±»łŗĶōĒ»ł£¬Ķ¬·ÖŅģ¹¹ĢåŹōÓŚ¶”Ėįõ„ĒŅ±½»·ÉĻŗ¬Ņ»NH2µÄĶ¬·ÖŅģ¹¹ĢåÓŠ£ŗ-NH2ÓėCH3CH2CH2CO-”¢£ØCH3£©2CH CO-·Ö±š“¦ÓŚĮŚ”¢¼ä”¢¶Ōø÷3ÖÖ£¬¹²6ÖÖ£»
ĘäÖŠŗĖ“Ź²ÕńĒāĘ×ĻŌŹ¾ĪŖ6×é·å£¬ĒŅ·åĆ껿֮±ČĪŖ3£ŗ2£ŗ2£ŗ2£ŗ2£ŗ2µÄ½į¹¹¼ņŹ½ĪŖ £¬
£¬
¹Ź“š°øŹĒ£ŗ6£» £»
£»
(6) øł¾ŻĢāÖŠĮ÷³Ģ£¬ČōŅŖÓÉ ĪŖĘšŹ¼ŌĮĻŗĻ³É
ĪŖĘšŹ¼ŌĮĻŗĻ³É ŌņŠčŅŖĻČ·¢ÉśĻõ»Æ·“Ó¦ŅżČė-NO2£¬ŌŁ»¹ŌĪŖ°±»ł£¬×īŗóĖ®½āµĆµ½²śĪļ
ŌņŠčŅŖĻČ·¢ÉśĻõ»Æ·“Ó¦ŅżČė-NO2£¬ŌŁ»¹ŌĪŖ°±»ł£¬×īŗóĖ®½āµĆµ½²śĪļ £¬ŗĻ³ÉĀ·ĻßĶ¼Éč¼ĘĪŖ£ŗ
£¬ŗĻ³ÉĀ·ĻßĶ¼Éč¼ĘĪŖ£ŗ £¬»ņĄūÓĆĢāøųŠÅĻ¢Éč¼ĘĪŖ£ŗ
£¬»ņĄūÓĆĢāøųŠÅĻ¢Éč¼ĘĪŖ£ŗ £¬
£¬
¹Ź“š°øŹĒ£ŗ »ņ
»ņ ”£
ӣ



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚŅ»øö¾ųČȶØČŻµÄĆܱÕČŻĘ÷ÖŠ£¬1molA Óė 2molB ·¢Éś·“Ó¦ A(g)£«2B(g) ![]() xC(g)£«2D(g) ”÷H£½bkJ”¤mol1(b£¼0)£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
xC(g)£«2D(g) ”÷H£½bkJ”¤mol1(b£¼0)£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A. ³ä·Ö·“Ó¦ŗ󣬷ųöČČĮæĪŖ b kJ
B. Čō x=1£¬ČŻĘ÷ÖŠŃ¹Ēæ²»±äŹ±²»ÄÜÅŠ¶Ļ·“Ó¦“ļµ½Ę½ŗā
C. µ± B ŗĶ D µÄĪļÖŹµÄĮæĪŖ 1:1 Ź±£¬±ķĆ÷øĆ·“Ó¦ŅŃ“ļµ½Ę½ŗā
D. “ļµ½Ę½ŗā¹ż³ĢÖŠ£¬Õż·“Ó¦ĖŁĀŹæÉÄÜŹĒĻČŌö“óŌŁ¼õŠ”
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČżĀČĒā¹č(SiHCl3)ŹĒÖʱø¹čĶ锢¶ą¾§¹čµÄÖŲŅŖŌĮĻ”£»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)SiHCl3ŌŚ³£ĪĀ³£Ń¹ĻĀĪŖŅ×»Ó·¢µÄĪŽÉ«ĶøĆ÷ŅŗĢ壬Óö³±ĘųŹ±·¢ŃĢÉś³É(HSiO)2OµČ£¬Š“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½_______________________________”£
(2)SiHCl3ŌŚ“߻ƼĮ×÷ÓĆĻĀ·¢Éś·“Ó¦£ŗ
2SiHCl3(g)=SiH2Cl2(g)+ SiCl4(g) ¦¤H1= +48 kJ”¤mol1
3SiH2Cl2(g)=SiH4(g)+2SiHCl3 (g) ¦¤H2= 30 kJ”¤mol1
Ōņ·“Ó¦4SiHCl3(g)=SiH4(g)+ 3SiCl4(g)µÄ¦¤H=__________ kJ”¤mol1”£
(3)¶ŌÓŚ·“Ó¦2SiHCl3(g)![]() SiH2Cl2(g)+SiCl4(g)£¬²ÉÓĆ“óæ×Čõ¼īŠŌŅõĄė×Ó½»»»Ź÷Ö¬“߻ƼĮ£¬ŌŚ323 KŗĶ343 KŹ±SiHCl3µÄ×Ŗ»ÆĀŹĖꏱ¼ä±ä»ÆµÄ½į¹ūČēĶ¼ĖłŹ¾”£
SiH2Cl2(g)+SiCl4(g)£¬²ÉÓĆ“óæ×Čõ¼īŠŌŅõĄė×Ó½»»»Ź÷Ö¬“߻ƼĮ£¬ŌŚ323 KŗĶ343 KŹ±SiHCl3µÄ×Ŗ»ÆĀŹĖꏱ¼ä±ä»ÆµÄ½į¹ūČēĶ¼ĖłŹ¾”£
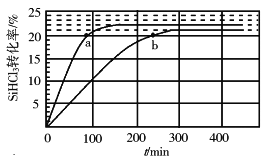
¢Ł343 KŹ±·“Ó¦µÄĘ½ŗā×Ŗ»ÆĀŹ¦Į=_________%”£Ę½ŗā³£ŹżK343 K=__________(±£Įō2Ī»Š”Źż)”£
¢ŚŌŚ343 KĻĀ£ŗŅŖĢįøßSiHCl3×Ŗ»ÆĀŹ£¬æɲÉČ”µÄ“ėŹ©ŹĒ___________£»ŅŖĖõ¶Ģ·“Ó¦“ļµ½Ę½ŗāµÄŹ±¼ä£¬æɲÉČ”µÄ“ėŹ©ÓŠ____________”¢___________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŠĀŠĶļ®æÕĘųµē³ŲÄÜĮæĆܶČøß”¢³É±¾µĶ£¬æÉ×÷ĪŖĪ“Ą“µē¶ÆĘū³µµÄ¶ÆĮ¦Ō“£¬Ę乤×÷ŌĄķČēÓŅĶ¼ĖłŹ¾”£ĻĀĮŠÓŠ¹ŲøƵē³ŲµÄĖµ·ØÕżČ·µÄŹĒ

A. ³äµēŹ±£¬½šŹōļ®ĪŖŃō¼«
B. ·ÅµēŹ±£¬ÕżøŗĮ½¼«ÖÜĪ§¶¼ÓŠLiOH
C. ·ÅµēŹ±£¬ĆæĻūŗÄ22.4LO2£¬×ŖŅĘ4molµē×Ó
D. ·ÅµēŗĶ³äµēŹ±£¬Li+ĒØŅĘ·½ĻņĻą·“
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĢś¼°Ęä»ÆŗĻĪļŌŚČĖĄąµÄÉś»īÉś²śÖŠÓŠ×ÅÖŲŅŖµÄ×÷ÓĆ£¬Fe2+”¢Fe3+ŹĒÓ°ĻģĖ®ÖŹµÄŅ»øöÖŲŅŖŅņĖŲ”£»Ų“šĻĀĮŠĪŹĢā£ŗ
I£ŗ²āĮæijŗÓĖ®Ńł±¾ÖŠĢśµÄŗ¬Įæ
(1)Ė®ŃłÖŠFe2+µÄŗ¬ĮæŌ½“ó£¬ČܽāŃõµÄŗ¬Įæ¾ĶŌ½µĶ£¬ÓĆĄė×Ó·½³ĢŹ½½āŹĶŌŅņ___________”£
(2)²ā¶ØFe2+Č”5mL c mo/LµÄKMnO4±ź×¼Ņŗ£¬Ļ”ŹĶÖĮ100mL”£Č”10.00mLŗÓĖ®Ė®Ńł£¬¼ÓČėĻ”ĮņĖįŗó£¬ÓĆĻ”ŹĶŗóµÄKMnO4ČÜŅŗ½ųŠŠµĪ¶Ø£¬ÓĆČ„KMnO4ČÜŅŗV1mL”£
¢ŁÓĆ___________(ĢīµĪ¶Ø¹ÜµÄĆū³Ę)Ź¢·ÅKMnO4±ź×¼Ņŗ”£
¢ŚµĪ¶Ø“ļµ½ÖÕµćµÄ±źÖ¾ŹĒ___________”£
(3)²ā¶ØFe3+£ŗČ”10.00mLĖ®Ńł£¬×ŖŅĘÖĮŹ¢ÓŠ¹żĮæŠæĮ£µÄÉÕ±ÖŠ³ä·Ö·“Ó¦”£¼ÓČė¹żĮæĻ”ĮņĖį£¬ÓƱķĆęĆóøĒ×”ÉÕ±²¢¼ÓČČ10·ÖÖÓ”£ĄäČ“ŗóÓĆ(2)ÖŠĻ”ŹĶŗóµÄKMnO4ČÜŅŗµĪ¶Ø£¬ĻūŗÄKMnO4ČÜŅŗV2mL”£
¢ŁŠæĮ£µÄ×÷ÓĆŹĒ___________”£
¢ŚŗÓĖ®ÖŠFe3+µÄÅØ¶ČŹĒ___________mol/L(ÓĆŗ¬×ÖÄøµÄ“śŹżŹ½±ķŹ¾)”£
¢ņ£ŗĒāŃõ»ÆŃĒĢś[Fe(OH)2]ŌŚ³£ĪĀ³£Ń¹ĻĀĪŖ°×É«¹ĢĢ唣
(4)µ±ČÜŅŗÖŠµÄĄė×ÓÅضČ<1”Į10£5mol”¤L£1Ź±£¬æÉŅŌČĻĪŖøĆĄė×ÓŅŃ³ĮµķĶźČ«”£ŅŃÖŖ³£ĪĀFe(OH)2µÄKspĪŖ8.0”Į10£16”£ĻÖµ÷½Śŗ¬Fe2+µÄijŗÓĖ®ŃłĘ·pH=9£¬ÓĆ¼ņŅŖ¼ĘĖć¹ż³ĢĖµĆ÷Fe2+ŹĒ·ńŅŃ¾“ļµ½³ĮµķĶźČ«£ŗ___________”£
(5)Ņ»ÖÖÓĆNa2SO4ČÜŅŗ×öµē½āŅŗ£¬µē½āÖĘČ”Fe(OH)2µÄŹµŃé×°ÖĆČēĶ¼ĖłŹ¾”£Ķصēŗó£¬ČÜŅŗÖŠ²śÉś°×É«³Įµķ£¬ĒŅ½Ļ³¤Ź±¼ä²»±äÉ«”£

¢Ł±ŲŠėŹ¹ÓĆĢśµē¼«µÄŹĒ___________(Ģī”°A"»ņ”°B”±)¼«”£
¢ŚBµē¼«µÄµē¼«·“Ó¦Ź½ĪŖ___________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøł¾ŻÄÜĮæ¹ŲĻµĶ¼£¬ĻĀĮŠ·ÖĪöÕżČ·µÄŹĒ

A. øĆ·“Ó¦ŹĒĪüČČ·“Ó¦
B. ĒśĻßaµÄČČŠ§Ó¦“ó
C. øĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗ4HCl + O2 ”ś 2Cl2 +2H2O + 115.6 kJ
D. Čō·“Ӧɜ³É2molŅŗĢ¬Ė®£¬·Å³öµÄČČĮæøßÓŚ115.6kJ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æäå»ÆÄĘ”¢ĀČ»ÆÄĘŗĶŃõ»ÆĆ¾µČĄė×Ó¾§ĢåµÄŗĖ¼ä¾ąŗĶ¾§øńÄÜ(²æ·Ö)ČēĻĀ±ķĖłŹ¾

£Ø1£©äå»ÆÄĘ¾§Ģå±ČĀČ»ÆÄĘ¾§Ģ徧øńÄÜ________(Ģī”°“ó”±»ņ”°Š””±)£¬Ö÷ŅŖŌŅņŹĒ_____”£
£Ø2£©Ńõ»ÆĆ¾¾§Ģå±ČĀČ»ÆÄĘ¾§Ģ徧øńÄÜ“ó£¬Ö÷ŅŖŌŅņŹĒ_________________________________”£
£Ø3£©äå»ÆÄĘ”¢ĀČ»ÆÄĘŗĶŃõ»ÆĆ¾¾§ĢåÖŠ£¬Ó²¶Č×ī“óµÄŹĒ________”£¹¤ŅµÖĘČ”µ„ÖŹĆ¾Ź±£¬ĶłĶłµē½āµÄŹĒĀČ»ÆĆ¾¶ų²»ŹĒŃõ»ÆĆ¾£¬Ö÷ŅŖŌŅņŹĒ_______________________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ³£ĪĀŹ±HClOµÄKa=3.0”Į10-8£¬HFµÄKa=3.5”Į10-4”£ĻÖ½«pHŗĶĢå»ż¶¼ĻąĶ¬µÄ“ĪĀČĖįŗĶĒā·śĖįČÜŅŗ·Ö±š¼ÓÕōĮóĖ®Ļ”ŹĶ£¬pHĖęČÜŅŗĢå»żµÄ±ä»ÆČēĶ¼ĖłŹ¾”£ĻĀĮŠŠšŹöÕżČ·µÄŹĒ

A. ĒśĻßIĪŖ“ĪĀČĖįĻ”ŹĶŹ±pH±ä»ÆĒśĻß
B. Č”aµćµÄĮ½ÖÖĖįČÜŅŗ£¬ÖŠŗĶĻąĶ¬Ģå»ż”¢ĻąĶ¬ÅØ¶ČµÄNaOHČÜŅŗ£¬ĻūŗÄ“ĪĀČĖįµÄĢå»ż½ĻŠ”
C. aµćŹ±£¬Čō¶¼¼ÓČėĻąĶ¬“󊔵ĊæĮ££¬“ĖŹ±ÓėĒā·śĖį·“Ó¦µÄĖŁĀŹ“ó
D. bµćČÜŅŗÖŠĖ®µÄµēĄė³Ģ¶Č±ČcµćČÜŅŗÖŠĖ®µÄµēĄė³Ģ¶ČŠ”
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŃŠ¾æ»Æѧ·“Ó¦Ź±£¬¼ČŅŖæ¼ĀĒĪļÖŹ±ä»ÆÓėÄÜĮæ±ä»Æ£¬ÓÖŅŖ¹Ų×¢·“Ó¦µÄæģĀżÓėĻŽ¶Č”£»Ų“šĻĀĮŠĪŹĢā:
(1)NH3»¹ŌNOŹĒÖŲŅŖµÄŃĢĘųĶŃĻõ¼¼Źõ£¬Ęä·“Ó¦¹ż³ĢÓėÄÜĮæ¹ŲĻµČēĶ¼ĖłŹ¾

¢ŁÉĻĶ¼ÖŠŅņĪŖøıäĮĖ·“Ó¦Ģõ¼ž£¬·“Ó¦µÄ»ī»ÆÄÜ£ŗb_______(Ģī”°£¾”±”°£¼£¢»ņ”°£½”±)a”£
¢ŚĶŃĻõ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½æɱķŹ¾ĪŖ·“Ó¦Īļ”śÉś³ÉĪļ”÷H£½______(ÓĆE1”¢E2µÄ“śŹżŹ½±ķŹ¾)”£
¢ŪŃŠ¾æ·¢ĻÖ£¬Ņ»¶ØĢõ¼žĻĀµÄĶŃĻõ·“Ó¦¹ż³ĢæÉÄÜČēĶ¼ĖłŹ¾£¬øł¾ŻŃõ»Æ»¹Ō·“Ó¦ÖŠĪļÖŹµÄ×÷ÓĆ£¬NOĪŖ_______¼Į£¬ĶŃĻõ×Ü·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_______________”£

(2)Ņ»¶ØĪĀ¶ČĻĀ£¬½«²»Ķ¬ĪļÖŹµÄĮæµÄH2O(g)ŗĶCO·Ö±šĶØČėČŻ»żĪŖ1LµÄŗćČŻĆÜČŻĘ÷ÖŠ£¬½ųŠŠ·“Ó¦H2O(g)£«CO(g)![]() CO2(g)£«H2(g)£¬µĆµ½Čē±ķĖłŹ¾µÄČż×鏿¾Ż
CO2(g)£«H2(g)£¬µĆµ½Čē±ķĖłŹ¾µÄČż×鏿¾Ż
ŹŌŃ鱹ŗÅ | ĪĀ¶Č/”ę | ĘšŹ¼Įæ/mol | Ę½ŗāĮæ/mol | “ļµ½Ę½ŗāŹ±¼ä/min | ||
H2O(g) | CO(g) | CO(g) | H2(g) | |||
1 | 650 | 2.0 | 4.0 | 3.0 | 1.0 | 5 |
2 | 900 | 1.0 | 2.0 | 1.8 | 0.2 | 4 |
3 | 900 | a | b | c | d | t |
¢Ł4mimÄŚ£¬ŹµŃé2ÖŠv(CO2)£½______£» 900”ꏱ£¬·“Ó¦µÄĘ½ŗā³£ŹżĪŖ______£»½µµĶĪĀ¶ČŹ±£¬Ę½ŗā³£Źż»į________(Ģī”°Ōö“ó”±”°¼õŠ””±»ņ”°²»±ä”±)”£
¢Ś650”ꏱ£¬ČōŌŚ“ĖČŻĘ÷ÖŠ³äČė2.0 mol H2O(g)”¢1.0molCO(g)”¢1.0 mol CO2(g)ŗĶ xmol H2(g)£¬ŅŖŹ¹·“Ó¦ŌŚæŖŹ¼Ź±ĻņÕż·“Ó¦·½Ļņ½ųŠŠ£¬ŌņxÓ¦Āś×ćµÄĢõ¼žŹĒ__________”£
Čōa£½2.0£®b£½1.0£¬ŌņĘ½ŗāŹ±ŹµŃé2ÖŠH2O(g)ŗĶŹµŃé3ÖŠCO(g)µÄ×Ŗ»ÆĀŹ(a)µÄ¹ŲĻµĪŖa(H2O) _______ (Ģī”°£¾”±£¼”±³É£½”±)a(CO)”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com