
| A、该混盐水溶液呈碱性 |
| B、该混盐溶液加入BaCl2可以生成白色沉淀 |
| C、该混盐与H2SO4反应有气体生成 |
| D、该混盐在酸性条件下可生成S,每产生1molS转移1.5NA个电子 |
| 4 |
| 3 |


科目:高中化学 来源: 题型:
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、10mL 0.1mol?L-1氨水与10mL 0.1mol?L-1盐酸溶液混合,c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| B、10mL 0.1mol?L-1NH4Cl溶液与5mL 0.2 mol?L-1NaOH盐酸混合,c(Na+)=c(Cl-)>c(OH-)>c(H+) |
| C、10mL 0.5mol?L-1CH3COONa溶液与6mL 1mol?L-1盐酸混合,c(Cl-)>c(Na+)>c(OH-)>c(H+) |
| D、c(NH4+)相等的(NH4)2SO4溶液、(NH4)2CO3溶液和NH4Cl溶液中,c[(NH4)2SO4]<c(NH4Cl)<c[(NH4)2CO3] |
查看答案和解析>>
科目:高中化学 来源: 题型:
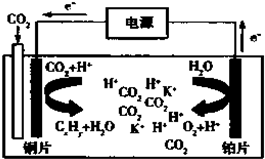 如图为CO2电催化还原为碳氢化合物的工作原理示意图,用一种钾盐水溶液作电解液.下列说法不正确的是( )
如图为CO2电催化还原为碳氢化合物的工作原理示意图,用一种钾盐水溶液作电解液.下列说法不正确的是( )| A、工作时,铜片作阴极 |
| B、工作时,K+向铜片电极移动 |
| C、工作时,铂片上的电极反应式为4OH--4e-=O2↑+2H2O |
| D、若CxHy为C2H4,则生成1 mol C2H4的同时生成2 molO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
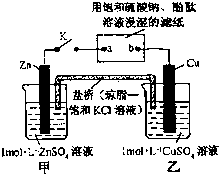
| A、盐桥中的Cl-向乙烧杯方向移动 |
| B、盐桥中有电子通过 |
| C、乙中的铜棒逐渐变细 |
| D、片刻后可观察到滤纸a点变红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、实验中使用的主要仪器是分液漏斗 |
| B、溴在四氯化碳中的溶解度比在水中的溶解度大 |
| C、不可把萃取剂四氯化碳换成酒精 |
| D、分液时,水及溴的四氯化碳溶液均从分液漏斗下口流出 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com