
 ��2L�ܱ������ڣ�800��ʱ��Ӧ��2NO��g��+O2��g���T2NO2��g����ϵ�У�n��NO����ʱ��ı仯�����
��2L�ܱ������ڣ�800��ʱ��Ӧ��2NO��g��+O2��g���T2NO2��g����ϵ�У�n��NO����ʱ��ı仯�����| ʱ�䣨s�� | 0 | 1 | 2 | 3 | 4 | 5 |
| n��NO����mol�� | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
���� ��1��ƽ�ⳣ��K=$\frac{������ƽ��ʱŨ����֮��}{��Ӧ��ƽ��ʱŨ����֮��}$��800�棬��3s��4s��5sʱNO�����ʵ�����0.007mol��˵�����淴Ӧ�ﵽƽ�⣬c��NO��=$\frac{n}{V}$�������¶ȣ�NO��Ũ������˵��ƽ�������ƶ������淽�������ȷ�Ӧ���������Ƿ��ȷ�Ӧ��
��2������һ���������ʵ����ı仯֪���÷�Ӧ������Ӧ�����ƶ�����������������ʵ����ڲ��������ڷ�Ӧ��ʼʱc��NO��=0.01mol/L����ƽ��ʱc��NO��=0.003 5 mol/L����c��NO��=0.0065mol/L�����ݷ�Ӧ����ʽ��֪��c��NO2��=��c��NO��������v=$\frac{��c}{��t}$����v��NO��������������֮�ȵ��ڻ�ѧ������֮�ȼ���v��O2����
��3�����淴Ӧ����ƽ��ʱ��ͬ�����ʵ�����������ȣ�����ֵ�Ũ�ȡ��������ֲ��䣬�ɴ�����������һЩ�����䣬�ж�ƽ���������Ӧ�淴Ӧ���з����仯�����������ɱ仯�����仯˵������ƽ�⣻
��4��Ϊʹ�÷�Ӧ�ķ�Ӧ�������ɲ�������ѹǿ�������¶ȡ��������������Ӧ��Ũ�ȵȷ������ٽ��ƽ���ƶ�ԭ���������
��5�����ݸ�˹���ɽ��⣮
��� �⣺��1��ƽ�ⳣ��K=$\frac{������ƽ��ʱŨ����֮��}{��Ӧ��ƽ��ʱŨ����֮��}$=$\frac{{c}^{2}��N{O}_{2}��}{{c}^{2}��NO��•c��{O}_{2}��}$��800�棬��3s��4s��5sʱNO�����ʵ������ֲ�����0.007mol��˵�����淴Ӧ�ﵽƽ�⣬c��NO��=$\frac{n}{V}$=$\frac{0.007mol}{2L}$=0.0035mol/L�������¶ȣ�NO��Ũ������˵��ƽ�������ƶ������淽�������ȷ�Ӧ���������Ƿ��ȷ�Ӧ��
�ʴ�Ϊ��$\frac{{c}^{2}��N{O}_{2}��}{{c}^{2}��NO��•c��{O}_{2}��}$��0.0035mol/L���ţ�
��2������һ���������ʵ����ı仯֪���÷�Ӧ������Ӧ�����ƶ�����������������ʵ����ڲ��������ڷ�Ӧ��ʼʱc��NO��=0.01mol/L����ƽ��ʱc��NO��=0.003 5 mol/L����c��NO��=0.0065mol/L�����ݷ�Ӧ����ʽ��֪��c��NO2��=��c��NO�������ʾNO2�仯��������b���ڷ�Ӧ��ʼʱc��NO��=0.01mol/L��2sʱc��NO��=$\frac{0.008mol}{2L}$=0.004mol/L����c��NO��=0.006mol/L����v��NO��=$\frac{0.006mol/L}{2s}$=0.003mol/��L•s��������֮�ȵ��ڻ�ѧ������֮�ȣ�v��O2��=$\frac{1}{2}$v��NO��=0.0015mol/��L•s����
�ʴ�Ϊ��b��0.0015mol/��L•s����1.5��10-3 mol/��L•s����
��3��a������Ӧ�ﵽƽ�⣬��v��NO2����=2v��O2�������������ʵ�������δָ������˲����жϷ�Ӧ�Ƿ�ﵽƽ�⣬��a����
b�����ڸ÷�Ӧ�Ƿ�Ӧǰ������������ȵķ�Ӧ��������������ѹǿ���ֲ��䣬��Ӧ�ﵽƽ�⣬��b��ȷ��
c��v����NO��=2v����O2������ͬ�������ʼ�Ĺ�ϵ���㷽���෴������֮�ȵ��ڼ�����֮�ȣ�˵������Ӧ���ʵ����淴Ӧ���ʣ�NO��O2��Ũ�Ȳ��䣬��Ӧ�ﵽƽ�⣬��c��ȷ��
d���������������������������������ֲ��䣬���ܶ�ʼ�ձ��ֲ��䣬���ܶȲ���ʱ����һ���ﵽƽ�⣬��d����
�ʴ�Ϊ��bc��
��4��a����ʱ�����NO2����ƽ�������ƶ�������Ӧ���ʼ�С����a����
b���ʵ������¶ȣ���Ӧ��������ƽ�����淴Ӧ�����ƶ�����b����
c������O2��Ũ�ȷ�Ӧ���������Ҹ÷�Ӧ������Ӧ�����ƶ�����c��ȷ��
d��ѡ���Ч����������Ӧ���ʣ���ƽ�ⲻ�ƶ�����d����
�ʴ�Ϊ��c��
��5����Mn��s��+O2��g���TMnO2��s����H1=-520kJ/mol
��S��s��+O2��g���TSO2��g����H2=-297kJ/mol
��Mn��s��+S��s��+2O2��g���TMnSO4��s����H3=-1065kJ/mol
����-��-�ٿɵ�MnO2��s��+SO2��g��=MnSO4��s����H=-248kJ/mol��
�ʴ�Ϊ��MnO2��s��+SO2��g��=MnSO4��s����H=-248kJ/mol��
���� ���⿼�黯ѧƽ�ⳣ������ѧ��Ӧ���ʼ��㡢��ѧƽ��״̬���жϡ���������Է�Ӧ���ʼ���ѧƽ���ƶ���Ӱ�졢��˹���ɵ�֪ʶ���ۺ���ǿ���Ѷ����У�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 ʵ�����Ʊ��������ķ�Ӧԭ����ʵ��װ�����£�
ʵ�����Ʊ��������ķ�Ӧԭ����ʵ��װ�����£�
| ���� | ���۵�/�� | ���е�/�� | ���ܶ�/g•cm-3 | ���ܽ��� |
| ���� | ��5.5 | ��80 | ��0.88 | ������ˮ |
| �������� | ��5.7 | ��210.9 | ��1.205 | ��������ˮ |
| ����������� | ��89 | ��301 | ��1.57 | ������ˮ |
| ��Ũ���� | ��83 | ��1.4 | ��������ˮ | |
| ��Ũ���� | ��338 | ��1.84 | ��������ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | Na+ | Mg2+ | Cl- | SO42- |
| Ũ��/��g•L-1�� | 63.7 | 28.8 | 144.6 | 46.4 |


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

| ��ɫ��״̬ | �е㣨�棩 | �ܶȣ�g•cm-3�� | |
| ������* | ��ɫ��Ƭ״���� | 249 | 1.2659 |
| ���������� | ��ɫ����Һ�� | 212.6 | 1.05 |
| �Ҵ� | ��ɫ����Һ�� | 78.3 | 0.7893 |
| ������ | ��ɫ����Һ�� | 80.8 | 0.7318 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| R | T | |
| X | Y | Z |
| A�� | ��̬�⻯���ȶ��ԣ�Y��T | |
| B�� | R�ֱܷ���X��Z�γɹ��ۻ����� | |
| C�� | Rλ��Ԫ�����ڱ��еڶ����ڵ�VA�� | |
| D�� | ZԪ�ص�����������Ӧ��ˮ����Ļ�ѧʽΪHZO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
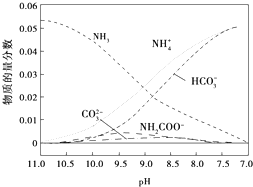
| A�� | ��pH=9.0ʱ��c��NH4+����c��HCO3-����c��NH2COO-����c��CO32-�� | |
| B�� | ��ͬpH����Һ�д��ڹ�ϵ��c��NH4+��+c��H+���T2c��CO32-��+c��HCO3-��+c��NH2COO-��+c��OH-�� | |
| C�� | ����ҺpH���Ͻ��͵Ĺ����У��к�NH2COO-���м�������� | |
| D�� | ����CO2��ͨ�룬$\frac{c��O{H}^{-}��}{c��N{H}_{3}•{H}_{2}O��}$�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ö��Ե缫��⺬��̪�ı���ʳ��ˮ������������Һ�ȱ�� | |
| B�� | ͭ�ĵ�⾫�������У���0.2 mol ���ӷ���ת��ʱ������һ����6.4 gͭ�ܽ� | |
| C�� | �����¸ֹ���ֱ����Դ��������������Ϊ��ӵ�Դ������������ | |
| D�� | �����Ի����У�ÿ����35.6 g���⣨Fe2O3•H2O�������ĵ�����Ϊ6.72 L����״���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 ���������һ����Ҫ�Ļ�ѧ�Լ�������Һ�����ȶ��������������»�ֽ����ɶ������̺������������Ի���������Һ�зֽ��ٶȺ���������ֽ��ٶȼӿ죮
���������һ����Ҫ�Ļ�ѧ�Լ�������Һ�����ȶ��������������»�ֽ����ɶ������̺������������Ի���������Һ�зֽ��ٶȺ���������ֽ��ٶȼӿ죮������������Һ�Ĵ���ÿ����Һ�������ͬ�� | ���������Һ��ɫ��ȥ��ʱ�� |
| �ȵ����1�� | 1min |
| ��ɫ���ٵ����2�� | 15s |
| ��ɫ���ٵ����3�� | 3s |
| ��ɫ���ٵ����4�� | 1s |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
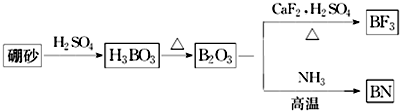
 �����Ʋ�1mol NH4BF4��������泥��к���2NA����λ����
�����Ʋ�1mol NH4BF4��������泥��к���2NA����λ����
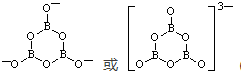 ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com