
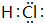 ,其中所含化学键的类型是共价键.
,其中所含化学键的类型是共价键.分析 A、B、C、D、E均为短周期元素,其原子序数依次增大.A的单质是最理想的燃料,则A为H元素;B的原子最外层电子数是次外层电子数的3倍,原子只能有2个电子层,最外层电子数为6,故B为O元素;B、D同主族,则D为S元素;C的焰色反应为黄色,则C为Na;E-与Ar具有相同的核外电子排布,则E为Cl.
解答 解:A、B、C、D、E均为短周期元素,其原子序数依次增大.A的单质是最理想的燃料,则A为H元素;B的原子最外层电子数是次外层电子数的3倍,原子只能有2个电子层,最外层电子数为6,故B为O元素;B、D同主族,则D为S元素;C的焰色反应为黄色,则C为Na;E-与Ar具有相同的核外电子排布,则E为Cl.
(1)A、B的元素符号分别是H、O,故答案为:H;O;
(2)A、E组成的化合物为HCl,电子式是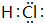 ,其中所含化学键的类型是共价键,故答案为:
,其中所含化学键的类型是共价键,故答案为: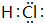 ;共价键;
;共价键;
(3)C、D两种元素的最高价氧化物的水化物的化学式分别是NaOH、H2SO4,故答案为:NaOH;H2SO4;
(4)同周期自左而右原子半径减小,故原子半径Na>S>Cl,故答案为:Na>S>Cl;
(5)将E的单质通入NaBr溶液中,发生反应的化学方程式是:Cl2+2NaBr=Br2+2NaCl,观察到的现象是:溶液由无色变为橙黄色,故答案为:Cl2+2NaBr=Br2+2NaCl;溶液由无色变为橙黄色.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,熟练掌握元素周期表与元素周期律,旨在考查学生对基础知识的巩固.


科目:高中化学 来源: 题型:选择题
| 选项 | 离子晶体 | 原子晶体 | 分子晶体 |
| A | NaOH | Ar | SO2 |
| B | H2SO4 | 石墨 | S |
| C | CH3COONa | 水晶 | 苯 |
| D | Ba(OH)2 | 金刚石 | 玻璃 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
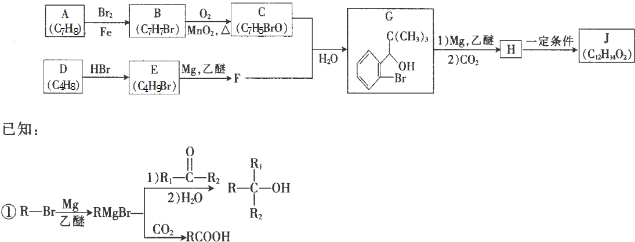
 .
.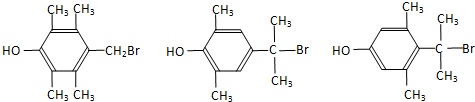 (写出一种即可).
(写出一种即可).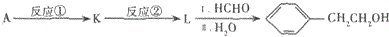
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(B)=0.8mol/(L•s) | B. | v(A)=0.6mol/(L•s) | C. | v(C)=0.9mol/(L•s) | D. | v(B)=1.0mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稳定性H2W<HZ | B. | 原子半径Y<Z | C. | 单质的还原性X<Y | D. | 最外层电子数Z<W |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
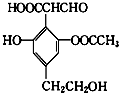
| A. | 该物质可以使酸性KMnO4溶液褪色,也可发生消去反应 | |
| B. | 可以与NaHCO3溶液反应放出CO2气体 | |
| C. | 可以与FeCl3溶液反应显色,也可与Ag(NH3)2OH反应 | |
| D. | 该物质可与H2反应,1mol该物质最多消耗5mol H2反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它与金刚石互为同素异形体 | |
| B. | 它与C60互称同分异构体 | |
| C. | 它与C60的物理性质与化学性质完全相同 | |
| D. | 它与13C互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 四 | ⑩ | ⑪ | ⑫ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com