
 £¬ŠĪ³É¹ż³Ģ
£¬ŠĪ³É¹ż³Ģ £»
£»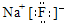 £¬ŠĪ³É¹ż³Ģ
£¬ŠĪ³É¹ż³Ģ £»
£» £¬ŠĪ³É¹ż³Ģ
£¬ŠĪ³É¹ż³Ģ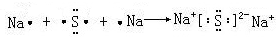 £»
£» £»
£» £¬ŠĪ³É¹ż³Ģ
£¬ŠĪ³É¹ż³Ģ £®
£® ·ÖĪö Ź×ĻČÅŠ¶Ļ»ÆŗĻĪļŹĒĄė×Ó»ÆŗĻĪļ»¹ŹĒ¹²¼Ū»ÆŗĻĪļ£»
ČōŹĒĄė×Ó»ÆŗĻĪļ£¬Ęäµē×ÓŹ½ ÓÉŅõ”¢ŃōĄė×ӵĵē×ÓŹ½×éŗĻ¶ų³É£¬ĻąĶ¬µÄĄė×Ó²»ÄÜŗĻ²¢£»
ČōŹĒ¹²¼Ū»ÆŗĻĪļ£¬Ęäµē×ÓŹ½ÓɶŌÓ¦Ō×ӵĵē×ÓŹ½×é³É£¬²¢ŅŖ±ķŹ¾³öĮ½Ō×ÓÖ®¼äµÄ¹²ÓƵē×Ó¶ŌĒéæö£®
ÓƵē×ÓŹ½±ķŹ¾Ąė×Ó»ÆŗĻĪļµÄŠĪ³É¹ż³Ģ£¬×ó±ßŠ“³É¼üŌ×ӵĵē×ÓŹ½£¬ĻąĶ¬µÄŌ×ÓæÉŅŌŗĻ²¢£¬ÓŅ±ßŠ“Ąė×Ó»ÆŗĻĪļµÄµē×ÓŹ½£¬ĻąĶ¬µÄĄė×Ó²»ÄÜŗĻ²¢£¬ÖŠ¼äÓĆ¼żŗÅĮ¬½Ó£¬×ó±ßÓĆĶä¼żĶ·±ķŹ¾µē×ӵĵƏ§£®
½ā“š ½ā£ŗ£Ø1£©H2OŹĒ¹²¼Ū»ÆŗĻĪļ£¬ŃõŌ×Ó·Ö±šÓėĮ½øöĒāŌ×ÓĶعżŅ»¶Ō¹²ÓƵē×Ó¶Ō½įŗĻ£¬µē×ÓŹ½ĪŖ £»
£»
H2OĪŖ¹²¼Ū»ÆŗĻĪļ£¬ø÷Ō×Ó“ļµ½ĪČ¶Ø½į¹¹£¬ÓƵē×ÓŹ½±ķŹ¾ŠĪ³É¹ż³ĢĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£» £»
£»
£Ø2£©·ś»ÆÄĘŹĒĄė×Ó»ÆŗĻĪļ£¬ÓÉ·śĄė×ÓÓėÄĘĄė×Ó¹¹³É£¬µē×ÓŹ½£ŗ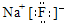 £»
£»
NaFĪŖĄė×Ó»ÆŗĻĪļ£¬ÓƵē×ÓŹ½±ķŹ¾ŠĪ³É¹ż³ĢĪŖ £»
£»
¹Ź“š°øĪŖ£ŗ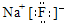 £»
£» £»
£»
£Ø3£©Na2SĪŖĄė×Ó»ÆŗĻĪļ£¬ÓÉĮņĄė×ÓÓėÄĘĄė×Ó¹¹³É£¬µē×ÓŹ½ĪŖ£ŗ £»
£»
Na2SĪŖĄė×Ó»ÆŗĻĪļ£¬ÓƵē×ÓŹ½±ķŹ¾ŠĪ³É¹ż³ĢĪŖ£ŗ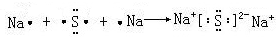 £»
£»
¹Ź“š°øĪŖ£ŗ £»
£»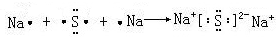 £»
£»
£Ø4£©H2ÖŠHŌ×Ó¼äŅŌ¹²¼Ū¼ü£¬¼“¹²ÓƵē×Ó¶Ō½įŗĻ£¬µē×ÓŹ½ĪŖ£ŗH£ŗH£»
H2ÖŠHŌ×Ó¼äŅŌ¹²¼Ū¼ü£¬ÓƵē×ÓŹ½±ķŹ¾ŠĪ³É¹ż³ĢĪŖ£ŗ £»
£»
¹Ź“š°øĪŖ£ŗH£ŗH£» £»
£»
£Ø5£©HClŹōÓŚ¹²¼Ū»ÆŗĻĪļ£¬Ō×Ó¼äŅŌ¹²ÓƵē×Ó¶Ō³É¼ü£¬µē×ÓŹ½ĪŖ £¬
£¬
HClĪŖ¹²¼Ū»ÆŗĻĪļ£¬ÓƵē×ÓŹ½±ķŹ¾ŠĪ³É¹ż³Ģ£ŗ £»
£»
¹Ź“š°øĪŖ£ŗ £»
£» £®
£®
µćĘĄ ±¾Ģāæ¼²éĮĖÓƵē×ÓŹ½µÄŹéŠ“ŅŌ¼°ÓƵē×ÓŹ½±ķŹ¾µ„ÖŹ”¢»ÆŗĻĪļŠĪ³É¹ż³Ģ£¬ĢāÄæÄѶČÖŠµČ£¬ŅŖĒóѧɜŹģĮ·ÕĘĪÕµē×ÓŹ½µÄøÅÄī¼°±ķŹ¾·½·Ø£¬×¢ŅāĄė×Ó»ÆŗĻĪļ”¢¹²¼Ū»ÆŗĻĪļµē×ÓŹ½µÄŠ“·Ø£®


 דŌŖ¼°µŚĻµĮŠ“š°ø
דŌŖ¼°µŚĻµĮŠ“š°ø Ķ¬²½°ĀŹżĻµĮŠ“š°ø
Ķ¬²½°ĀŹżĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | H2SO4 | B£® | CH2=CH2 | C£® | CH3COOH | D£® | CH3CH2OH |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
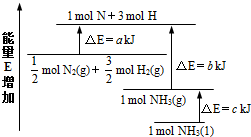 °±ĘųŹĒµŖŃ»·ÖŠµÄÖŲŅŖĪļÖŹ£¬ŌŚČĖĄąµÄÉś²śÉś»ī֊ӊ׏ć·ŗµÄÓ¦ÓĆ£®
°±ĘųŹĒµŖŃ»·ÖŠµÄÖŲŅŖĪļÖŹ£¬ŌŚČĖĄąµÄÉś²śÉś»ī֊ӊ׏ć·ŗµÄÓ¦ÓĆ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1mol/£ØL•s£© | B£® | 0.5mol/£ØL•s£© | C£® | 1.5 mol/£ØL•s£© | D£® | ĪŽ·Ø¼ĘĖć |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Čō²»æ¼ĀĒHClOŗĶH20µÄµēĄė£¬øĆČÜŅŗÖŠH+µÄÅضČĪŖ0.1mol/L | |
| B£® | ČōŌŚøĆČÜŅŗÖŠ¼ÓČė×ćĮæNa0H£¬ŌņæɵƵ½0.1molµÄNaClO | |
| C£® | Čō½«“ĖČÜŅŗŌŚĒæ¹āĻĀ¹āÕÕ£¬²śÉśĘųÅŻ£¬ŌņĘųÅŻÖ÷ŅŖ³É·ÖŹĒO2 | |
| D£® | “ĖČÜŅŗ¾ĆÖĆŗó£¬ÓÉÓŚHClOµÄ“óĮæ·Ö½ā£¬»įµ¼ÖĀĘäpHֵɿøß |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | H2SO4 | B£® | HCl | C£® | AgNO3 | D£® | NaOH |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
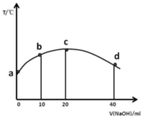 ČōĶł20ml 0.01mol/LCH3COOHČÜŅŗÖŠÖšµĪ¼ÓČėŅ»¶ØÅØ¶ČµÄÉÕ¼īČÜŅŗ£¬²āµÄČÜŅŗµÄĪĀ¶Č±ä»ÆČēĶ¼ĖłŹ¾£¬ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
ČōĶł20ml 0.01mol/LCH3COOHČÜŅŗÖŠÖšµĪ¼ÓČėŅ»¶ØÅØ¶ČµÄÉÕ¼īČÜŅŗ£¬²āµÄČÜŅŗµÄĪĀ¶Č±ä»ÆČēĶ¼ĖłŹ¾£¬ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | cµćŹ±£¬“×ĖįµÄµēĄė³Ģ¶ČŗĶµēĄė³£Źż¶¼×ī“ó£¬ČÜŅŗ³ŹÖŠŠŌ | |
| B£® | Čōbµć»ģŗĻČÜŅŗĻŌĖįŠŌ£¬Ōņ2c£ØNa+£©=c£ØCH3COO-£©+c£ØCH3COOH£© | |
| C£® | »ģŗĻČÜŅŗÖŠĖ®µÄµēĄė³Ģ¶Č£ŗb£¾c£¾d | |
| D£® | ÓÉĶ¼æÉÖŖ£¬øĆ·“Ó¦µÄÖŠŗĶČČĻČŌö“óŗó¼õŠ” |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com